ЭТАРА РЕАКЦИЯ, окисление метильной группы в ароматич. соед. в альдегидную под действием хромилхлорида (иногда к Э. р. относят любые р-ции в орг. химии с участием СrO2С12):
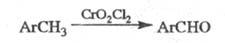
Ароматич. ядро может содержать заместитель:
Hal, NO2, Alk и АlkO (хотя две последние группы также могут
окисляться в ходе р-ции). Вместо СrО2С12 можно использовать
CrO2(OCOR)2 (R= CH3, С6Н5,
СС13), что способствует увеличению выхода.
Обычно хромилхлорид смешивают с ароматич.
соед. в среде инертного орг. р-рителя (CS2, ССl4,
СНС13, С6Н5С1 и др.) при 10-50 oС.
Образовавшийся комплекс состава АrСН3 x 2СrО2С12
(часто выпадает в осадок) обрабатывают Н2О. Выходы составляют
50-70%. Основные побочные продукты - хлорированные ароматич. соед. и продукты
более глубокого окисления.
Механизм Э. р. известен лишь в общих чертах.
Установлено, что стадия, определяющая скорость р-ции,- расщепление связи
С — Н в метильной группе при образовании аддукта с первой молекулой СrO2С12.
Полагают, что этот процесс может идти по ионному либо радикальному механизму,
давая в обоих случаях на первой стадии аддукт типа АrСН2—О —Сr(ОН)С12,
к-рый быстро присоединяет вторую молекулу хромилхлорида. Образующееся соед.
имеет, по-видимому, структуру АrСН[ОСr(ОН)С12]2.
В условиях Э. р. метилзамещенные алициклич.
соед. в присут. каталитич. кол-в олефинов (ок. 1%) дают соответствующие
альдегиды с выходом 25%.
При действии CrO2(OR)2
и циклич. олефины образуются линейные диальдегиды:
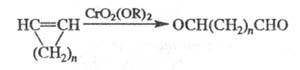
Э. р. используют в препаративной практике. Р-ция открыта А. Этаром в 1877.
Лит.: Грагеров И.П., Пономарчук М.П., "Ж. орган. химии", 1967, т. 3, № 3, с. 458-64; 1969, т. 5, № 6, с. 1145-47; Марч Дж., Органическая химия, пер. с англ., т. 4, М., 1988, с. 295-96; Наг ford W., "Chem. Вег.", 1958, Bd 58, S. 25; Nenitzescu C, "Bull. Soc. chim. France", 1968, p. 1349.
Г. И. Дрозд.


