ЭЛЕКТРОДЫ в электрохимии, электронно-проводящие фазы, контактирующие с ионным проводником (электролитом). Часто под Э. понимают лишь одну электронно-проводящую фазу. При пропускании тока от внеш. источника через систему из двух электродов, соединенных друг с другом через электролит, на Э. протекают два процесса: заряжение двойного электрического слоя и электрохим. р-ция. В отличие от фазовых контактов металл-металл, металл-полупроводник, полупроводник-полупроводник и т. п. на фанице фаз, составляющих электрохим. систему, вид носителей тока меняется, т. к. в электролите ток переносится ионами, а в электронно-проводящей фазе - электронами. Непрерывность прохождения тока через фаницу фаз в этом случае обеспечивается электродной р-цией. Э. наз. анодом, если на его пов-сти преобладает р-ция, приводящая к генерированию электронов, т. е. происходит окисление в-в, содержащихся в электролите, либо ионизация металла анода. Э. наз. катодом, если с его пов-сти электроны металла переходят на частицы реагирующих в-в, к-рые при этом восстанавливаются.
Классификация Э. проводится по природе
окислителей и восстановителей, к-рые участвуют в электродном процессе.
Э. 1-го рода наз. металл (или неметалл), пофуженный в электролит, содержащий
ионы этого же элемента. Металл Э. является восстановленной формой в-ва,
а его окисленной формой - простые или комплексные ионы этого же металла
(см. Электрохимическая кинетика). Напр., для системы Сu Сu2+ + 2е, где е - электрон, восстановленной формой является
Сu, а окисленной - ионы Сu2+. Соответствующее такому электродному
процессу Нернста уравнение для электродного потенциала Е имеет
вид:
Сu2+ + 2е, где е - электрон, восстановленной формой является
Сu, а окисленной - ионы Сu2+. Соответствующее такому электродному
процессу Нернста уравнение для электродного потенциала Е имеет
вид:
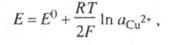
где E° - стандартный потенциал при
т-ре Т;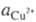 -
термодинамич.
активность ионов Сu2+; F - постоянная Фарадея; R -
газовая постоянная. КЭ. 1-го рода относятся амальгамные Э., т. к. для
них восстановленная форма - амальгама металла, а окисленная - ионы этого
же металла. Напр., для амальгамы таллия устанавливается равновесие: Tl+
+ e(Hg)
-
термодинамич.
активность ионов Сu2+; F - постоянная Фарадея; R -
газовая постоянная. КЭ. 1-го рода относятся амальгамные Э., т. к. для
них восстановленная форма - амальгама металла, а окисленная - ионы этого
же металла. Напр., для амальгамы таллия устанавливается равновесие: Tl+
+ e(Hg) Tl(Hg).
В такой системе могут изменяться концентрации и окисленной, и восстановленной
форм, поэтому ур-ние Нернста имеет вид:
Tl(Hg).
В такой системе могут изменяться концентрации и окисленной, и восстановленной
форм, поэтому ур-ние Нернста имеет вид:
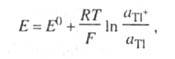
где aтl, - термодинамич. активность
таллия в амальгаме.
Э. 2-го рода- системы из металла М, покрытого
слоем его же труднорастворимой соли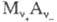 (или оксида) и погруженного в р-р, содержащий анионы этой соли (для оксида
-ионы ОН-). Окисленной формой является соль
(или оксида) и погруженного в р-р, содержащий анионы этой соли (для оксида
-ионы ОН-). Окисленной формой является соль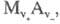 а восстановленная форма представлена металлом М и анионом Az-:
а восстановленная форма представлена металлом М и анионом Az-:

где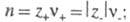 z
- зарядовое число иона. В системе устанавливается равновесие между
атомами М и анионами Az-в р-ре, к-рое включает два "парциальных"
равновесия: между металлом и катионом соли и между анионом соли в ее твердой
фазе и анионом в р-ре. Такие Э. наз. обратимыми по аниону.
z
- зарядовое число иона. В системе устанавливается равновесие между
атомами М и анионами Az-в р-ре, к-рое включает два "парциальных"
равновесия: между металлом и катионом соли и между анионом соли в ее твердой
фазе и анионом в р-ре. Такие Э. наз. обратимыми по аниону.
Ур-ние Нернста имеет вид:
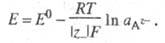
К Э. 2-го рода относятся многие электроды
сравнения, напр. каломельный, хлорсеребряный, оксидно-ртутный.
Э. 3-го рода- системы из металла, контактирующего
с двумя труднорастворимыми солями. В результате электрохим. р-ции на Э.
менее растворимая соль превращается в более растворимую, а потенциал Э.
определяется термодинамич. активностью катионов более растворимой соли.
Так, в системе Рb2+| РbС12, AgCl, процесс Ag происходит
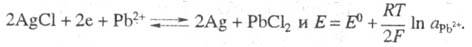
Металл Э. может не участвовать в р-циях,
а служить лишь передатчиком электронов от восстановленной формы в-ва к
окисленной; такие Э. наз. окислительно-восстановительными или редокс-электродами.
Напр., платиновый Э. в р-ре, содержащем ионы [Fe(CN)6]4-
и [Fe(CN)6]3-, осуществляет перенос электронов между
этими ионами в качестве передатчика (медиатора). Среди окислит.-восстановит.
Э. выделяют газовые Э., состоящие из химически инертного металла (обычно
Pt), к к-рому подводится электрохимически активный газ (напр., Н2
или С12). Молекулы газа адсорбируются на пов-сти металла, распадаясь
на адсорбиров. атомы, к-рые непосредственно участвуют в переносе электронов
через границу раздела фаз. Наиб. распространен водородный Э.,на пов-сти
к-рого образуются адсорбир. атомы Надс и устанавливается равновесие:
Н2 2Надс
2Надс 2Н+ + 2е. Разл. типы Э. можно объединить в рамках т. наз. концепции
электронного равновесия на границе металл-электролит, согласно к-рой каждому
равновесному электродному потенциалу соответствует определенная термодинамич.
активность электронов в электролите.
2Н+ + 2е. Разл. типы Э. можно объединить в рамках т. наз. концепции
электронного равновесия на границе металл-электролит, согласно к-рой каждому
равновесному электродному потенциалу соответствует определенная термодинамич.
активность электронов в электролите.
Э. наз. идеально поляризуемым, если вследствие
термодинамич. или кинетич. причин переход электронов через межфазную границу
невозможен. При изменении потенциала такого Э. происходит только изменение
строения двойного электрич. слоя, что сопровождается протеканием тока заряжения,
спадающего до нуля, когда перестройка двойного электрич. слоя заканчивается
(см. Ток обмена). Для неполяризуемых, или обратимых, Э. переход
электронов через границу фаз, напротив, незаторможен, и при пропускании
тока через такой Э. его потенциал практически не изменяется.
По функциям в электрохим. системе Э. подразделяют
на рабочие, вспомогательные и электроды сравнения. Рабочим наз. Э., на
к-ром происходит исследуемый электрохим. процесс. Вспомогат. Э. (или противоэлектрод)
обеспечивает возможность пропускания тока через электрохим. ячейку, а Э.
сравнения - возможность измерения потенциала рабочего Э. Специфика широко
используемых в электрохимии жидких Э. (ртуть, амальгамы, галлий, жидкие
сплавы на основе Ga -галламы, расплавы металлов и т. п.) связана с идеальной
гладкостью их пов-сти, истинная площадь к-рой совпадает с ее геом. величиной,
а также с энергетич. однородностью и изотропностью св-в пов-сти Э. и возможностью
растворения выделяющихся металлов в материале Э.
На практике Э. классифицируют по хим.
природе материала (металлические, неметаллические, оксидные, Э. из соед.
с ковалентной связью, углеграфитовые и т.д.), форме (сферические, плоские,
цилиндрические, дисковые и т. д.), условиям функционирования (неподвижные,
вращающиеся и т. п.), размерам (микро- и ультрамикроэлектроды), пористости,
гидрофильности, участию электродного материала в электродном процессе (расходуемые
и нерасходуемые) и др. признакам. Использование капельного ртутного электрода
лежит в основе полярографии. Вращающийся дисковый электрод представляет
интерес как система, для к-рой существует строгое решение диффузионной
кинетич. задачи. К особо практически важным Э. следует отнести каталитически
активные и высоко коррозионностойкие оксидные рутениево-титановые аноды
(ОРТА), применение к-рых революционизировало самое широкомасштабное электрохим.
произ-во - электролитич. получение хлора и щелочей.
Модифицирование Э., получившее широкое распространение в электрокатализе, произ-ве химических источников тока, электрохимических сенсоров и т. п., основано как на физических (ионная имплантация, разрыхление пов-сти, выращивание монокристаллич. граней, создание монокристаллич. структур, физ. адсорбция ионов и молекул и др.), так и хим. методах. В частности, химически модифицированные Э. представляют собой проводящий или полупроводниковый материал, покрытый мономолекулярными (в т. ч. субатомными), полимолекулярными, ионными, полимерными слоями, в результате чего Э. проявляет хим., электрохим. и/или оптич. св-ва слоя. Хим. модифицирование достигается хемосорбцией на пов-сти Э. ионов и молекул, ковалентным связыванием разл. агентов с поверхностными атомными группами, покрытием пов-сти орг., металлорг. или неорг. полимерными слоями, созданием композитов из электродного материала и в-ва -модификатора.
Микроэлектроды имеют по крайней
мере один из размеров настолько малый, что св-ва Э. оказываются размерно
зависимыми. Размеры микроэлектродов лсжат в интервале 0,1-50 мкм, миним.
площадь составляет 10-14 м2 (ультрамикроэлектроды),
тогда как в большинстве электроаналит. экспериментов применяют Э. с площадью
5 х 10-5м2, в лаб. электросинтезе - 10-2
м2. Осн. преимущество микроэлектродов - возможность снизить
с их помощью диффузионные ограничения скорости электродного процесса и,
следовательно, изучать кинетику очень быстрых электродных р-ций. Из-за
малой величины токов электрохим. ячейки с микроэлектродами характеризуются
незначительным омич. падением потенциала, что позволяет изучать системы
с высокими концентрациями реагирующих частиц, обычно используемые в технол.
процессах, применять высокие скорости сканирования потенциала при вольтамперометрич.
измерениях, проводить работы в плохо проводящих средах и т. п. Микроэлектроды
используют для анализа ультрамалых проб, исследования процессов в живых
организмах, в клинич. целях. Ультрамикроэлектроды применяют в туннельной
сканирующей микроскопии и в электрохим. нанотехнологии.
См. также Ионоселективные электроды,
Псевдоожиженный электрод, Суспензионный электрод.
Лит.: Дамаскин Б.Б., Петрий О. А., Электрохимия, М., 1987; Багоцкий B.C., Основы электрохимии, М., 1988.
О.А. Петрий.


