ШТИГЛИЦА РЕАКЦИЯ (перегруппировка Штиглица), превращение триарилметилгидроксиламинов в анилы (имины, у к-рых с атомом N связан Аr) под действием пентахлорида фосфора
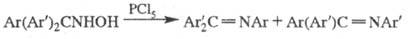
Гидроксиламины могут содержать в качестве
заместителей в ароматич. ядре Alk, Alk2N, AlkO, Hal и NO2.
Электронодонорные заместители облегчают Ш. р. Способность арила к миграции
уменьшается в ряду: R2NC6H4 > ROC6H4
> RC6H4 > O2NC6H4
(заместители в пара-положении).
Обычно смесь гидроксиламина и РС15
в инертном орг. р-рителе (напр., эфире или бензоле) выдерживают 1-2 ч при
комнатной т-ре и затем ок. 1 ч при кипячении. Выходы, как правило, высокие.
Механизм Ш. р. не изучен. Предполагают,
что на начальной стадии образуется эфир Аr(Аr)2CNHOPC14,
к-рый в результате синхронных процессов миграции связей и выброса уходящей
группы (возможно, НОРСl4) дает в итоге анил, РОС13 и
НС1.
Аналогичную перегруппировку претерпевают
тритил-N-гaлогенамины под действием оснований, а также тритилазиды при
нагр. (механизм последней р-ции сходен с механизмом перегруппировки Курциуса;
см. Курциуса реакция):
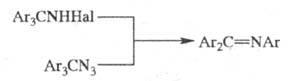
Иногда эти две р-ции также наз. Ш. р. Ш. р. используют в препаративной практике, открыта И. Штиглицом в 1913.
Лит.: Mapч Дж., Органическая химия, пер. с англ., т. 4, М., 1988, с. 163-64; Mayo P. (ed.), Molecular rearrangement, N. Y.- L., 1963, p. 479; Коvaciс P. [a. o.], "Chem. Rev.", 1970, v. 70, № 6, p. 664.
Г. И. Дрозд.


