ХИНОЛИЗИДИН (октагидрохинолизин,
норлупинин), мол. м. 139,24; бесцв. жидкость; т. кип. 169-170 °С,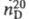 1,4796.
Хорошо раств. в воде и орг. р-рителях.
1,4796.
Хорошо раств. в воде и орг. р-рителях.
X. - сильное основание, рКа9,37.
С HHal, пикриновой и платинохлористоводородной к-тами образует устойчивые
соли (т. пл. пикрата 137 °С, хлороплатината - 114 °С).
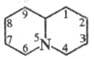
X. обладает св-вами третичных циклич. аминов. При действии СН3I X. превращается в соль транс-5-метилхинолизидиния:
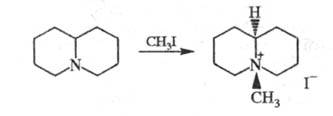
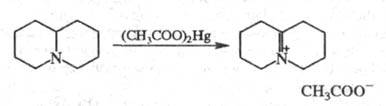
Обработка X. ацетатом Hg приводит к дегидрированию цикла с образованием иммониевой соли:
X. и его производные - осн. структурные
фрагменты хинолизидиновых алкалоидов групп лупинина, нуфарина, цитизина,
спартеина и матрина, входит также в состав нек-рых индольных, изохинолиновых
и др. алкалоидов.
X. получают декарбоксилированием лупиновой
к-ты, выделенной из растений рода Lupinus (семейство Leguminosae), путем
перегонки ее со смесью Са(ОН)2 и NaOH или из метилового эфира
этой к-ты по р-циям:
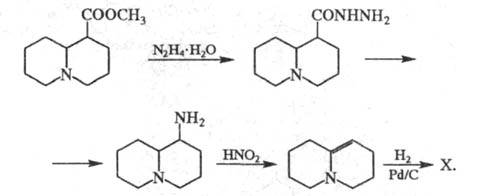
Осн. методы синтеза из соединений др. рядов:
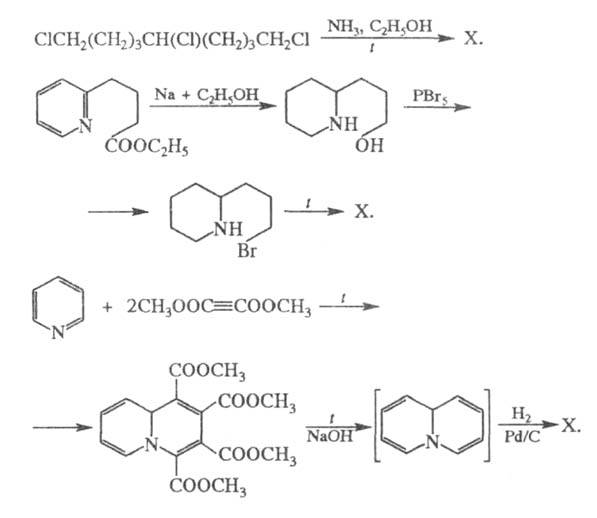
Нек-рые производные X.- лек. препараты (напр., пахикарпин, цитизин); многие производные токсичны.
Лит.: Садыков С.А., Асланов Х.А., Кушмурадов Ю. К., Алкалоиды хинолизидинового ряда, Химия, стереохимия, биогенез, М., 1975; Общая органическая химия, пер. с англ., т. 8, М., 1985, с. 286.
В. И. Келарев.


