ФОТОХИМИЯ, наука
о хим. превращениях в-в под действием электромага, излучения - ближнего ультрафиолетового
(~ 100-400 нм), видимого (400-800 нм) и ближнего инфракрасного (0,8 - 1,5 мкм).
Исследования хим. действия
излучения на разл. в-ва и попытки его теоретич. истолкования начинаются с кон.
18 в., когда Дж. Сенеби высказал предположение о том, что необходимая для достижения
определенного хим. эффекта продолжительность действия света обратно пропорциональна
его интенсивности.
В 19 в. параллельно происходило открытие новых р-ций орг. и неорг. в-в под действием
света и физ.-хим. исследование механизма и природы фотохим. р-ций. В 1818 T.
Гротгус отверг гипотезу о тепловом действии света, предположил аналогию в воздействии
на в-во света и электричества и сформулировал принцип, согласно к-рому причиной
хим. действия м. о. только тот свет, к-рый поглощается в-вом (закон Гротгуса).
Дальнейшими исследованиями было установлено, что кол-во продукта фотохим. р-ции
пропорционально произведению интенсивности излучения на время его действия (P.
Бунзен и Г. Роско, 1862) и что необходимо учитывать интенсивность только поглощенного,
а не всего падающего на в-во излучения (Я. Вант-Гофф, 1904). Одно из важнейших
достижений Ф.- изобретение фотографии (1839), основанной на фотохим. разложении
галогенидов серебра.
Принципиально новый этап
в развитии Ф. начался в 20 в. и связан с появлением квантовой теории и развитием
спектроскопии. А. Эйнштейн (1912) сформулировал закон квантовой эквивалентности,
согласно к-рому каждый поглощенный в-вом фотон вызывает первичное изменение
(возбуждение, ионизацию) одной молекулы или атома. Вследствие конкуренции хим.
р-ций возбужденных молекул и процессов их дезактивации, а также обратного превращения
нестабильных первичных продуктов в исходное в-во, хим. превращения претерпевает,
как правило, лишь нек-рая доля возбужденных молекул. Отношение числа претерпевших
превращение молекул к числу поглощенных фотонов наз. квантовым выходом фотохим.
р-ции. Квантовый выход, как правило, меньше единицы; однако в случае, напр.,
цепных р-ций он может во много раз (даже на неск. порядков) превышать единицу.
В России важное значение
имели в нач. 20 в. работы П.П. Лазарева в области фотохимии красителей и кинетики
фотохим. р-ций. В 40-е гг. А.Н. Терениным была высказана гипотеза о триплетной
природе фосфоресцентного состояния, играющего важную роль в фотохим. р-циях,
и открыто явление триплет-триплетного переноса энергии, составляющее основу
одного из механизмов фотосенсибили-зации хим. р-ций.
Использование достижений
квантовой химии, спектроскопии, хим. кинетики, а также появление новых эксперим.
методов исследования, в первую очередь методов изучения очень быстрых (до 10-12
с) процессов и короткоживущих промежут. в-в, позволило развить детальные представления
о законах взаимод. фотонов с атомами и молекулами, природе возбужденных электронных
состояний молекул, механизмах фотофиз. и фотохим. процессов. Фотохим. р-ции
протекают, как правило, из возбужденных электронных состояний молекул, образующихся
при поглощении фотона молекулой, находящейся в основном (стабильном) электронном
состоянии. Если интенсивность света очень велика [более 1020 фотонов/
(с·см2)], то путем поглощения двух или более фотонов могут заселяться
высшие возбужденные электронные состояния и наблюдаются двух- и многофотонные
фотохим. р-ции (см. Двухквантовые реакции, Многофотонные процессы). Возбужденные
состояния не являются лишь "горячей" модификацией их основного состояния,
несущей избыточную энергию, а отличаются от основного состояния электронной
структурой, геометрией, хим. св-вами. Поэтому при возбуждении молекул происходят
не только количественные, но и качеств, изменения их хим. поведения. Первичные
продукты р-ций возбужденных молекул (ионы, радикалы, изомеры и т.п.) чаще всего
являются нестабильными и превращаются в конечные продукты в результате серии
обычных термич. хим. ф-ций.
Для качеств. и количеств.
исследования продуктов используют всевозможные аналит. методы, в т. ч. оптич.
спектроскопию и радиоспектроскопию. Для определения дозы облучения и квантовых
выходов применяют актинометрию. Св-ва короткоживущих возбужденных состояний
обычно изучают методами оптич. эмиссионной (флуоресцентной и фосфоресцентной)
и абсорбционной спектроскопии. Особенно важное значение для исследования механизмов
фотохим. р-ций имеют
импульсные методы: импульсный фотолиз, лазерная спектроскопия и др. (см.
Люминесцентный анализ). Эти методы позволяют изучать кинетику первичных
р-ций возбужденных молекул, нестабильные промежуг. продукты и кинетику их превращений.
Фотохим. методы применяют и для исследования обычных термич. р-ций радикалов,
ионов и др. промежут. в-в. Важную информацию о механизмах Ф. дают радиоспек-троскопич.
методы, основанные на динамич. поляризации ядер и электронов (см. Химическая
поляризация ядер).
В совр. Ф. выделяют след.
разделы: Ф. малых молекул, позволяющую выяснить динамику элементарного акта
в возбужденных электронных состояниях молекул; орг. и неорг. Ф., изучающие фотопревращения
соответствующих хим. со-ед. и методы фотохим. синтеза; механистич. (физ.) Ф.,
изучающую механизмы и кинетич. закономерности фотохим. р-ций и тесно связанная
с фотофизикой, хим. кинетикой, квантовой химией, теорией строения молекул и
др. разделами физ. химии.
Важные практич. применения
Ф. связаны с фотографией, фотолитографией и др. процессами записи и обработки
информации, пром. и лаб. синтезом орг. и неорг. в-в (фото-нитрозирование циклогексана
с целью получения капролак-тама, синтез витаминов группы D, напряженных
полициклич. структур и др.), синтезом и модификацией полимерных материалов (фотополимеризация,
фотомодификация и фотодеструкция полимеров), квантовой электроникой (фотохим.
лазеры, затворы, модуляторы), микроэлектроникой (фоторезисты), преобразованием
солнечной энергии в химическую.
Фотохим. процессы играют
очень важную роль в природе. Биол. фотосинтез обеспечивает существование
жизни на Земле. Подавляющую часть информации об окружающем мире человек и большинство
животных получают посредством зрения, основанного на фотоизомеризации родопсина,
к-рая запускает цепь ферментативных процессов усиления сигнала и тем самым
обеспечивает чрезвычайно высокую чувствительность вплоть до регистрации отдельных
фотонов. Озон образуется в верх. слоях атмосферы из кислорода под действием
коротковолнового (<180 нм) излучения Солнца по р-ции: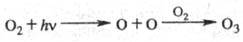
Он поглощает излучение
Солнца в области 200-300 нм, губительно действующее на живые организмы.
Лит.: Теренин А.Н.,
Фотоника молекул красителей и родственных органических соединений, Л., 1967;
Барлтроп Дж., Койл Дж., Возбужденные состояния в органической химии, пер. с
англ., M., 1978; Окабе X., Фотохимия малых молекул, пер. с англ., M., 1981;
Бугаенко Л.Т., Кузьмин М.Г., П о л а к Л.С., Химия высоких энергий, M.,
1988. М.Г. Кузьмин.


