ФОСФОРА ГАЛОГЕНИДЫ,
тригалогениды PX3, пентагало-гениды PX5 (X = F, Cl, Br),
смешанные галогениды, напр. PClF2, PCl2F3,
окси- POX3 и тиогалогениды PSX3, низшие галогениды - галогениды
P(II), напр. P2Cl4, P2I4. Св-ва
Ф. г. приведены в табл. PCl3, PBr3, POCl3,
PSCl3, P2Cl4 - бесцв. жидкости; PI3
- красные кристаллы гексаген, сингонии; PCl5 - бесцв. зеленоватые
кристаллы тетрагон. сингонии; POBr3 -бесцв. кристаллы; PBr5
- красновато-желтые кристаллы ром-бич, сингонии; P2I4
- оранжевые кристаллы триклинной сингонии, т.пл. 126,1 0C, плотн.
4,18 г/см3; остальные - бесцв. газы. Молекулы Ф. г. сравнительно
малополярны.
СВОЙСТВА НЕКОТОРЫХ ГАЛОГЕНИДОВ
ФОСФОРА
|
Соединение |
Т.пл., 0с |
T. кип., 0с |
Плотн., г/см3 |
Дж/(моль •К)а |
кДж/моль |
Дж/(моль·К) |
||
|
PF3 |
-151,5 |
-101,5 |
3,907 г/л |
58,69 |
-957,4 |
272,95 |
||
|
PCl3 |
-90,34 |
75,3 |
1,57 |
71,59 |
-289,5 |
311,60 |
||
|
PBr3 |
-40,5 |
175,3 |
2,87 |
— |
-175,7б |
57,4б |
||
|
PI3 |
61,0 |
Разлагается |
3,89 |
— |
-46,0в |
— |
||
|
PF5 |
-93,75 |
-84,55г |
5,805 г/л |
84,70 |
-1593,3 |
300,92 |
||
|
PCl5 |
160 |
159г |
2,11 |
113,32 |
-376,0 |
367,11 |
||
|
PBr5 |
— |
106 (с разл.) |
3,57 |
— |
-230,0в |
— |
||
|
PFCl4 |
-60,0 |
— |
— |
107,85 |
-646,1 |
357,89 |
||
|
PClF4 |
-132 |
— |
— |
93,0 |
-1365,0 |
326,76 |
||
|
PCl2F3 |
-125 |
10 |
5,4 г/л |
97,35 |
-1122,1 |
335,33 |
||
|
PBr2F3 |
-20 |
— |
— |
— |
— |
— |
||
|
POF3 |
39,8 |
-40,15 |
3,7д |
68,87 |
-1252,0 |
285,31 |
||
|
POCl3 |
1,18 |
107,2 |
1,65 . |
84,35 |
-568,4 |
324,5 |
||
|
POBr3 |
55,0 |
192 |
2,82 |
— |
-479,5в |
— |
||
|
PSCl3 |
-36,2 ( |
125 |
1,63 |
|
|
|
||
|
P2Cl4 |
-28,0 (с разл.) |
— |
— |
— |
— |
— |
||
|
P2I4 |
126,1 |
— |
4,18 |
— |
— |
— |
||
а Для
газа. б Для жидкости. в Для кристаллов.г
Т-ра возгонки.д Относительно воздуха.
Молекулы PX3
имеют конфигурацию тритон, пирамиды с атомом P в вершине. Длина связи P — X
меняется от 0,155 нм для PF3 до 0,255 нм для PI3, угол
XPX ~ 100°. Полярность молекул падает при переходе от PF3 к PI3,
т-ра плавления растет в результате увеличения межмол. взаимодействия. Трихлорид
PCl3 дымит во влажном воздухе (из-за гидролиза с выделением HCl),
энергично взаимод. с водой, образуя фосфористую и соляную к-ты. Хорошо раств.
в диэтиловом эфире, бензоле, CHCl3, CS2, CCl4.
Получают пропусканием Cl2 в р-р белого P в CS2 или сжиганием
P в атмосфере сухого Cl2. Применяют для получения PCl5,
POCl3, PSCl3, фосфор-орг. соед., в произ-ве красителей,
лек. ср-в, инсектицидов (эфиры тиофосфорных к-т) и ПАВ. Токсичен, ПДК 0,2 Мг/м3.
Молекулы пентахлорида PCl5,
находящегося в жидком или газообразном состоянии, имеют конфигурацию три-гон.
бипирамиды с атомом P в основании. Расстояния Cl-Cl в основании бипирамиды 0,308
нм, длина экваториальной связи P-Cl 0,21 нм, апикальной - 0,225 нм. Твердый
PCl5 построен из тетраэдрич. ионов 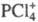 и октаэдрических
и октаэдрических 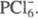 Длина связей P — Cl в тетраэдре 0,197 нм, в октаэдре 0,204 нм (экваториальные)
и 0,208 нм (апикальные). В парах выше 300 0C полностью разлагается
на PCl3 и Cl2, DH р-ции 129,7 кДж/моль. Гидролизуется
водой сначала до POCl3, затем до H3PO4. Лучший
р-ритель для PCl5- CCl4, раств. также в CS2.
При взаимод. PCl5 с NH4Cl получается фосфонитрил-хлорид
PNCl2, образующий при 120-150 0C циклич. тример, к-рый
выше 300 0C дает неорг. полимер (Cl2P = N)n
(см. Полифосфазены). Получают PCl5 взаимод. PCl3
с избытком Cl2, а также пропусканием Cl2 в р-р PCl3
в CS2. PCl5 -хлорирующий агент, его используют при получении
хлоран-гидридов фосфорных к-т, фосфоновых к-т из олефинов, в произ-ве лек. ср-в
и красителей. Токсичен, ПДК 0,2 мг/м3.
Длина связей P — Cl в тетраэдре 0,197 нм, в октаэдре 0,204 нм (экваториальные)
и 0,208 нм (апикальные). В парах выше 300 0C полностью разлагается
на PCl3 и Cl2, DH р-ции 129,7 кДж/моль. Гидролизуется
водой сначала до POCl3, затем до H3PO4. Лучший
р-ритель для PCl5- CCl4, раств. также в CS2.
При взаимод. PCl5 с NH4Cl получается фосфонитрил-хлорид
PNCl2, образующий при 120-150 0C циклич. тример, к-рый
выше 300 0C дает неорг. полимер (Cl2P = N)n
(см. Полифосфазены). Получают PCl5 взаимод. PCl3
с избытком Cl2, а также пропусканием Cl2 в р-р PCl3
в CS2. PCl5 -хлорирующий агент, его используют при получении
хлоран-гидридов фосфорных к-т, фосфоновых к-т из олефинов, в произ-ве лек. ср-в
и красителей. Токсичен, ПДК 0,2 мг/м3.
Молекула оксихлорида POCl3
имеет форму искаженного тетраэдра с атомом P в центре; 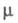 8,01· 10-30 Кл·м.. Полярный р-ритель, подвергается самоионизации
(POCl3
8,01· 10-30 Кл·м.. Полярный р-ритель, подвергается самоионизации
(POCl3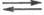 POCl+2+ С1-), раств. неорг. соли, напр. NaCl,
NH4Cl. Хорошо раств. в бензоле, CHCl3, CCl4,
CS2. Сильно дымит во влажном воздухе, гидролизуется водой до H3PO4.
Получают пропусканием O2 через PCl3 при 20-50 0C,
взаимод. PCl5 с P2O5 или H2C2O4.
Применяют для получения инсектицидов, орг. фосфатов H3PO4,
в частности трибутилфосфата. Токсичен, ПДК в воздухе рабочей зоны 0,05
мг/м3.
POCl+2+ С1-), раств. неорг. соли, напр. NaCl,
NH4Cl. Хорошо раств. в бензоле, CHCl3, CCl4,
CS2. Сильно дымит во влажном воздухе, гидролизуется водой до H3PO4.
Получают пропусканием O2 через PCl3 при 20-50 0C,
взаимод. PCl5 с P2O5 или H2C2O4.
Применяют для получения инсектицидов, орг. фосфатов H3PO4,
в частности трибутилфосфата. Токсичен, ПДК в воздухе рабочей зоны 0,05
мг/м3.
Тиохлорид PSCl3
по св-вам близок к POCl3; получают взаимод. S с PCl3 в
автоклаве в присут. AlCl3. Используют в произ-ве инсектицидов (эфиры
тиофосфорных к-т).
Фториды и бромиды P получают
из простых в-в, PF5 применяют в произ-ве фторофосфатов, как ингибитор
коррозии металлов в среде N2O4.
Лит.: Везер В.-Дж.,
Фосфор и его соединения, пер. с англ., M., 1962; У га и Я. А., Неорганическая
химия, M., 1989. Я. А. Угай.



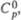
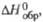
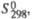
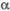 -форма)
-40,8 (b)
-форма)
-40,8 (b)