ФОСФИНОВЫЕ КИСЛОТЫ,
соед. общей ф-лы R2P(O)OH, где R - орг. радикал. Соли и эфиры Ф.
к. наз. фосфинатами. За редким исключением (напр., при R = CF3)
Ф. к.- кристал-лич. в-ва. Низшие Ф. к. хорошо раств. в воде, с увеличением мол.
м. R р-римость в воде снижается и возрастает р-римость в орг. р-рителях. Для
алифатич. и ароматич. Ф. к. значения рКа в H2O
2,3-3,5 (в 80%-ном этаноле примерно на две единицы выше). К-та (CF3)2P(O)OH
одна из наиб. сильных рКа<1).
В спектре ЯМР 31P
хим. сдвиги для Ф. к. находятся в области 22-75 м.д., полоса поглощения в ИК
спектре связи P = O- в области 1140-1210 см -1.
При 400 0C Ф.
к. дегидратируются с образованием ангидридов; при обработке Ф. к. диазоалканами,
триалкилфосфитами или спиртами в присут. катализаторов (карбодиимидов, фе-ниларсоновой
к-ты и др.) образуются полные эфиры; при действии COCl2, SOCl2
или PCl5 в эквимолярных кол-вах образуются хлорангидриды, с избытком
PCl5 или SF4 - диор-ганилтригалогенфосфораны. Разрыв связей
P — С наблюдается
при действии щелочи на Ф. к. с пергалогеналкильными радикалами. Восстановители
превращают Ф.к. в фосфины. Известны многочисленные р-ции Ф.к., сопровождающиеся
модификацией орг. радикала, а также алкилирование и аци-лирование группы НО.
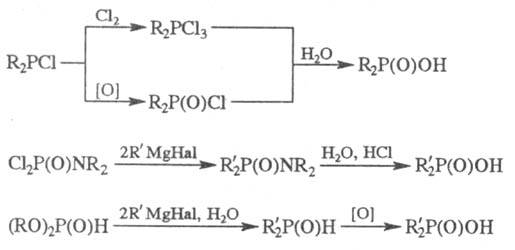
Ф. к. с незамещенными алкильными
и арильными радикалами обычно получают из диорганилхлорфосфинов, амидо-дихлорфосфатов
или диорганилфосфитов:
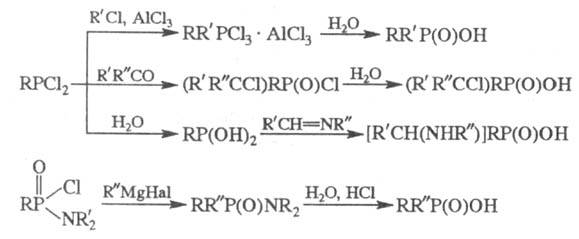
Ф. к. с разноименными орг.
радикалами можно получать по схеме:
Ф.к. образуются также в
р-ции H3PO2 с олефинами, при окислении R2P(S)SH,
диорганилдифосфиндисульфидов и вторичных фосфинов; в результате присоединения
фосфонистой и органилфосфонистых к-т к альдегидам и кетонам. Р-ция H3PO2
с альдегидами и вторичными аминами приводит к a-аминоалкилзамещенным Ф. к.,
напр.:

Ф. к. используют в лаб.
практике.
Лит.: Нифантьев
Э.E., Химия фосфорорганических соединений, M., 1971, с. 260-72; Crofts Р., в
кн.: Organic phosphorus compounds, eds. G. Koso-lapoff, L. Maier, v. 6,
N. Y., 1973, p. 1-209. G. И. Дрозд.


