ТРИФТОРНАДУКСУСНАЯ КИСЛОТА
(перокситрифторуксусная к-та)
CF3C(O)OOH, мол. м. 130,03; устойчива только в р-рах CF3COOH
или инертных р-рителей (CH2Cl2, CHCl3 и др.).
По кислотности намного слабее CF3COOH (рКа 3,7).
Высокоэффективный селективный
окислитель. При взаимод. с ненасыщ. соединениями в кислой среде образует монотрифторацетилпроизводные
1,2-гликолей, в буферных р-рах
Na2CO3, NaHCO3, Na2HPO4
- эпоксиды:
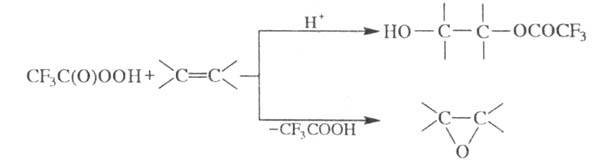
Нек-рые алкены в присут.
BF3 окисляются T. к. до кетонов, ароматич. углеводороды - до соответствующих
фенолов и хинонов, напр.:
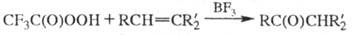
Алифатич. и ароматич. альдегиды
под действием Т.к. превращ. в соответствующие к-ты, кетоны - в эфиры (см. Байера
— Виллигера реакция). Первичные амины и оксимы окисляются до нитросоед.,
2,5-дизамещенные пиридины -до N-оксидов.
Безводные р-ры T. к. получают
действием 90%-ной H2O2 на (CF3CO)2O
в CH2Cl2, водные - смешиванием 90%-ной или 30%-ной H2O2
с CF3COOH.
Осн. применение T. к.-
окислитель в орг. синтезе.
При попадании на кожу или
слизистые оболочки Т.к. вызывает глубокие, долго не заживающие ожоги. Конц.
р-ры Т.к. при наф. с орг. в-вами могут взрываться.
Лит.: Физер Л.,
Физер M., Реагенты для органического синтеза, пер. с англ., т. 3, M., 1970,
с. 422-31; Xe йн с А., Методы окисления органических соединений, пер. с англ.,
M., 1988, с. 115-16, 154-55. И. И. Крылов.


