ТИОФЕНОЛ (фенилмеркаптан,
меркаптобензол) C6H5SH, мол. м. 110,18; бесцв. жидкость
с неприятным запахом; т. пл. -14,8°С, т. кип. 168,7 °С, 70°С/16
мм рт. ст.; 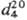 1,0766;
1,0766; 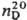 1,5893;
1,5893;
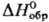 -111,42 кДж/моль,
-111,42 кДж/моль,
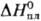 104,25 кДж/кг;
104,25 кДж/кг;
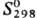 337,52 Дж/(моль · К);
337,52 Дж/(моль · К); 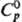 105,52 Дж/(моль · К); m 4,436·10-30Кл·м;
рКа 9,55 (25 °С, метанол). Т. не раств. в воде, смешивается
во всех соотношениях с большинством орг. р-рителей.
105,52 Дж/(моль · К); m 4,436·10-30Кл·м;
рКа 9,55 (25 °С, метанол). Т. не раств. в воде, смешивается
во всех соотношениях с большинством орг. р-рителей.
По хим. св-вам Т.- типичный
представитель тиолов. Легко образует устойчивые соли щелочных и тяжелых
металлов, особенно характерны хорошо кристаллизующиеся ртутные соли (напр.,
C6H5SHgCl); вступает в р-ции нуклеоф. замещения и присоединения
к кратным связям; при стоянии на воздухе или при действии иода окисляется до
дифенилди-сульфида (р-цию с иодом используют для количеств. определения Т.);
окисление в жестких условиях приводит к бен-золсульфокислоте; с Сl2
или Вr2 образует фенилсульфенил-галогениды C6H5SHal.
При натр. в жидкой или газовой фазе Т. генерирует радикал C6H5S•,
к-рый замещает атомы галогена у sp2-гибридизованного атома углерода,
а также присоединяется к ацетилену с образованием бензотиофена.
Получают Т. обычно взаимод.
S с фенилмагнийбромидом или восстановлением бензолсульфохлорида:
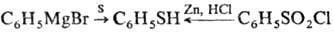
Используют также др. методы,
применяемые в синтезе тиофенолов.
Применяют Т. в синтезе
красителей, полимеров, ингибиторов радикальных р-ций, стабилизаторов и др. добавок
к синтетич. каучукам.
Для Т. ПДК 2-5 мг/м3,
ЛД5о для крыс 46,2 мг/кг (перорально),
9,8 МГ/КГ (внутрибрюшно). Э. Н. Дерягина.
Лит. см. при ст.
Тиолы.


