СУЛЬФАНЫ (полисероводороды),
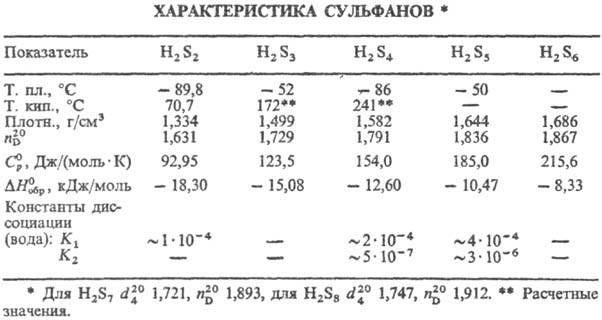
соед. общей ф-лы H2Sn, где n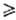 2.
В индивидуальном состоянии выделены С. с n до 8 (см. табл.). С.-желтые
маслянистые тяжелые жидкости с резким запахом, сильно преломляющие свет. Устойчивы
при 0°С в отсутствие воздуха, наиб. устойчив H2S2.
При длит. хранении
при комнатной т-ре отщепляют H2S с образованием С. с большим значением
п. При нагр. в вакууме выше ~ 100°С разлагаются. Сравнительно устойчивы
в кислой среде, их разложение ускоряется под действием окислителей, воздуха,
воды, спиртов. С. раств. в любом соотношении в бензоле, диэтиловом эфире, CS2,
СНСl3; дисульфан H2S2 растворяет S.
2.
В индивидуальном состоянии выделены С. с n до 8 (см. табл.). С.-желтые
маслянистые тяжелые жидкости с резким запахом, сильно преломляющие свет. Устойчивы
при 0°С в отсутствие воздуха, наиб. устойчив H2S2.
При длит. хранении
при комнатной т-ре отщепляют H2S с образованием С. с большим значением
п. При нагр. в вакууме выше ~ 100°С разлагаются. Сравнительно устойчивы
в кислой среде, их разложение ускоряется под действием окислителей, воздуха,
воды, спиртов. С. раств. в любом соотношении в бензоле, диэтиловом эфире, CS2,
СНСl3; дисульфан H2S2 растворяет S.
Получают С. действием соляной
к-ты на соответствующий полисульфид Na, в случае полисульфида неопределенного
состава образуется смесь С., к-рую разделяют перегонкой в вакууме. Применение
находят производные С.-полисульфиды (см. Сульфиды неорганические),
дихлор-сульфаны (см. Серы галогениды), орг. производные (см.
Полисульфиды органические). С. токсичны.
Лит.: Лаптев Ю.В.,
Сяркис А. Л., Колонии Г. Р., Сера и сульфидо-образование в гидрометаллургическях
процессах, Новосиб., 1987. И.Н. Один.


