СЕРИН (2-амино-3-гидроксипропионовая
к-та, b-гидро-ксиаланин, Ser, S) HOCH2CH(NH2)СООН,
мол. м. 105,09; бесцв. кристаллы. Для L-изомера т.пл. 228 °С (с разл.),
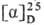 + 14,45°
(конц. 0,5 г в 100 мл 5,6 н. НС1). Для D- и D, L-C. т.пл. соотв. 228°С и
246°С (с разл.); т.возг. для D, L- и L-C. 150°С/10-4 мм рт.
ст.; раств. в воде, не раств. в этаноле и диэтиловом эфире. При 25 °С рКa
2,21 (СООН), 9,15 (NH2); pI 5,68. L-C. имеет сладковатый вкус.
+ 14,45°
(конц. 0,5 г в 100 мл 5,6 н. НС1). Для D- и D, L-C. т.пл. соотв. 228°С и
246°С (с разл.); т.возг. для D, L- и L-C. 150°С/10-4 мм рт.
ст.; раств. в воде, не раств. в этаноле и диэтиловом эфире. При 25 °С рКa
2,21 (СООН), 9,15 (NH2); pI 5,68. L-C. имеет сладковатый вкус.
С. обладает св-вами аминокислот
и спиртов. О-Ацилиро-вание С. осуществляют в нейтральной или кислой среде, N-ацилирование-в
сильно щелочной. О-Ацилсерин может претерпевать О,N-ацильную перегруппировку.
При энергичном восстановлении (напр., при действии HI и Р) С. переходит в аланин.
При нагр. со щелочами С. распадается с образованием пировиноградной к-ты; при
периодатном окислении образует формальдегид, NH3 и глиоксиловую к-ту;
с формальдегидом образует 1,3-оксазолидин-4-карбо-новую к-ту. В синтезе пептидов
гидроксигруппу С. защищают бензильной или трет-бутильной группами.
Остаток L-C. встречается
во всех организмах в составе молекул белков, особенно много их в фиброине шелка;
остаток С. входит также в молекулу фосфатидилсерина. Активность ряда
ферментов (трипсин, химотрипсин, холин-эстераза) связана со специфич. реакц.
способностью гид-роксигруппы остатка С., входящего в структуру их активных центров.
С.-кодируемая заменимая
аминокислота, образуется в организме в результате трансаминирования и послед.
дефосфорилирования 3-фосфопировиноградной к-ты, участвует в биосинтезе триптофана
и серосодержащих аминокислот, обратимо расщепляется на глицин и формальдегид,
претерпевает дезаминирование, превращаясь в пировиноградную к-ту. Из С. в организме
синтезируются этанол-амин и холин.
Синтез С. осуществляют
гидроксигалогенированием и послед. аминированием акриловой к-ты или гидроксимети-лированием
ацетамидомалонового эфира и послед. гидролизом продукта р-ции, напр.:
НСНО + СН3С(O)NHCH(СООС2Н5)2
: : СН3С(О)NHC(СН2ОН)(СООС2Н5)2
: С.
В спектре ПМР С. в D2
О хим. сдвиги протонов (в м. д.) у a-атома С составляют 3,846, у b-атома-3,989
и 3,95. Характерная цветная р-ция на С.-действие йодной к-ты и реактива Несслера.
С. впервые выделен Э. Крамером в 1865 из шелка. Мировое произ-во L-C. ок. 130 т/год (1989). В.В.Баев.


