САПОНИНЫ (от лат.
sapo-мыло), группа растит. глико-зидов, водные р-ры к-рых образуют стойкую мыльную
пену; обладают гемолитич. активностью и являются ядами для животных, дышащих
жабрами. К С. также относят гли-козиды стероидов и тритерпеноидов морских организмов.
С.-бесцв. или желтоватые
кристаллита, или аморфные в-ва с высокой т-рой плавления (плавятся с разл.);
хорошо раств. в воде, плохо-в холодном этаноле, лучше-в горячем и в метаноле,
не раств. в бензоле, хлороформе и диэтиловом эфире.
При кислотном или ферментативном
гидролизе С. расщепляются на углеводную составляющую и агликон (сапо-генин).
В зависимости от природы сапогенина С. подразделяют на стероидные и тритерпеновые.
Стероидные С. в качестве
сапогенинов содержат обычно производные спиростана (ф-ла I) или фуростана (II).
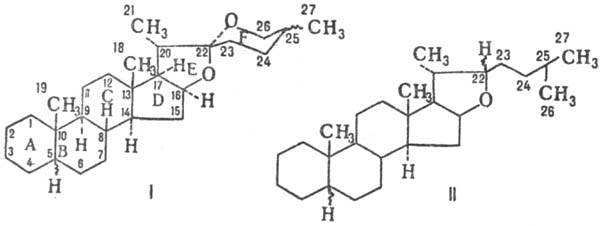
Спиростановые сапогенины,
за редким исключением, содержат 27 атомов углерода. Благодаря присутствию хи-рального
центра С-25 производные спиростана образуют изомеры (25R) и (25S),
или изо- и нео-изомеры (соотв. группа СН3 ориентирована
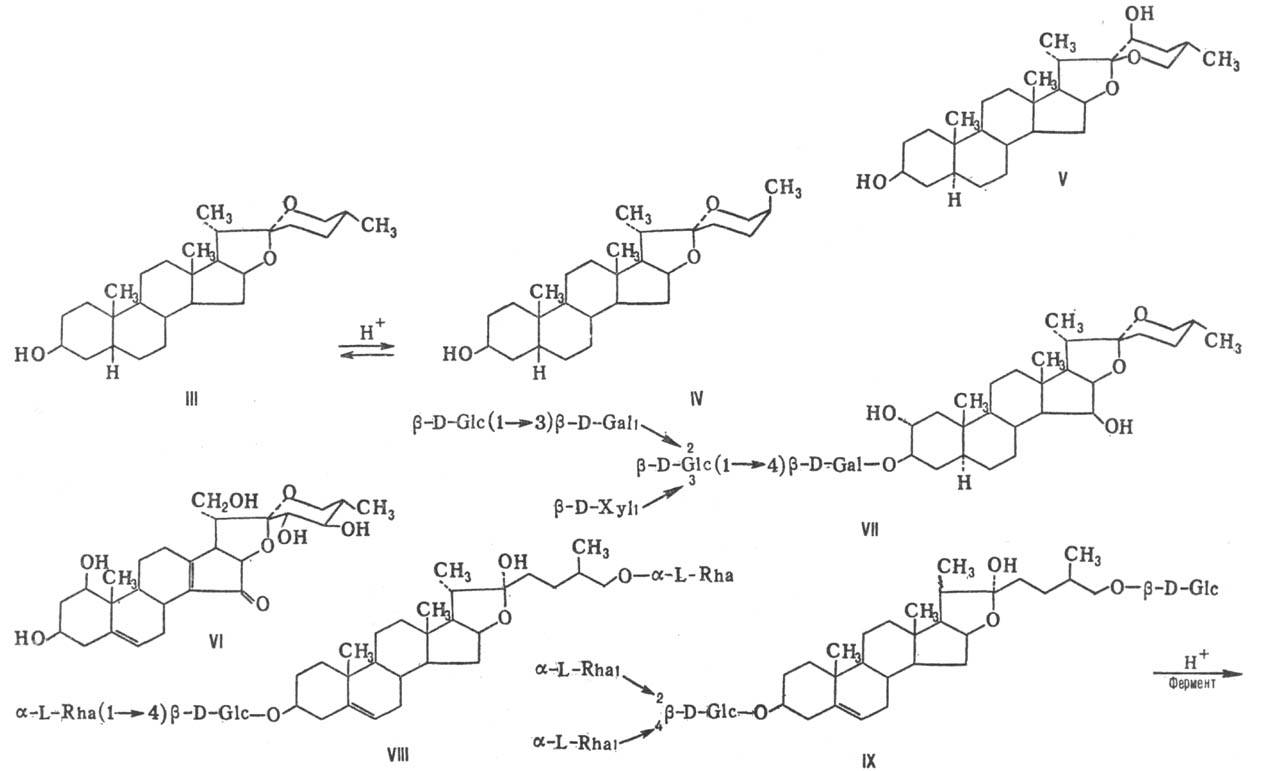
экваториально и аксиально). Смилаге-нин (III) и сарсасапогенин (IV)-типичные
представители агликонов этого типа; их структуры находятся в подвижном равновесии:
В растениях возможно совместное
присутствие (25R)-и (25S)-спиростанов, количеств. соотношение
к-рых может меняться во время хранения. Большое разнообразие изомерных
пар сапогенинов обусловлено кол-вом, конфигурацией и взаимным расположением
заместителей (обычно атом О, группа ОН), степенью ненасыщенности стероидного
ядра и стереохимией колец А и В.
Известно лишь неск. прир.
спиростанов, скелет к-рых имеет структурные и стереохим. отличия от скелета
соед. I.
Напр., для хиспигенина
(V) характерна обращенная конфигурация хирального центра С-22; трилленогенин
(VI) является производным 18-норспиростана. Агликоны С. ряда спиростана обычно
получают гидролизом спиростановых С. или выделяют из растений в своб. виде.
У большинства спиростановых
С. углеводный остаток связан с сапогенином через гидроксил при С-3. Вместе с
тем встречаются гликозиды с углеводным компонентом при атомах С-1, С-2, С-5,
С-6, С-11 или С-24. Кол-во моносаха-ридных остатков в молекулах С.-от одного
до шести. Обычно в состав углеводных цепей входят остатки D-глю-козы, D-галактозы,
D-ксилозы, L-рамнозы и L-арабинозы. Известны С., содержащие остатки D-хиновозы,
D-апиозы и D-фукозы. Молекула может содержать также алкоксикар-бонильные группы.
Ацильная группа (остатки уксусной, бензойной, 2-гидрокси-2-метилглутаровой,
серной к-т) может находиться как в сапогенной, так и в углеводной частях молекулы.
Нек-рые спиростановые С.
[напр., дигитонин (VII); Glc-глюкоза, Gal-галактоза, Xyl-ксилоза] способны образовывать
труднораств. комплексы с холестерином или др. 3b-гидроксистероидами.
С. ряда фуростана имеют
в своей основе скелет соед. II. Как правило, они содержат углеводную цепь при
С-3 и остаток D-глюкозы при С-26. Исключение составляет афромон-тозид (VIII;
Rha-рамноза). Отщепление остатка сахара от С-26 под действием к-т или ферментов
приводит к спироста-новым С., напр. в случае перехода от протодиосцина (IX)
к диосцину (X).
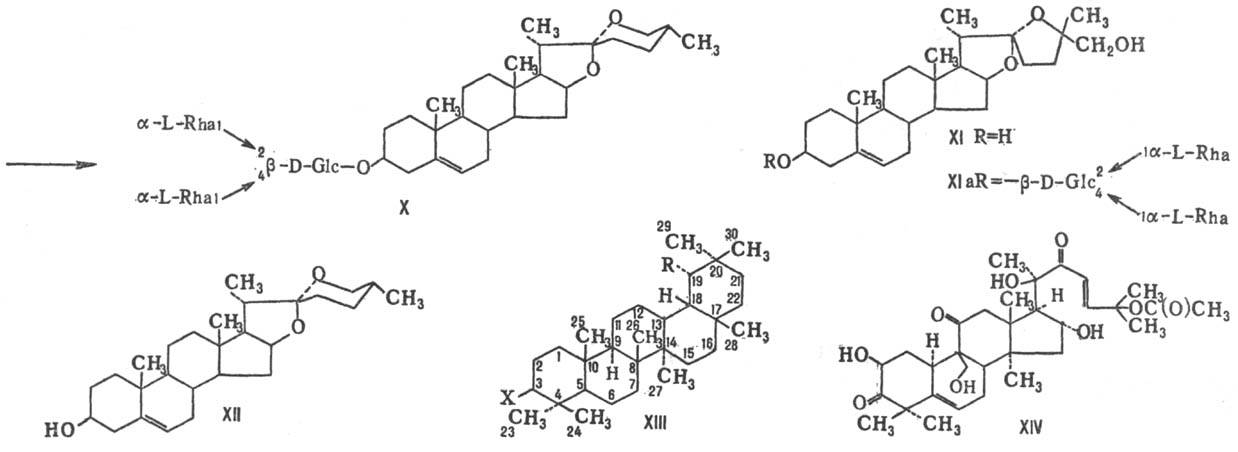
Др. тип фуростановых сапогенинов
представлен нуати-генином (XI) и его гликозидами, напр. акулеатизидом А (XIa).
Сапогенины спиростанового
типа, особенно диосгенин (XII),-осн. полупродукт в производстве стероидных препаратов
(см. Kopmuкоиды). Для спиростановых С. характерно гемолитич.,
канцеролитич., фунгистатич. и гипохолестери-немич. действие. У фуростановых
С. гемолитич. активность выражена гораздо слабее. Установлено, что фуростановые
С., в отличие от спиростановых, не осаждают холестерин из спиртовых р-ров.
Абс. большинство стероидных
С. продуцируется высшими растениями. Наиб. богаты ими семейства амараллисовых
(Amaryllidaceae), диоскорейных (Dioscoreaceae), лилиевых (Liliaceae). Известно
ок. 200 сапогенинов ряда спиростана и примерно такое же кол-во их гликозидов.
Доказано строение более 80 гликозидов фуростанового типа.
Биосинтез спиростанов в
растениях осуществляется из холестерина и, вероятнее всего, проходит через промежут.
стадию образования фуростанов.
Тритерпеновые сапогенины
являются обычно производными олеанана (XIII; X и R = Н) или урсана (ф-ла XIII;
X = Н, R = СН3; СН3-29 отсутствует). В природе широко
распространены С., сапогенинами к-рых являются амирины (напр., b-амирин,
ф-ла XIII, X = ОН, R = Н; в положении 12-13 двойная связь).
В бахчевых культурах содержатся
С. тритерпенового ряда (их идентифицировано св. 50), обладающие горьким неприятным
вкусом. Сапогенины этих С.-кукурбитацины (см., напр., ф-лу XIV-кукурбитацин
А).
С.-пенообразователи в огнстушащих
составах, а также для пива и др. напитков; компоненты мн. лек. настоек и препаратов
(сердечных, мочегонных, отхаркивающих и ДР·)·
Лит.: Физер Л.,
Физер М., Стероиды, пер. с англ., М., 1964; Деканосид-зе Г. Е., Чирва В. Я.,
Сергиенко Т. В., Биологическая роль, распространение и химическое строение тритерпеновых
гликозидов, Тб., 1984; Химия спиро-станолов, М., 1986; Строение и биологическая
активность стероидных гликозидов ряда спиростана и фуростана, Киш., 1987; Пасешниченко
В. А., Биосинтез и биологическая активность растительных терпеноидов и стероидов,
М., 1987; Tschesche R., Wulff G., в кн/ Fortschr. Chem. Org. Naturstoff, Bd
30, Bonn, 1973.
М. Б. Горовиц.


