ПУРИН (9H-имидазо
[4,5-d] пиримидин), ф-ла I, мол. м. 120,11; бесцв. кристаллы;
т. пл. 216-217°С; легко возгоняется в вакууме; хорошо раств. в воде, горячем
этаноле, бензоле, толуоле, плохо-в ацетоне, диэтиловом эфире, этилацетате, хлороформе.
Устойчив к нагреванию в водных р-рах к-т и щелочей, а также действию окислителей
(горячая HNO3 и др.). П. амфотерен (рКа 2,39 и
9,93). Образует соли с НС1, HBr, HNO3 (т. пл. 205 °С), пикриновой
к-той (т. пл. 208 °С), нек-рыми металлами (по атому водорода имидазольного
кольца). С бромом образует неустойчивый комплекс. Для П. характерна прототропная
таутомерия:
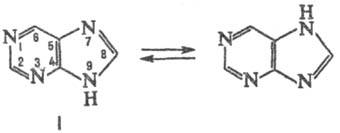
П.-я-дефицитная гетероароматич.
система. Электроф. агенты присоединяются гл. обр. по атомам N. При нагр. с уксусным
ангидридом П. превращ. в смесь 7(9)-ацетил-производных. Действие диметилсульфата
в водной щелочи или диазометана в спиртово-эфирном р-ре на П., а также обработка
его серебряной или таллиевой соли эквимоляр-ным кол-вом СН3I в ДМФА
(20°С) приводит к 9-метил-пурину. С избытком СН3I в ДМФА с выходом
65% получается 7,9-диметилпуринийиодид; 6-метилпурин в аналогичных условиях
превращ. в 6,9-диметшшурин. Взаимод. PhCH2Br с таллиевой солью П.
приводит к 9-бензилпурину. Электроф. замещение по атомам С характерно только
для производных П. с активирующими заместителями и идет всегда по положению
8, напр. при хлорировании газообразным хлором, прямом бромировании, нитровании.
Производные П. легко вступают
в р-ции нуклеоф. замещения, напр.:
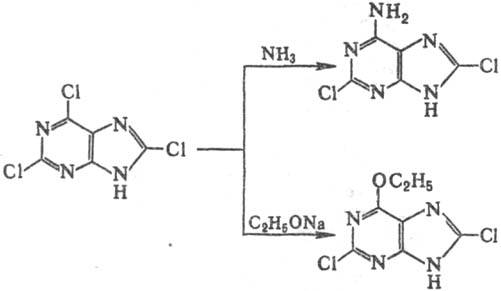
Щелочной гидролиз 2,6,8-трихлорпурина
с послед. восстановлением приводит к гипоксантину (бесцв. кристаллы, разлагающиеся
при 150 °С; pKa1 1,98, рКа2
8,94, рКа3 12,1):
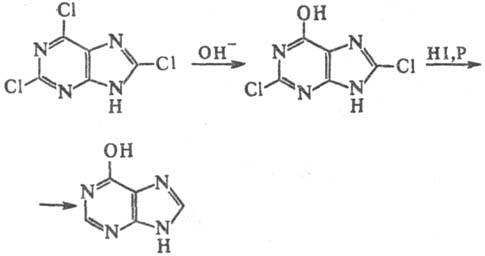
При сплавлении с серой
при 245 °С П. превращ. в 8-мер-каптопурин; под действием света присоединяет
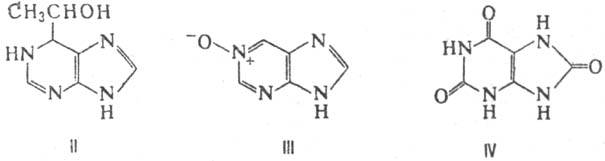
этанол с образованием 1,6-дигидро-6-(1-гидроксиэтил) пурина (ф-ла II). Окисление
действием Н2О2 в уксусном ангидриде приводит к смеси пурин-1-оксида
(III) и пурин-3-оксида. В присут. ксантиноксидазы происходит ферментативное
окисление П. в мочевую к-ту (IV).
П. встречается в природе
в форме 9-b-D-рибофуранозиль-ного производного-небуларина, к-рый выделен
из грибков Agaricus nebularis и плесени Streptomyces yokosukonensis. Из небуларина
П. может быть получен при гидролизе 3%-ным р-ром НС1.
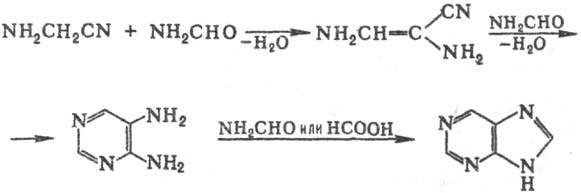
Синтезируют П. циклизацией
4,5-диаминопиримидина, к-рый, в свою очередь, м. б. получен взаимод. амино-ацетонитрила
с формамидом (250 °С):
Др. методы синтеза П.-дегалогенирование
6-хлор-, 2,6-дихлор- или 2,6,8-трихлорпурина под действием Zn-пыли в водном
р-ре или над Pt-катализатором, а также десульфи-рование 6-меркапто- или 2,6-димеркаптопурина
над Ni-Pe-нея в водном р-ре.
Производные, содержащие
систему П., широко распространены в природе и играют большую роль во мн. биол.
процессах. Важнейшие производные П.-аденин, гуанин (см. Пуриновые основания),
гипоксантин, кофеин (см. также Пури-новые алкалоиды), мочевая
кислота. Ядро П. входит в состав нек-рых антибиотиков и нуклеотидов, являющихся
структурными фрагментами нуклеиновых к-т. П. и ряд его производных обладают
противоопухолевой, противовирусной и противоаллергич. активностью.
Лит.: Гетероциклические
соединения, под ред. Р. Эльдерфилда, пер. с англ., т. 8, М., 1969, с. 130-300;
Heterocyclic compounds, ed. by A. Weissberger, v. 24, N.Y., 1971, p. 117-34.
И.М. Овчарова.


