ПРЕВОРЕАКЦИЯ, получение
транс-гликолей взаимод. олефинов со смесью иода и Ag-соли карбоновой
к-ты с послед. гидролизом диэфира гликоля водным р-ром щелочи:
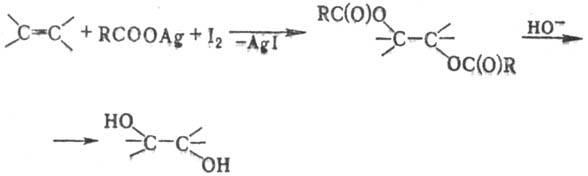
Первую стадию р-ции (получение
диэфира) проводят в орг. р-рителю (обычно СС14 или бензол) при длит.
кипячении (до 15 ч). При этом вначале образуется комплекс Симонини, или реактив
Прево [RCOOAg·RC(O)OI], к-рый реагирует с олефином. Вторая стадия - выделение
диэфира (для этого
отфильтровывают осадок AgI, р-ритель отгоняют) и его гидролиз. Выходы гликолей
30-90%. Наиб. высокие выходы получаются при использовании простейших олефинов
и бензоата Ag. При применении в р-ции солей карбоно-вых к-т алифатич. ряда и
солей дикарбоновых к-т выходы транс-гликолей обычно снижаются; в этом
случае нередко образуются в больших кол-вах трудноотделимые и реак-ционноспособные
примеси. Применение вместо I2 др. галогенов (С12 или Вr2)
значительно усложняет выбор условий проведения р-ции (р-ритель, т-ра) и способы
очистки транс-гликоля от примесей.
В условиях П. р. из 1,3-диенов
образуются преим. тетролы (при избытке соли карбоновой к-ты и иода) или смеси
1,2-и 1,4-диолов.
Осн. побочные продукты
П.р.-алкил- или арилиодиды, ангидриды и иодангидриды карбоновых к-т, олигомеры
и полимеры. Если исходные продукты или р-ритель содержат влагу, то в качестве
примеси образуются также цис-диолы.
Считается, что П. р. протекает
по ионному механизму по схеме:
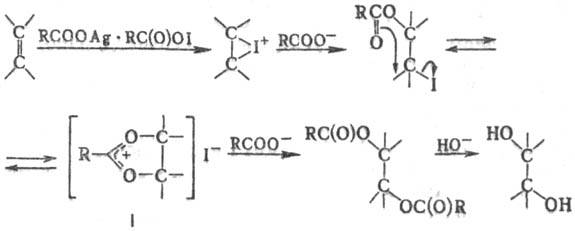
Модификация П. р.-получение
цис-диолов взаимод. олефинов с комплексом Симонини в присут. Н2О
(в этом случае гидролизу подвергаются соед. I, а не диэфир).
П. р. используют в препаративных
целях в тонком орг синтезе. Она открыта в 1933 К. Прево.
Лит.. Вильсон Ч.,
в сб.: Органические реакции, пер. с англ., сб. 9, М., 1950, с. 463 66; Общая
органическая химия, пер. с англ., т. 2, М., 1982, с. 124 25; Маки Р , Смит Д.,
Путеводитель по органическому синтезу, пер. с англ., М., 1985, с. 229-31 Г
И Дрозд


