ПОЛИЯДЕРНЫЕ СОЕДИНЕНИЯ
(многоядерные соед.), координац. соед., в молекулах к-рьгх имеется неск.
атомов металлов, окруженных лигандами и связанных друг с другом посредством
мостиковых групп. Наиб. изучены би-и триядерные координац. соединения. Когда
число атомов металлов велико, такие соед. наз. координационными или металлсодержащими
полимерами, металлополимерами (см. Координационные полимеры). Соотношение
между П. с. и координац. полимерами такое же, как и между мономерами (и олигомерами)
и полимерами в карбоцепных высокомол. соединениях. К П. с. иногда относят соед.,
содержащие ячейки из непосредственно связанных друг с другом атомов металлов,
обычно наз. кластерами. Различают гомо- и ге-терометаллические П. с.
Расстояния металл-металл в П. с. варьируют в широких пределах, иногда могут
достигать 1 нм и более.
Число известных П. с. огромно.
Прир. и пром. р-ры ионов металлов, как правило, содержат П. с. Многие координац.
соед. в паровой фазе также имеют строение П. с., напр. Fе2С16
(ф-ла I).
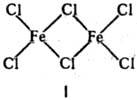
Биядерные координац. соед.
по структуре удобно классифицировать по числу мостиковых групп, связывающих
моноядерные фрагменты. При одной мостиковой группе связь М— . —М м. б. линейной
(плоской), напр. LM—F—ML, соед. II, III, или изогнутой-соед. IV (X = С1, Вг,
Д V.
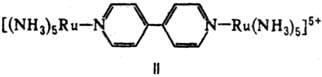
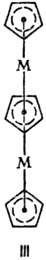
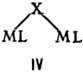
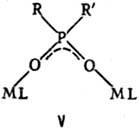
При двух мостиковых группах
часто реализуется устойчивый плоский квадрат-соед. VI.
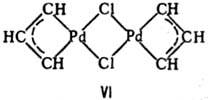
Макс. число мостиковых
групп между двумя атомами металлов 4.
Триядерные координац. соед.
могут иметь линейное или циклич., напр соед. VII, строение.
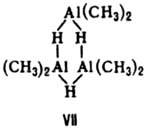
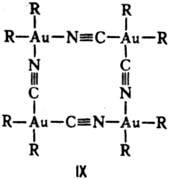
В тетраядерных координац.
соед. атомы металлов могут выстраиваться в цепь, напр. соед. VIII, образовать
цикл (соед. IX) или тетраэдр (соед. X).
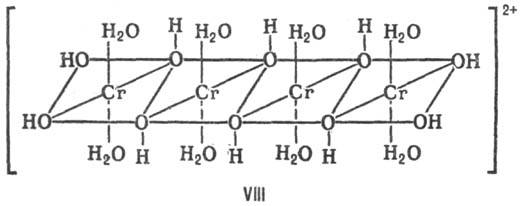
 J
J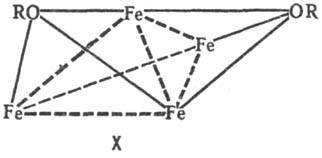
С увеличением числа
атомов металлов в П. с. число возможных типов структур и их сочетаний увеличивается.
Олигомеры с числом атомов металлов п = 5-15 часто имеют глобулярное строение,
типичный пример-анионы гетерополикислот.
В р-рах П. с. образуются
при наличии полидентатных лигандов и избытка ионов металлов. Поскольку образующиеся
из молекулы воды лиганды полидентатны (ОН-бидентатный и О-тридентатный), то
в водных р-рах солей металлов всегда имеет место в той или иной степени полиядерное
комплексообразование, усиливающееся также благодаря образованию мостиковых водородных
связей. Для идентификации и изучения П. с. в р-рах используют спектрофотометрию,
разл. варианты радиоспектроскопии, в т.ч. ядерную магн. релаксацию.
Гидролиз - один из осн.
путей образования П. с. Характерный пример-укрупнение комплексов Bi:
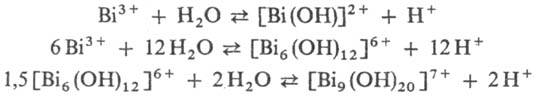
Практически все многозарядные
катионы образуют в водных р-рах П. с. в соответствующей области рН. Так, в р-рах
Sn(II) всегда присутствует катион [Sn2(OH)2]2+,
а также [Sn3(OH)4]2+, в к-ром атомы Sn образуют
треугольник Sn3 с расстоянием Sn—Sn ~ 0,36 нм. Аналогично существование
П. с. в р-рах Pt(II) доказано выделением соли [Pt4(OH)4](ClO4)4·2H2O,
катион Pt4(OH)4 имеет форму куба. Однако многие би-, три-
и тетраядерные комплексы получены только в определенных эмпирически найденных
условиях, при определенных соотношениях реагентов, р-ри-телей и т.п.
Чаще всего П. с. получают
путем связывания части лигандов в моноядерных комплексных соед., напр.:
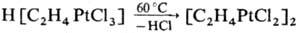
Др. путь-р-ции функц. групп
в лиганде, напр.:
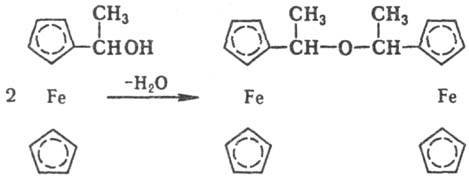
Реакц. способность П. с.
в большинстве простейших р-ций, характерных для координац. соед., таких, как
окислит.-вос-становит. р-ции, замещение лигандов, обмен лигандами во внеш.
сфере и т.п., мало чем отличается от реакц. способности моноядерных комплексов
с теми же лигандами.
Типичная для П. с. р-ция-расщепление
мостиковых связей с образованием, как правило, моноядерных координац. соединений:
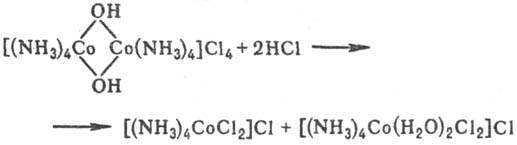
Одно из наиб. характерных
св-в П.с.-внутримол. электронный обмен, исследуемый такими методами, как ЯМР,
метод остановленной струи, электрохимические и т.д. Найдено, что по мере уменьшения
расстояния между ионами и увеличения электронной проводимости лигандов скорость
обмена возрастает на неск. порядков.
Особый интерес представляют
магн. св-ва П. с. Ряд магнитных П. с. образует диэлектрич. кристаллы, содержащие
в качестве структурных элементов решетки ионы переходных металлов, участвующие
в обменных взаимодействиях друг с другом; они эффективно экранированы лигандами
от др. парамагн. центров. Такие системы иногда наз. "обменными кластерами".
Они оказались удобными модельными системами для исследования обменных взаимодействий
и создания микроскопич. теории магнетизма.
Отдельные типы П. с. находят
практич. применение в качестве эффективных катализаторов, разл. материалов (магн.,
диэлектрич., полупроводниковых).
Лит.: Хайдук И.,
"Успехи химии", 1961, т. 30, в. 9, с. 1124-74; Харгит-таиМ., ХаргиттаиИ.,
Геометрия молекул координационных соединений в парообразной фазе, пер. с англ.,
М., 1976; Цукерблат Б. С., Белинский М. И., Магнетохимия и радиоспектроскопия
обменных кластеров, Киш., 1983; Burgess J., Metal ions in solution, Chichester-N.
Y., 1978. С.П. Губин.


