ПОЛИФЕНИЛЕНЫ. Однозначного
определения в литературе нет. К П. можно отнести полимеры, содержащие в основной
цепи соединенные непосредственно друг с другом фениленовые группы (в т.ч. замещенные),
последовательность к-рых может прерываться мостиковыми атомами или группами
атомов. Известны П. линейной и трехмерной структур, образование к-рых определяется
методами их синтеза.
Получение. 1) Окислит.
дегидрополиконденсация мономеров в присут. системы к-та Льюиса-окислитель.
В качестве мономеров используют
бензол, из к-рого с количеств. выходом образуется неплавкий и нерастворимый
n-П. (кат.-А1С13-СuС12; 80 °С), бифенил, о-
и м-тер-фенилы и др. ароматич. соед., а также разл. смеси этих соед.
(напр., бензола и 1,3,5-трифенилбензола). Из смесей получены р-римые сополимеры,
из к-рых можно формовать изделия. Для получения практически ценных изделий из
р-римых П. их превращ. в сшитые П., для чего, напр., предварительно смешивают
с n-ксилиленгликолем, а затем формуют изделие, к-рое и подвергают отверждению
в присут. n-толуол-сульфокислоты. Из
алкилбензолов, хлор- или фторбензола, дифенил-оксида или дифениламина получены
низкомолекулярные П.
2) Полиарилирование ароматич.
соед. при термич. разложении ароматич. дисульфохлоридов.
Для синтеза используют
обычно м-бензолдисульфохло-рид и смесь изомерных терфенилов; р-ция протекает
по схеме:
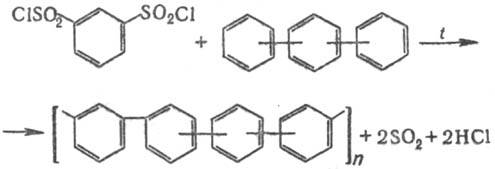
Процесс проводят в две
стадии: при 255-275 °С получают р-римый и плавкий П., затем из смеси его
с м-бензол-дисульфохлоридом формуют изделия, к-рые отверждают при 300-325
°С. В результате образуется неплавкий и нерастворимый П.
3) Взаимодействие по р-ции
Дильса-Альдера диэтиниль-ных ароматич. соед. и бис-тетраарилциклопентадиенонов
(тетрациклонов) или бис-2-пиронов с послед. ароматизацией.
Из тетрациклонов получают
при 180-250 °С фенилирован-ные П. (мол. м. 20000-100000) по схеме:
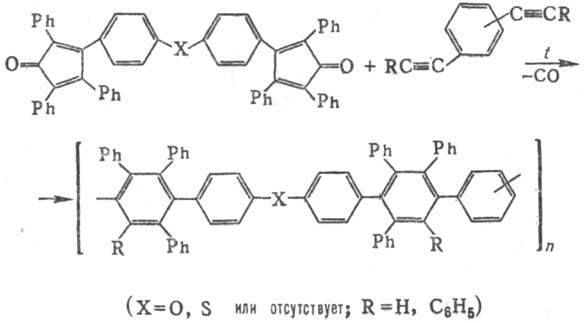
При взаимод. n-фенилен-бис-2-пирона
с n-диэтинилбен-золом получен неплавкий и нерастворимый кристаллический
n-П.
4) Полициклотримеризация
(см. Полициклизация)ди-и моноэтинильных соед. по схеме:
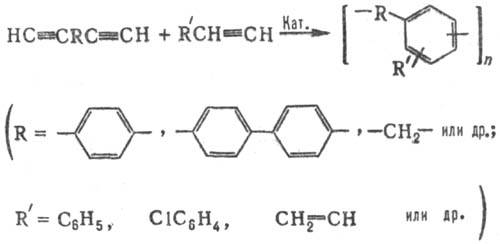
На первой стадии в р-ре
в присут. катализатора, напр. Циглера-Натты (С2Н5)2
А1С1-ТiС14, получают плавкие и р-римые форполимеры, содержащие концевые
этинильные группы, на второй при 200-300 °С (обычно при переработке их в
изделия) образуются сетчатые П.
5) Полициклоконденсация
кеталей ди- и моноацетилари-ленов в присут. кислых катализаторов по схеме:
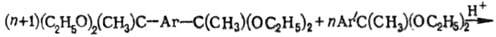
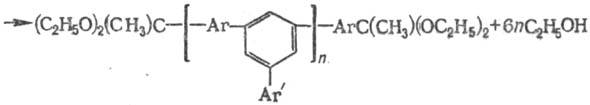
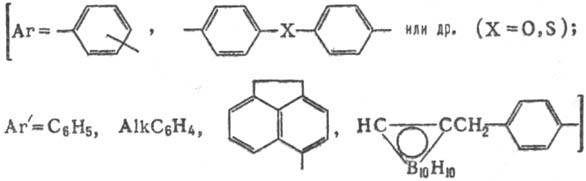
Процесс проводят в две
стадии, как и в предыдущем методе. Из смеси ди- и моноацстилароматич. соед.
в присут. триэтилортоформиата НС(ОС2Н5)3 вначале
получают форполимер, к-рый м. б. модифицирован одним из способов: 1) концевые
ацетильные группы превращают в группы, способные к полимеризации или циклотримеризации;
2) вводят в цепь П. способные к полимеризации фрагменты, напр. аценафтиленовые
группы. На второй стадии получают П. трехмерной структуры, осуществляя полимеризацию
и (или) циклотримеризацию модифицир. форполимера или взаимод. немодифицир. форполимера
с отвердителем, напр. с кремнийорг. соед., содержащим концевые группы SiH.
П. получают также каталитич.
поликонденсацией гало-генопроизводных ароматич. соед. по р-циям Вюрца-Фит-тига,
Ульмана, Гриньяра и т.д., разложением бис-диазо-ниевых солей в присут.
CuCl по р-ции Гомберга-Бахмана-Хея и мн. др. методами.
Совр. тенденции развития
методов синтеза П. заключаются в разработке способов получения плавких и р-римых
форполимеров, содержащих, как правило, реакционноспо-собные функц. группы, к-рые
при переработке превращаются в сетчатые полимеры.
Свойства и применение.
П.-твердые аморфные или кристаллич. в-ва. Их св-ва зависят от мол. массы
и строения макромолекулы, напр. от наличия заместителей в бензольных кольцах,
изомерии фениленовых групп, наличия не-фениленовых звеньев и разветвленности.
n-П.-неплавкий и
нерастворимый в орг. р-рителях кристаллич. полимер. Фенилированные П., полученные
по методу 3,-аморфные полимеры; хорошо раств. в толуоле, хлороформе и др. орг.
р-рителях.
Для П. характерны высокие
тепло- и термостойкость (300-600 °С), высокие коксовые числа и, как правило,
очень высокая хим. стойкость (даже к к-там и щелочам), высокая радиац. и абляц.
стойкость, обычно хорошие диэлектрич. и др. ценные св-ва.
Полностью ароматические
П. можно гидрировать, сульфировать, нитровать и т.д., т.е. они вступают в р-ции,
характерные для низкомол. ароматич. соединении. Сульфированные П. раств. в смесях
ацетон-вода и при сплавлении со щелочами превращ. в гидроксизамещенные П. Нитрозамещенные
П. восстанавливаются в аминозамещенные.
В широком пром. масштабе
П. пока не производятся; в небольших кол-вах выпускается п-П. в
США (под торговым назв. эймак-221).
Лит.: Энциклопедия
полимеров, т. З, М., 1977, с. 74-77; Тепляков М. М. [и др.], "Высокомол.
соед.", А., 1990, т. 32, с. 1683-90; Kovacic P., Jones M. В., "Chem.
Rev.", 1987, v. 87, p. 357-79; Teplyakov М. М. [a.e.], "Makromol.
Chem.", 1990, v. 191, p. 801-07; Rehahn M., Schliiter A.-D., Wegner G.,
"Macromol. Chem.", 1990, v. 191, p. 1991-98. M. M. Тепляков.


