ПИРРОЛИЗИДИН (1-азабицикло[3.3.0]октан),
мол.м. 111,18; бесцв. маслянистая жидкость с аминным запахом; т. кип. 1480C;
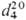 0,9149;
0,9149;
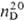 1,4700;
раств. в воде. Существует преим. в конформации с цис-сочленением колец.
1,4700;
раств. в воде. Существует преим. в конформации с цис-сочленением колец.
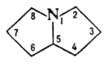
По хим. св-вам П.-третичный
амин; легко образует соли и четвертичные аммониевые основания, напр. тетрахлораурат
C7H13N·HAuCl4
с т.пл. 2350C, гексахлор-платинат 2C7H13N·H2PtCl6
с т. пл. 205-2060C, пикрат с т.пл. 258-2600C, иодметилат
с т.пл. 344-3450C. При окислении легко превращ. в N-оксид. При действии
щелочей на четвертичные соли П. происходит расщепление кольца; послед. гидрирование
продуктов р-ции приводит к 1-метил-2-пропилпирролидину:
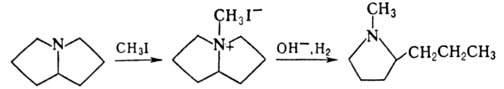
Получают П. действием конц.
H2SO4 на N-бrом-2-пrо-пилпирролидин,
циклизацией N,N- дибром-4-аминогептана, каталитич. дегидратированием 2-(3-аминопропил)фурана
с послед. гидрированием промежуточно образующегося 1,2-триметиленпиррола, конденсацией
оснований Манниха, полученных из пиррола, с малоновым эфиром с послед. восстановит.
циклизацией:
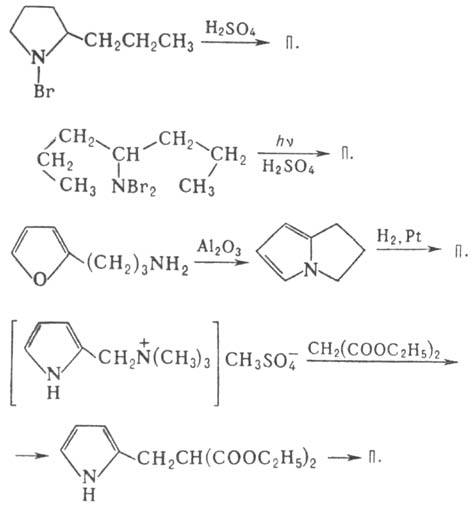
Циклич. система П.-основа
алкалоидов сложноцветных (Compositae), бурачниковых (Boraginaceae), люпиновых
(Lupinus L.) и нек-рых др. растений.
Лит.: Kochetkov
N. К., Likhosherstov A. M., в сб.: Advances in he-terocyclic chemistry, v.
5, N. Y.-L., 1965, p. 315-67. M. А. Юровская.


