ПИРИДАЗИН (1,2-диазин,
ойазин), мол. м. 80,09; бесцз. жидкость; т. пл. -80C, т. кип. 2080C,
48°С/1 мм рт. ст.; 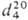 1,1054;
1,1054; 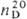 1,5218; рКа 2,33 (200C); g 0,047 Н/м (340C);
m 13,14·10-30 Кл·м;
1,5218; рКа 2,33 (200C); g 0,047 Н/м (340C);
m 13,14·10-30 Кл·м; 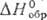 — 278,4 кДж/моль. Раств. в воде, спиртах, бензоле,
диэтиловом эфире, не раств. в петролейном эфире. Производные: гидрохлорид, т.
пл. 161-1630C; пикрат, т. пл. 170-1750C (с разл.); комплекс
с PtCl4 , т. пл. 1800C. Молекула П. плоская.
— 278,4 кДж/моль. Раств. в воде, спиртах, бензоле,
диэтиловом эфире, не раств. в петролейном эфире. Производные: гидрохлорид, т.
пл. 161-1630C; пикрат, т. пл. 170-1750C (с разл.); комплекс
с PtCl4 , т. пл. 1800C. Молекула П. плоская.
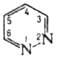
С большим трудом вступает
в р-ции с электроф. агентами. С алкилгалогенидами образует соли по одному атому
N, с оксониевыми солями-по обоим, с аминирующими агентами-соли моно-N-аминопиридазиния.
При взаимод. с над-кислотами окисляется до моно- и ди-N-оксидов П. С маг-нийорг.
соед. образует 4-замещенные, с литийорг. соед.-3-замещенные; р-ция идет через
продукты присоединения, к-рые далее м. б. окислены до производных П. Дейтероводо-родный
обмен под действием смеси CH3OD-CH3ONa происходит преим.
по положению 4. Гомолитич. бензилирова-ние П. приводит к получению 4-бензилпиридазина,
бензои-лирование-к смеси 4-бензоил- и 4,5-дибензоилпиридазинов. При фотолизе
П. в газовой фазе происходит раскрытие цикла с образованием азота и винилацетилена,
при восстановлении Na в спирте-с образованием тетраметиленди-амина. При комнатной
т-ре П. легко вступает в диеновый синтез с малеиновым ангидридом, давая аддукт
состава 2:1; при 3000C изомеризуется в пиримидин. Для 3- и 4-метил-пиридазинов
характерна конденсация с бензальдегидом по метильной группе.
П. получают взаимод. гидразина
с диацеталем малеино-вого альдегида или с a-кетоглутаровой к-той c послед.
превращениями, напр. по схеме:
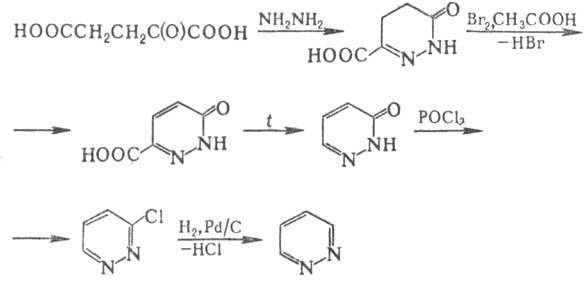
Др. способы получения П.
и его замещенных: восстановление 3-хлор и 3,6-дихлорпиридазинов, декарбоксилирование
пиридазинкарбоновых к-т, взаимод. 2,5-диацетокси- или 2,5-диметокси-2,5-дигидрофурана
с гидразином.
Методы синтеза основных
функцион. производных П.-га-логенопиридазинов, аминопиридазинов и пиридазинонов:
4-и 5-галогенопроизводные получают обычно циклизацией соед. с открытой цепью,
3- и 6-производные-путем галоге-нирования соотв. замещенных пиридазинов с помощью
POCl3,
PCl5 или PBr5; аминопиридазины - взаимод. гало-генопиридазинов
с NH3, аминами или мочевиной; пирида-зиноны-заменой галогена в галогенопроизводных
П. на алкоксигруппу с послед. гидролизом.
Замещенные П. проявляют
биол. активность (пестицид-ную, антивирусную, антибактериальную); нек-рые конден-сированные
П. входят в состав лек. ср-в (напр., апрессин, непрессол). 3,6( 1H,2H)-Диоксопиридазин
- селективный регулятор роста растений.
Лит.: Обшая органическая
химия, пер. с англ., т. 8, M., 1985, с. 119-43; Comprehensive heterocyclic chemistry,
N. Y., 1984, v. 2, pt 2А, p. 1-98; v. 3, pt 2В, p. 1 56; T i s 1 е г M., S t
а n о v n i k В., в сб.: Advances in heterocyclic chemistry, v. 24, N.
Y., 1979, p. 363 45. В. Ф. Седова.


