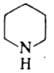
ПИПЕРИДИН (гексагидропиридин,
пентаметиленимин), мол. м. 85,15; бесцв. жидкость с резким аминным запахом;
т. пл. -9 0C. т. кип. 106,17 0C, 36,7 °С/70 мм рт.ст.;
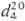 0,8606;
0,8606;
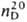 1,4530;
рКа 11,25 (250C). Смешивается во всех соотношениях
с водой и большинством орг. р-ри-телей; образует азеотропную смесь с водой (т.
кип. 92,80C, 35% воды по массе). Обладает св-вами вторичных
алифатич. аминов. Легко образует соли (гидрохлорид, т. пл. 244-2450C;
пикрат, т. пл. 151-1520C); с HNO2 дает N-нитрозопроизводное,
с ангидридами и галогенангидридами - N-ацилпроизводные [N-ацетилпиперидин, т.
пл. 1090C, т. кип. 226-2270C; N-бен-зоилпиперидин, т.
пл. 480C; N-(n-нитробензоил)пиперидин, г. пл. 1210C].
Легко алкилируется по атому азота; при конденсации с S образует сульфид C5H10NSNC5H10;
в присут. солей Ag, CuO, а также при нагр. с конц. H2SO4 дегидрируется
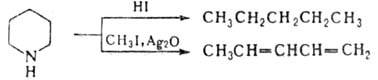
в пиридин. Р-ции с раскрытием цикла происходят под действием конц. HI в жестких
условиях или при расщеплении по Гофману:
1,4530;
рКа 11,25 (250C). Смешивается во всех соотношениях
с водой и большинством орг. р-ри-телей; образует азеотропную смесь с водой (т.
кип. 92,80C, 35% воды по массе). Обладает св-вами вторичных
алифатич. аминов. Легко образует соли (гидрохлорид, т. пл. 244-2450C;
пикрат, т. пл. 151-1520C); с HNO2 дает N-нитрозопроизводное,
с ангидридами и галогенангидридами - N-ацилпроизводные [N-ацетилпиперидин, т.
пл. 1090C, т. кип. 226-2270C; N-бен-зоилпиперидин, т.
пл. 480C; N-(n-нитробензоил)пиперидин, г. пл. 1210C].
Легко алкилируется по атому азота; при конденсации с S образует сульфид C5H10NSNC5H10;
в присут. солей Ag, CuO, а также при нагр. с конц. H2SO4 дегидрируется
в пиридин. Р-ции с раскрытием цикла происходят под действием конц. HI в жестких
условиях или при расщеплении по Гофману:
Осн. методы синтеза П.:
каталитич. гидрирование (Ni, 170-2000C) или электрохим. восстановление
пиридина (последний метод применяется в пром-сти); разл. способы замыкания цикла,
напр.:
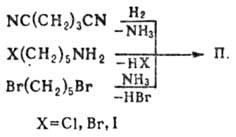
П.-структурный фрагмент
алкалоида черного перца пиперина и др. алкалоидов (лобелина, тропика, анабазина,
морфина), а также мн. лек. препаратов (анальгетиков, ане-стетиков и др.); нек-рые
производные П., в частности пента-метилендитиокарбамат,- ускорители вулканизации.
В лаб. практике П.-реагент
в синтезе енаминов, катализатор Манниха реакции, Михаэля реакции, Кнёвенагеля
реакции, Клайзена-Шмидта реакции.
Лит.. Гетероциклические
соединения, под ред. P. Эльдерфилда, пер. с англ., т. 1, M., 1953, с. 430; Физер
Л., Физер M., Реагенты для органического синтеза, пер. с англ., т. 3, M., 1970,
с. 102-107.


