ПЕРФТОРИЗОБУТИЛЕН (1,1,3,3,3-пентафтор-2-трифтор-метилпропен)
(CF3)2C=CF2, мол.м. 200,03; бесцв. газ с характерным
запахом; т. кип. 6,5 0C; 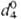 (для жидкости) 1,5922; раств. в диэтиловом эфире, ацетоне, ТГФ, не раств. в
воде.
(для жидкости) 1,5922; раств. в диэтиловом эфире, ацетоне, ТГФ, не раств. в
воде.
П. один из наиб. электроф.
фторолефинов. Легко реагирует с нуклеофилами: гидролизуется водой в орг. р-рителях
до a-гидрогексафторизомасляной кислоты, со спиртами дает эфиры (CF3)2CHCF2OR
и (CF3)2C=CFOR, с диметилами-ном енамин (CF3)2C=CFN(CH3)2
и аминаль (CF3)2C = =C[N(CH3)2].
Ацилпероксиды и H2O2 окисляют П до эпоксидов.
Р-ция П. с фторидами щелочных
металлов приводит к перфтор-трет-бутил-аниону, из к-рого получают разл.
соед., содержащие группу (CF3 )3С, напр.:
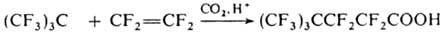
Получают П. пиролизом дифтордихлорметана,
тетрафторэтилена, перфторциклобутана, политетрафторэтилена (при 700 750 0C).
Применяют П. в лаб. практике для синтеза гексафторацетона и др. фторорг. соединений.
П чрезвычайно токсичен.
Летальная концентрация 0,5-10 4 % по объему (крысы, экспозиция 6
ч).
Лит Зейфман Ю В
[и др.]. "Успехи химии". 1984, т 53, в 3. с 431 64
Е. M Рохлин


