ОРГАНИЧЕСКИЙ СИНТЕЗ,
раздел орг. химии, в к-ром рассматриваются пути и методы искусств. создания
орг. соед. в лаб. и пром. масштабах. Широко применим в лаб. условиях (гл. обр.
для исследоват. целей) и в пром-сти (см. Основной органический синтез. Тонкий
органический синтез).
Успешное развитие О. с.
началось после разработки теории хим. строения (см. Органическая химия)и
накопления сведений о хим. св-вах орг. соед. (2-я пол. 19 в.). С этого времени
О. с. как осн. источник новых орг. соед. играет фундам. роль в становлении орг.
химии как науки и в ее дальнейшем развитии, обеспечивая постоянно расширяющийся
круг изучаемых объектов. Развитие О. с. в 20 в., особенно в последние десятилетия,
характеризуется все возрастающим вниманием к синтезу прир. соед. и их аналогов,
значит. укреплением методич. базы (созданием надежных синтетич. методов), началом
создания самостоят. теории О. с. Осуществление синтеза сложнейших прир. соед.
(напр., хлорофилла, витамина В12, биополимеров), создание материалов
с необычными св-вами (напр., т. наз. металлов органических)показывает,
что для современного О. с. практически не существует неразрешимых задач.
В статье рассмотрены вопросы,
касающиеся планирования О. с.,т. е. выбора оптим. пути получения соед. с заранее
заданной структурой. Конкретные методы синтеза-образование новой связи С—С,
введение функц. групп и др. изложены в статьях, посвященных р-циям (напр., алкилиро-вание,
Арбузова реакция, диеновый синтез, нитрование).
Обычно синтез целевого
соед. осуществляют из относительно простых и доступных (т. е. выпускаемых пром-стью)
исходных в-в. Как правило, при синтезе сложных в-в путь от исходных соед. к
целевому разбивается на ряд этапов (стадий), на каждом из к-рых происходит образование
одной-двух связей (фрагментов) будущей молекулы или подготовка к образованию
таких связей.
Осуществление О. с. сопряжено
с решением двух осн. вопросов: 1) разработка общего плана синтеза, т.е. выбор
оптим. исходных соед. и последовательности стадий, ведущих кратчайшим путем
к целевому продукту (стратегия синтеза); 2) выбор (или разработка новых) синтетич.
методов, обеспечивающих возможность построения необходимой связи в определенном
месте собираемой молекулы (тактика синтеза).
Основу тактики О. с. составляют
различные синтетич. методы, каждый из к-рых представляет собой стандартную совокупность
одной или неск. р-ций и приемов выделения продуктов, к-рые обеспечивают возможность
построения или разрыва определенного типа связи (или связей), необходимой для
синтеза целевого соединения. Важные характеристики эффективного синтетич. метода
- общность (слабая зависимость результата от конкретных особенностей структуры
исходных соед.), селективность (участие в осн. р-циях метода лишь определенных
функц. групп) и высокие выходы продуктов. Типичным примером эффективного синтетич.
метода может служить синтез олефинов по Виттигу (р-ции 1-3) из алкилгалогенидов
и карбонильных соед.:

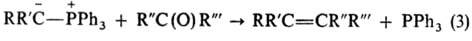
Осн. методы О. с. можно
разбить на три группы: 1) конструктивные, ведущие к образованию новых связей
С—С, назначение к-рых-построение скелета будущей молекулы (напр., р-ция Гриньяра,
р-ция Фриделя-Крафтса, цикло-присоединение); 2) деструктивные, ведущие к разрыву
определенных связей С—С с целью удаления той или иной группировки из молекулы
после того, как ее роль в синтезе сыграна (напр., декарбоксилирование, периодатное
окисление диолов); 3) методы трансформации функц. групп. Последнее важно для
введения в молекулы исходных или проме-жут. соед. функц. групп и их защиты (см.
Защитные группы), требующихся для осуществления очередной конструктивной
р-ции, а на заключит. стадиях синтеза-для введения необходимых функц. групп
в целевое соединение.
Методы трансформации функц.
групп (напр., превращ. спиртов в алкилгалогениды, простые и сложные эфиры, карбонильные
соед. и обратные им превращения) хорошо разработаны. Это позволяет говорить
о синтетич. эквивалентности функц. групп и целых фрагментов молекул, если они
легко взаимопревращаемы. Напр., при синтезе замещенных бензиловых спиртов (4
и 5) и алкиларилов (4 и 6) введение в молекулу арена ацильного остатки (4) в
синтетич. плане эквивалентно введению 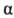 -гидроксиалкилъного
или алкильного остатка, поскольку карбонильная группа в про-межут. кетоне легко
м. б. восстановлена до спиртовой (5) или до СН2-звена (6):
-гидроксиалкилъного
или алкильного остатка, поскольку карбонильная группа в про-межут. кетоне легко
м. б. восстановлена до спиртовой (5) или до СН2-звена (6):

Принцип синтетич. эквивалентности
позволяет использовать практически весь арсенал существующих р-ций для сборки
целевой структуры почти независимо от конкретного распределения (или отсутствия)
в ней функц. групп; напр., наращивание углеродной цепи путем алкилирования моно-замещенных
ацетиленидов можно рассматривать как метод синтеза цис-олефинов, легко
получаемых из дизамещенных ацетиленов путем частичного гидрирования.
Рассмотрение вопросов синтетич.
эквивалентности привело к введению в О. с. понятия "синтон", под
к-рым подразумевают реальные или нереальные (виртуальные) частицы, присоединение
к-рых к субстрату соответствует введению в него определенной (обычно достаточно
крупной и распространенной в орг. соед.) группы. Синтон-понятие абстрактное,
описывающее в символич. виде результат к.-л. синтетич. операции. Ему должен
соответствовать тот или иной реагент (реагенты), участвующий в реальной р-ции.
Так, напр., записанной на синтонном языке р-ции (7), ведущей к карбоновым к-там,
соответствуют реальные р-ции (8 и 9), в к-рых синтетич. эквивалентом синтона
-СООН выступает CN- (записывается -СООН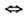 -CN), синтона R+-ал-килгалогенид или алкилсулъфонат (R+
-CN), синтона R+-ал-килгалогенид или алкилсулъфонат (R+
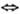 RX):
RX):
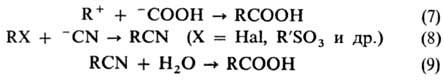
Представление о синтонах
широко используют для решения тактич. и стратегич. задач в ретросинтетическом
анализе. При этом целесообразно осуществлять разборку (на схемах символ )
целевой молекулы таким образом, чтобы она вела к наиб. "распознаваемым"
(т.е. хорошо разработанным и употребительным) синтонам. Так, напр., целесообразным
путем ретросинтетич. анализа карбоновых к-т может служить разборка (а), ведущая
к рассмотренным выше синтонам, либо разборка (б), ведущая к синтонам
I и II:
)
целевой молекулы таким образом, чтобы она вела к наиб. "распознаваемым"
(т.е. хорошо разработанным и употребительным) синтонам. Так, напр., целесообразным
путем ретросинтетич. анализа карбоновых к-т может служить разборка (а), ведущая
к рассмотренным выше синтонам, либо разборка (б), ведущая к синтонам
I и II:
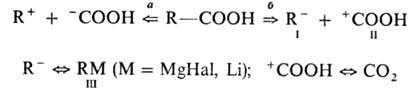
Реагентами, эквивалентными
синтонам I и II, могут служить соотв. металлоорг. соед. III и СО2,
а реальными р-циями, отвечающими такой разборке,-р-ции 10 и 11:
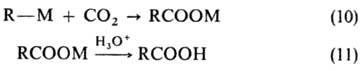
Использование синтонного
подхода в поиске оптим. путей синтеза позволяет в значит. мере формализовать
(свести к набору нек-рых руководящих правил) выбор пути О. с., основывавшийся
ранее гл. обр. на личном опыте и интуиции исследователя. Синтонный подход позволяет
иногда прийти чисто логич. путем к решениям эвристич. характера. Последнее связано
гл. обр. с использованием "переполяризованных" синтонов, в к-рых
вводимый в молекулу фрагмент характеризуется необычной, парадоксальной, с точки
зрения обычных представлений орг. химии, полярностью или структурой. Примером
может служить ретросинтетич. анализ альдегидов (12), ведущий к электроф. синтону
R+, синтетич. эквиваленты к-рого традиционны, и "парадоксальному"
синтону -СН=О. Последний м. б. реализован путем использования его
синтетич. эквивалента-метилен-дитиоацеталя (IV), включение к-рого в последовательность
р-ций (13) обеспечивает возможность генерирования карб-аниона (V) и получение
целевого альдегида:
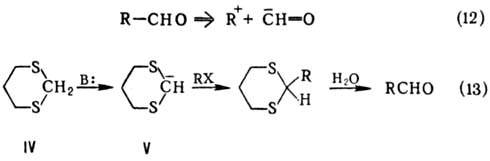
Т. обр., последовательность
р-ций (13) эквивалентна первоначальной парадоксальной разборке (12).
Наряду с традиц. синтетич.
методами, обеспечивающими сборку одной связи в молекуле, большую роль играют
методы, в к-рых р-ция или последовательность р-ций обеспечивает образование
неск. связей и одновременно сборку крупного мол. фрагмента, как, напр., в аннелировании
по Робинсону (см. Робинсона -Манниха реакция). Поскольку методы такого
типа позволяют решать не только частные тактич. задачи, но и вопросы целостного
построения ключевого элемента структуры конечного продукта, их принято относить
к числу стратегических.
При разработке стратегии
сложного О. с. используют неск. разл. подходов. В логич. отношении наиб. простой
из них состоит в последоват. ретросинтетич. разборке связей, входящих в целевую
молекулу таким образом, чтобы в итоге выйти к подходящим исходным соединениям.
Каждый шаг такой разборки должен приводить к распознаваемым синтонам, с тем
чтобы обратная операция (сборка соответствующей связи в реальном синтезе) была
обеспечена эффективным синтетич. методом. Для любой более или менее сложной
орг. молекулы можно написать множество ретросинтетич. схем, построенных на таком
принципе. Это же справедливо и для большинства промежут. соед., возникающих
на каждом шаге ретросинтетич. анализа. В результате строится "древо"
решений, выбор оптим. пути в к-ром требует глубокого анализа. Исследование теоретич.
основ О. с. направлено, в частности, на создание методов отсечения наим. перспективных
вариантов и поиск наиб. плодотворных. В этих исследованиях ключевое место занимает
понятие стратегии,
связи, т.е. такой связи, с разборки к-рой целесообразно начинать ретросинтетич.
анализ (для целевых и промежут. соед.). Сформулирован ряд принципов выбора стратегич.
связи, формализованных до такой степени, что на их основе появилась возможность
создания программ для ЭВМ с целью осуществления ретросинтетич. анализа в т.
наз. компьютерном синтезе. Однако такой подход имеет ряд недостатков.
Один из них состоит в том, что молекула в этом случае рассматривается как сумма
ковалентных связей, т.е. без учета специфики, присущей конкретной структуре
как целому.
Тщательный же анализ такой
специфики (второй путь планирования О. с.) позволяет в ряде случаев находить
неожиданные эвристич. решения, обеспечивающие высокую эффективность синтеза.
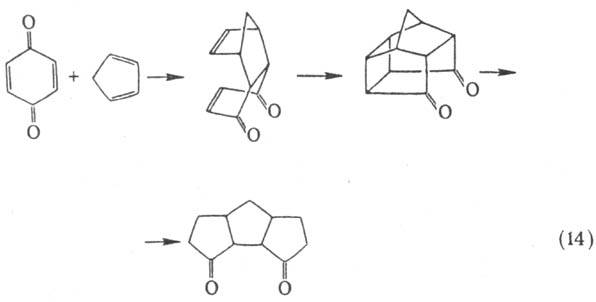
Пример такого решения трехста-дийный синтез прир. производных циклопентаноидов
(14), осуществленных Г. Мета и А. Редди в 1981:
Третий принцип планирования
состоит в выборе той или иной стратегич. р-ции как ключевой стадии синтеза (напр.,
построение присущего целевому соед. углеродного скелета) с послед. ретросинтетич.
"подгонкой" целевой структуры к продукту этой р-ции. Несмотря на
то что такой путь обычно сопряжен с включением в схему синтеза ряда дополнит.
стадий (введения, удаления или защиты функц. групп), он нередко обеспечивает
высокую эффективность схемы в целом, поскольку позволяет в одну-две стадии решить
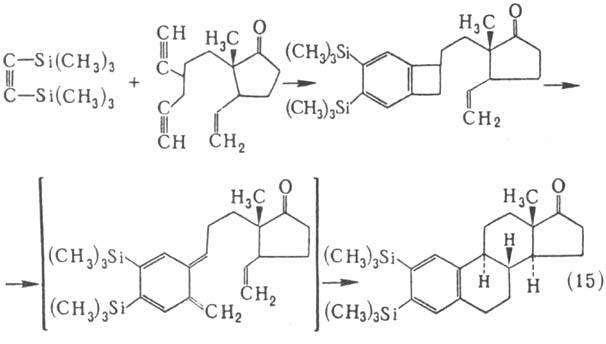
осн. стратегич. задачу синтеза. Так, в кратчайшем из известных на сегодня синтезе
стероидов (его разработали Р. Фанк и К. Фольгардт в 1980) задача создания полициклич.
скелета решается с помощью трех стратегич. р-ций, выполняемых в одном реакц.
сосуде без выделения промежут. продуктов (схема 15):
"Болевая точка"
многостадийного синтеза - низкий выход целевого продукта. При среднем выходе
на стадию У общий выход на п стадий составляет Yn =
Yn.
Поэтому важно при планировании
сложного синтеза минимизировать число стадий и выбирать наиб. эффективные синтегич.
методы для его осуществления.
Др. путь повышения общего
выхода - использование т. наз. конвергентных схем синтеза. При традиц. подходе
сборка сложной молекулы
из фрагментов Аi осуществляется путем последоват. усложнения
исходного субстрата в соответствии с "линейной" схемой (16):
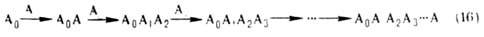
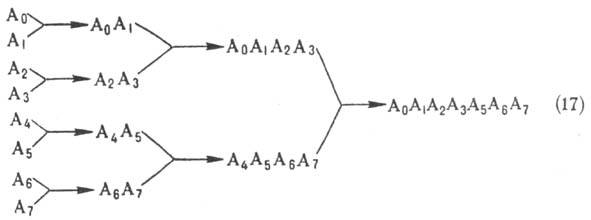
В отличие от такого приема,
конвергентные схемы синтеза предполагают параллельную сборку укрупняющихся мол.
блоков и заключит. сборку целевой молекулы из двух крупных блоков по схеме типа
(17):
Для такой полностью конвергентной
схемы зависимость общего выхода от числа стадий имеет вид 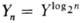 , что обусловливает значительно более слабую зависимость Yn
от числа стадий (см. также табл.).
, что обусловливает значительно более слабую зависимость Yn
от числа стадий (см. также табл.).
ЗАВИСИМОСТЬ ВЫХОДА КОНЕЧНОГО
ПРОДУКТА (В %) ОТ ЧИСЛА СТАДИЙ (средний
выход одной стадии 80%)
|
Схема синтеза |
Число стадий |
||||||
|
8 |
16 |
32 |
64 |
80 |
|||
|
Линейная |
16.8 |
2,8 |
0,08 |
6 10 5 |
2 10 6 |
||
|
Конвергентная |
51,2 |
41 |
32,8 |
26 |
24,4 |
||
Конвергентные схемы имеют
также др. преимущества перед линейными: возможность разобщения сходных функц.
групп по разным ветвям схемы, в результате чего значительно упрощаются задачи
обеспечения селективности р-ций (см. Региоселективностъ и региоспецифичность);
возможность одновременной проработки разл. ветвей схемы, а также внесения
необходимых изменений в те или иные участки схемы без нарушения общего стратегич.
замысла. Осуществимость конвергентного пути синтеза строится на использовании
р-ций, обеспечивающих возможность сборки молекул из крупных блоков, что, наряду
с синтонным подходом, в значит. мере обусловило успехи О. с. (синтез хлорофилла,
витамина В12, полинуклеотидов и др.) и перевод многих чисто препаративных
синтезов в промышленные (напр., синтез стереоидных гормонов и простагландинов).
Лит.. Чижов О. С.,
Чижов А О., Рациональное планирование сложного органического синтеза, М., 1986;
Бочков А Ф , Смит В А., Органический синтез, М., 1987. А.Ф. Бочков.


