ОКТАНЫ (от греч.
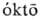 - восемь)
С8Н18, мол. м. 114,224. Существует 18 изомерных октанов.
В статье описаны нормальный октан СН3(СН2)6СН3
и изооктан (СН3)3ССН2СН(СН3)2
(2,2,4-триметилпентан). О.-бесцв. жидкости (см. табл.) со слабым запахом прямогонного
бензина, неограниченно смешиваются с углеводородами, плохо раств. в диэтиловом
эфире, ацетоне и этаноле, практически не раств. в воде; изооктан образует бинарные
азео-тропные смеси с бензолом, метанолом, этанолом и др. спиртами.
- восемь)
С8Н18, мол. м. 114,224. Существует 18 изомерных октанов.
В статье описаны нормальный октан СН3(СН2)6СН3
и изооктан (СН3)3ССН2СН(СН3)2
(2,2,4-триметилпентан). О.-бесцв. жидкости (см. табл.) со слабым запахом прямогонного
бензина, неограниченно смешиваются с углеводородами, плохо раств. в диэтиловом
эфире, ацетоне и этаноле, практически не раств. в воде; изооктан образует бинарные
азео-тропные смеси с бензолом, метанолом, этанолом и др. спиртами.
О.-типичные алифатич. углеводороды.
При пиролизе октана образуются в осн. метан, этан, этилен; при крекинге на алюмосиликатном
катализаторе возрастает выход углеводородов С3-С5; в присут.
ароматизирующих катализаторов (Pt/C, оксиды Сг, Мо, V на Аl2О3)
при 450-500 °С с высоким выходом образуется смесь о-ксилола и этилбен-зола.
Изооктан при нагр. до 500-570 °С превращается в смесь метана и изобутилена
с небольшим содержанием этана, этилена, пропилена и водорода; при каталитич.
крекинге в присут. WS2 при 400 °С и давлении 25 МПа или с АlСl3
и НСl при 20-140°С образуется в осн. изобутан; с алюмосиликатами при 500
°С- метан, бутан, изобутан, бутилен и изобутилен, а при 550 °С также
пропилен.
НЕКОТОРЫЕ СВОЙСТВА ОКТАНОВ
|
Показатель |
Октан |
Изооктан |
||
|
Т.пл., °С |
-56,798 |
-107,38 |
||
|
Т.кип., °С |
125,667 |
99,24 |
||
|
|
0,7026 |
0,6919 |
||
|
n20D |
1,3974 |
1,39145 |
||
|
tкрит
, °С |
296,2 |
- |
||
|
pкрит,
МПа. |
2,464 |
- |
||
|
dкрит
кг/м3 . |
235,0 |
- |
||
|
|
1,641 |
1,648 |
||
|
|
4,088 |
3,699 |
||
|
|
-207,94 |
-224,68 |
||
|
|
-5474,37 |
-5464,99 |
||
|
|
16,32 |
12,552 |
||
|
КПВ, % по объему |
0,95-6,5 |
0,95-6 |
||
|
Т. самовоспл.,
°С |
220 |
430 |
||
|
Т.всп., оС |
13 |
-9 |
||
Октан содержится в бензиновой
фракции нефти и продуктах ее деструктивной переработки, в алкилате, образуется
при синтезе углеводородов по методу Фишера-Тропша. В пром-сти его выделяют из
указанных продуктов ректификацией в сочетании с селективной адсорбцией на цеолитах
или комплексообразованием с мочевиной. В лаб. условиях получают гидрированием
октенов, по р-ции Вюрца из 1-хлорбутана и др.
Технически чистый изооктан
получают димеризацией изобутилена с послед. гидрированием на никелевом или медно-хромовом
катализаторе. При алккилировании изобутана изобутиленом в присут. H2SO4,
HF или др. кислотных катализаторов получают техн. изооктан, содержащий значит.
кол-ва изомерных октанов разветвленного строения и продуктов полиалкилирования
(т-ра выкипания 98-185 °С, октановое число 92-97).
Применяют октан в произ-ве
ксилолов, октанола, окта-наля, а также как р-ритель. Как компонент бензина большого
значения не имеет из-за низкой детонац. стойкости (октановое число 19). Применение
изооктана обусловлено его
высокой детонац. стойкостью (октановое число принято за 100). Технически чистый
изооктан используется в качестве первичного эталонного топлива для определения
сортности бензина, технический-как компонент авиац. бензинов. Хим. превращ.
изооктана практич. значения не имеют.
Октаны легко воспламеняются,
в смеси с воздухом взрывоопасны. Нетоксичны, не обладают аллергенными и канцерогенными
св-вами.
Лит.: Петров Ал.
А., Химия алканов, М., 1974. А. А. Братков.



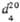
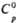 , кДж(кг·К)
, кДж(кг·К)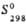 , кДж/(кг·К)
, кДж/(кг·К)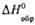 , кДж/моль
, кДж/моль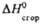 , кДж/моль
, кДж/моль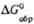 ,
кДж/моль
,
кДж/моль