НОРБОРНАДИEН (бицикло[2.2.1]гепта-2,5-диен,
ф-ла I), мол.м. 92,2; бесцв. жидкость; т.пл. - 19,1°С, т.кип. 89,5 °С;
d420 0,9064; nD20
1,4702; DH0обр (газ) -240,16 кДж/моль; не раств.
в воде, раств. в орг. р-рителях. Н.-бициклич. напряженный диен, обладает высокой
реакц. способностью.
Каталитич. гидрирование
Н. приводит последовательно к
норборнену и норборнану. При нагревании Н. изомеризуется
в циклогептатриен (тропилиден). Для Н. характерны разл.
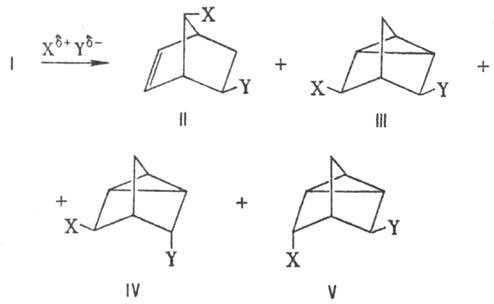
типы перегруппировок в р-циях электроф. и радикального присоединения,
напр. перегруппировка Вагнера-Меервейна с образованием
соед. ф-лы II (см. Норборнен), а также перегруппировки,
связанные с участием второй двойной связи и приводящие
к соед. нортрицикленового скелета с экзо- и эндо-конфигурациями
заместителей (III-V):
Н. вступает в диеновый
синтез в качестве диенофила по одной или обеим связям С=С; р-цией Н. с гексахлорцикло-пентадиеном
получен альдрин (см. Инсектициды).
Взаимное превращение Н.
и квадрициклана-наиб. изученная р-ция валентной изомеризации:
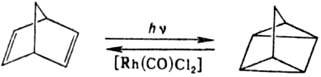
Обратная р-ция идет с выделением
энергии, что может найти практич. применение в фотохим. аккумуляторах солнечной
энергии.
Получают Н. диеновым синтезом
из циклопентадиена и ацетилена при 350°С.
Н.-промежуточное соед.
в синтезе простатландинов.
Для стабилизации при хранении
к Н. добавляют ингибитор 2,6-ди-трет-бутил-4-метилфенол (0,05%).
Лит.: Неницеску
К. Д., Органическая химия, пер. с румын., т. 1, М., 1963, с. 304; Общая органическая
химия, пер. с англ., т. 1, М., 1981, с. 598.
Н. В. Зык.


