НИТРОХЛОРБЕНЗОЛЫ, соед.
общей ф-лы ClC6H5-n(NO2)n.
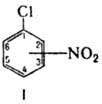
Наиб. практич. интерес представляют мононитрохлорбен-золы (ф-ла I; мол. м. 157,56)
и динитрохлорбензолы. Все мононитрохлорбензолы-
светло-желтые кристаллы (см. табл.); 3-Н.
существует в стабильной и метастабильной модификациях. Не раств. в воде, хорошо
раств. в этаноле, диэтиловом эфире,
бензоле, ацетоне, хлороформе.
Большинство хим. превращений 2- и 4-Н. связано с подвижностью атома Сl, обусловленной сильным электроноакцепторным действием группы NO2. В р-циях с разл. нуклеофилами атом Сl замещается на группы OAlk, Alk, OAr, NH2, NAlk2, CONH2 и CN.
3-Н. в р-ции замещения атома
Сl не вступает. 4-Н. под действием Na2S2
образует 4,4'-динитродифенилдисулъфид-промежут. соед. в произ-ве сульфаниламидных
препаратов. Восстановление Н. в кислой среде приводит к соответствующим аминопроизводным,
напр. при действии на 4-Н. SnCl2 в НСl образуется 4-хлор-анилин.
В щелочной среде Zn и Fe восстанавливают Н. до гидразосоединений; напр., 2-Н.
превращ. в 2,2'-дихлоргидра-зобензол, к-рый при подкислении перегруппировывается
в 3,3'-дихлорбензидин. Р-ции электроф. замещения идут по ароматич. ядру, причем
заместитель входит, как правило, в мета-положение по отношению к группе
NO2. Так, хлорирование 4-Н. хлором приводит к 1,2-дихлор-4-нитробензолу,
сулъфирование под действием Н2SО4-к 2-хлор-5-нитро-бензолсульфокислоте;
2-Н. при сульфировании превращ. в 3-нитро-4-хлорбензолсульфокислоту. Нитрование
Н. нитрующей смесью (56% H2SO4, 30% HNO3 и
14% H2O) при 65 °С приводит к образованию динитрохлорбензолов.
Так, при нитровании 2-Н. образуется смесь 2,4-динитрохлор-бензола (основной
продукт), 2,6- и 3,4-динитрохлорбензолов, при нитровании 4-Н.-2,4-динитрохлорбензол.
СВОЙСТВА МОНОНИТРОХЛОРБЕНЗОЛОВ

* Стабильная модификация,
nD80 1,5374. ** nD100
1,5376.
В пром-сти 2- и 4-Н. получают
нитрованием хлорбензола при 40-70°С нитрующей смесью (52,5% H2SO4,
35,5% HNO3 и 12% Н2О) по непрерывной технологии. Образующуюся
смесь изомеров (34% 2-Н., 65% 4-Н. и 1% 3-Н.) охлаждают до 15°С; при этом
большая часть 4-Н. выкристаллизовывается. Из остатка фракционной перегонкой
с послед. кристаллизацией выделяют 2-Н. (3-Н. при такой схеме процесса обычно
не выделяют). 3-Н. получают хлорированием нитробензола в присут. иода. Др. лаб.
способы получения Н.-диазотирование соответствующих нитроани-линов и взаимод.
нитрофенолов с РСl5.
Аналит. определение Н.
осуществляют, восстанавливая их в соответствующие амины; последние с фенолом
и NaClO дают синее окрашивание.
2- и 4-Н.- сырье для произ-ва
нитроанилинов, анизидинов, нитро- и аминофенолов, n-фенилендиамина, динитрохлорбензолов,
1,2-дихлор-4-нитробензола-промежут. продуктов в синтезе
азокрасителей, сернистых красителей, пигментов, ингибиторов коррозии, реактивов
для фотографии, инсектицидов (напр., паратиона), лек. ср-в. 3-Н. используют
только в орг. синтезе.
Н. токсичны при вдыхании
и попадании внутрь, раздражают кожу. Окисляют гемоглобин крови в метгемоглобин
(наиб. действием обладает 3-Н.), отрицательно действуют на ф-цию печени, тройничный
и зрительный нервы, вестибулярный аппарат, вегетативную нервную систему. ПДК
1 мг/м3.
Произ-во в США 2-Н. 25
тыс. т, 4-Н. 45 тыс. т (1981).
Лит. см. при ст.
Нитросоединения. В. И. Ерашко.


