НИТРОНЫ, N-оксиды
азометинов, соед. общей ф-лы 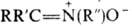 . Различают альдонитроны (R-H, R' и R:-орг. радикалы) и кетонитроны (R,
R', R: - орг. радикалы). По номенклатуре
ИЮПАК Н. называют, добавляя слово "оксид" к назв. алкилиденамина,
напр.
. Различают альдонитроны (R-H, R' и R:-орг. радикалы) и кетонитроны (R,
R', R: - орг. радикалы). По номенклатуре
ИЮПАК Н. называют, добавляя слово "оксид" к назв. алкилиденамина,
напр.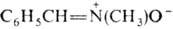 N-бензилиденметиламин-N-оксид.
Н. изомерны сазиридинам (изонитронам).
N-бензилиденметиламин-N-оксид.
Н. изомерны сазиридинам (изонитронам).
Н., как правило, кристаллич.
в-ва. ИК спектр имеет характеристич. полосу при 1550-1620 см-1 (C=N),
в УФ спектрах несопряженных Н. lмакс 240 нм (lge ~ 4), в спектре
ПМР альдонитронов хим. сдвиг (d) ~ 7 м.д. (a-Н), в спектре ЯМР 13С
хим. сдвиг a-С-атома ~ 142 м.д.
Электронное строение Н.
может быть представлено резонансными структурами:
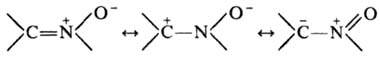
Н.-слабые основания, при
действии к-т протонируются по атому О с образованием непрочных солей. Алкилирова-ние
и ацилирование также происходят по атому О; ацили-рование обычно сопровождается
перегруппировкой, приводящей к амидам:
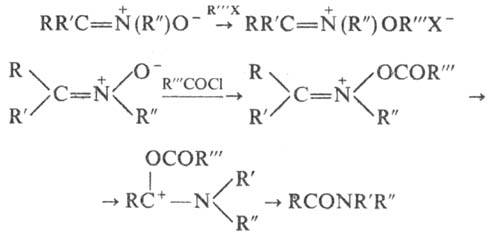
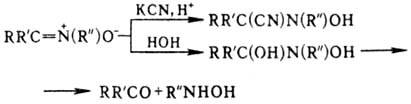
Н. вступают в р-ции 1,3-присоединения
с нуклеофилами, образуя производные М,М-дизамещенных гидроксиламина; при гидролизе
образуются карбонильные соед. и гидро-ксиламины:
Атомы водорода С-алкильных
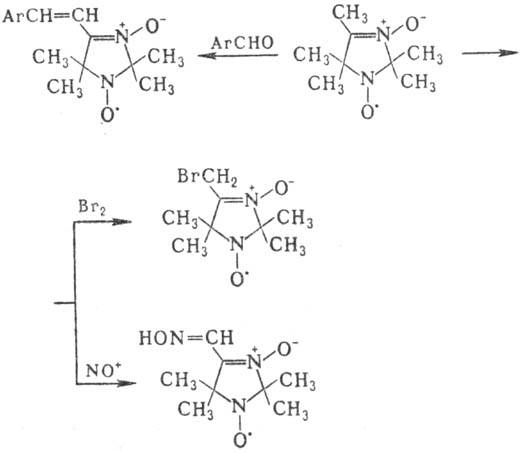
групп обладают кислыми св-вами: легко обмениваются на дейтерий, галоген, нитро-зогруппу,
вступают в конденсацию типа альдольной, напр.:
Н. легко вступают в р-ции
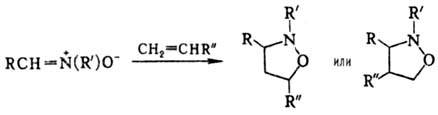
диполярного [3 + 2]-цикло-присоединения с алкенами, диенами и др. Альдонитроны,
особенно в случае цис-расположения атомов Н и О, более реакционноспособны,
чем кетонитроны. Р-ции позволяют получать с высокими выходами разл. гетероциклич.
соед., напр.:
Под действием сильных оснований
Н. претерпевают 1,3-прототропный сдвиг:
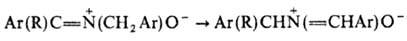
Нек-рые Н. легко дают циклич.
димеры; при УФ облучении изомеризуются в оксазиридины, при нагр. происходит
обратная р-ция:
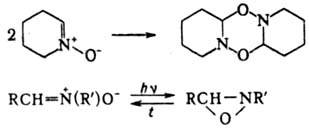
Н. устойчивы к действию
большинства окислителей. Водный р-р периодата окисляет альдонитроны до N-гидрокси-амидов.
Восстановление Н. комплексными гидридами металлов приводит к N,N-дизамещенным
гидроксиламина, а при каталитич. восстановлении образуются азометины и вторичные
амины:
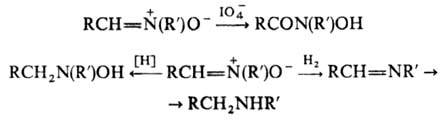
Н. реагируют со своб. радикалами
с образованием нитро-ксильных радикалов, что используют в методе спиновых ловушек:
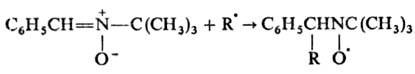
Осн. методы синтеза Н.:
1) конденсация карбонильных соед. с N-замещенными гидроксиламина:
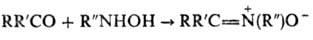
2) алкилирование оксимов
алкилгалогенидами или непредельными карбонильными соед., напр.:
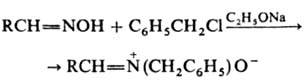
3) конденсация нитрозоароматич.
соед. с бензилгалогени-дами или N-метиленпиридиниевыми солями:
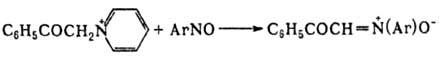
4) окисление N,N-дизамещенного
гидроксиламина:
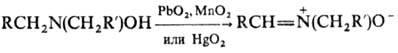
Благодаря доступности и
многообразию превращений Н. широко применяются для синтеза сложных прир. в-в,
стабильных нитроксильных радикалов и в изучении механизмов р-ций.
Лит.: Общая органическая
химия, пер. с англ., т. 3, М,, 1982, с. 613-18; Имидазолиновые нитроксильные
радикалы, Новосиб., 1988; Breuer Eli, The chemistry of functional groups, ed.
by S. Patai, pt 1, 1982. Л.Б. Володарский.


