НИКЕЛЯ СУЛЬФИДЫ. М
о н о с у л ь ф и д NiS-нестехио-метрич. соед., для него, как и для др. Н. с.,
характерна определенная область гомогенности (см. табл.); существует в двух
кристаллич. модификациях; т-ра перехода g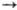 b снижается от 389 °С (при содержании S 50 ат. %) до 282 °С (~ 50,2
ат. % S).
b снижается от 389 °С (при содержании S 50 ат. %) до 282 °С (~ 50,2
ат. % S).
С у л ь ф и д Ni3S2
переходит при 555 °С в высокотемпературную фазу Ni3bxS2
с широкой областью гомогенности. Сульфид Ni3S4 разлагается,
не плавясь, при 356 °С на NiS2 и b-NiS. Получены нестехиометрич.
фазы: Ni6S5 (существует в интервале т-р 397-573 °С,
разлагается при 573 °С на Ni3+xS2 и
b-NiS) и Ni7S6 (при 399°С разлагается на Ni6S5
и b-NiS). Все Н. с. практически не раств. в воде, орг. р-рителях. Разлагаются
HNO3, царской водкой. При нагр. в вакууме выше 500 °С диссоциируют
с образованием паров S и фаз, обогащенных Ni. При нагр. на воздухе окисляются.
Получают Н. с. взаимод.
Ni с S при нагр. в вакууме; NiS, NiS2-прокаливанием смеси NiO (или
NiCO3) с S и К2СО3. Моносульфид получают также
осаждением H2S из водных р-ров солей Ni в слабокислой среде-вначале
осаждается черный аморфный NiS, р-римый в разб. соляной к-те (т. наз. a-NiS),
к-рый затем переходит в b-NiS, нерастворимый в разб. соляной к-те. Ni3S2,
Ni6S5-компоненты никелевого файнштейна (промежут. продукта
переработки на Ni силикатно-никелевых и др. руд).
В природе Н. с. встречаются
в виде минералов: миллерита (желтый никелевый колчедан) g-NiS, хизлевудита Ni3S2,
годлевскита Ni7S6, полидимита Ni3S4,
ваэсита NiS2, пент-ландита Ni5-xFе4+хS8
(0<= х<= 0,5). Руды, содержащие пент-ландит, миллерит,-сырье в
произ-ве Ni; NiS, Ni3S2-катализаторы гидрогенизации и
дегидрогенизации; NiS2-катализатор в орг. синтезах.
Н. с. токсичны. ПДК в воздухе
рабочей зоны 0,005 мг/м3.
Лит.: Самсонов Г.
В., Дроздова С. В., Сульфиды, М., 1972, с. 186-90; Ванюков А. В., Исакова Р.
А., Быстрое В. П., Термическая диссоциация сульфидов металлов, А.-А., 1978,
с. 82-90. И. Н. Один.


