НИАЦИН (витамин
РР, от англ. pellagra preventing -предупреждающий пеллагру), группа биологически
активных соед., включающая никотиновую кислоту и ее производные. Наиб.
распространены в природе сама к-та и ее амид, обладающие одинаковой витаминной
активностью.
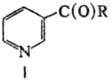
Н и к о т и н о в а я к-та
(мол. м. 123,11; ф-ла I, R = OH)-бесцв. кристаллич. в-во, т. пл. 236-237 °С.
Водный р-р имеет максимумы поглощения при 261,5 нм (e = 3,1•103 при
рН 5,6) и 385 нм. Н и к о т и н а м и д (мол. м. 122,13; I, R = NН2)-
бесцв. кристаллич.
в-во, т. пл. 128-131 °С; хорошо раств. в воде
и этаноле, плохо-в хлороформе, ацетоне и эфире. Для водного
р-ра максимумы поглощения при 261,5 нм (e = 2,85.103
при рН 5,72) и 300 нм. Оба соед. весьма устойчивы при хранении
и выдерживают нагревание в водных р-рах при 120°С. В р-рах к-т и щелочей
никотинамид превращ. в никотиновую к-ту.
Биол. роль никотиновой
к-ты и никотинамида обусловлена их участием в биосинтезе никотинамидных кофермен-тов
(коферментных форм Н.): н и к о т и н а м и д а д е н и н-н у к л е о т и д
а (НАД; II, R = Н) и н и к о т и н а м и д а д е н
и н д и н у к л е о т и д ф о с ф а т а [HАДФ; II, R = PO(OH)2].
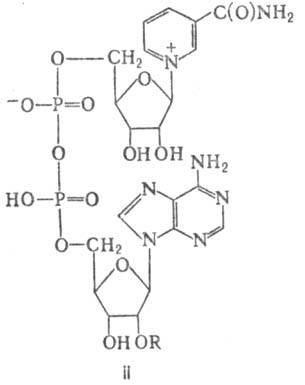
НАД и НАДФ - коферменты
многочисленных (более 100) де-гидрогеназ, функционирующих на начальных этапах
биол. окисления самых разнообразных соед.: углеводов, аминокислот, жирных к-т
и др. Среди них ферменты гликолиза (глицеральдегидфосфатдегидрогеназа, лактатдегидрогеназа),
пентозофосфатного цикла окисления углеводов (глюкозо6-фосфат-дегидрогеназа,
6-фосфоглюконатдег идрогеназа), цикла трикарбоновых
к-т (малат- и изоцитратдегидрогеназы) и др.
В катализируемых этими
ферментами окислит.-восстано-вит. р-циях НАД и НАДФ играют роль промежут. акцепторов
и переносчиков электронов и атомов водорода. Механизм переноса сводится к обратимому
восстановлению пиридинового кольца в молекуле никотинамидных кофер-ментов, напр.:
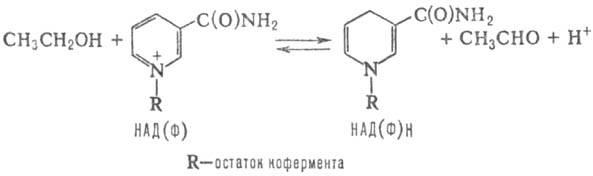
В результате таких р-ций
НАД и НАДФ переходят в восстановленное состояние - НАДН и НАДФН. Когда последние
выступают в качестве доноров электронов и протона, эти превращ. протекают в
обратном направлении. Образование НАД(Ф)Н осуществляется стереоспецифично.
Функцион. различие между
двумя коферментными формами состоит в том, что НАДН, как правило, служит поставщиком
электронов в цепь биол. окисления, сопряженного с окислительным фосфорилированием,
т. е. с процессами аккумуляции
энергии в форме АТФ; НАДФН служит доно-ром водорода при биосинтезе жирных к-т
и стеринов с участием ацетил-кофермента А; восстановит. аминировании кетокислот
с образованием из них аминокислот (напр., глутаминовой к-ты из a-кстоглутаровой);
восстановлении рибозы до дезоксирибозы; образовании восстановленных форм фолиевой
к-ты (ди- и тетрагидрофолата; см. Фолацин); восстановлении глутатиона
и метгсмоглобина; в разл. р-циях гидроксилирования и др. Кроме того, никотинамид-ным
коферментам принадлежит важная роль в генерировании Н+ при секреции
соляной к-ты в желудке.
Наряду с коферментными
ф-циями, выполняемыми в составе дегидрогеназ, НАД является также аллостерич.
регулятором (регуляторные ф-ции обусловлены воздействием на участки фермента,
не входящие в активный центр) активности ряда ключевых ферментов энергетич.
обмена; донором остатка адениловой к-ты при репарации (восстановлении) разрывов
фосфодиэфирных связей в цепях ДНК, осуществляемой ДНК-лигазой; регулятором синтеза
и репликации (самовоспроизведении) ДНК и др.
Биосинтез никотинамидных
коферментов осуществляется в организме человека и животных из никотиновой к-ты
и никотинамида с участием АТФ. В своб. виде никотиновая к-та и никотинамид в
животных тканях присутствуют в незначит. кол-ве. Почти весь присутствующий в
организме Н. находится в виде остатка никотинамида, включенного в состав молекул
никотинамидных коферментов. Конечные продукты обмена Н. в организме, в виде
к-рых они гл. обр. выводятся с мочой,-N-метилникотиновая к-та (тригонел-лин),
никотинилглицин (никотинуровая к-та), N-метилнико-тинамид, N-оксид никотинамида
и др.
В отличие от большинства
др. витаминов Н. может частично образовываться в организме в результате эндогенного
синтеза из триптофана. При этом из 60 мг L-трипто-фана образуется 1 мг никотиновой
к-ты. Потребность человека (и животных) в этом витамине принято выражать в ниациновых
эквивалентах: 1 такой эквивалент равен 1 мг никотиновой к-ты или 60 мг L-триптофана.
Кол-во Н., образующегося в организме человека, невелико, и основная его часть
должна поступать с пищей. Потребность здорового человека в Н. составляет 6,5
мг на 1000 ккал (4187 кДж) энергозатрат или 15-25 мг никотиновой к-ты в сутки.
Потребность в витамине возрастает при тяжелой физич. работе, беременности и
кормлении, приеме нек-рых лек. ср-в (напр., сульфаниламидных препаратов, антибиотиков).
При недостаточном поступлении
в организм Н. наблюдаются вялость, апатия, быстрая утомляемость, головокружение,
бессонница, сердцебиение, бледность и сухость кожи, пониж. сопротивляемость
к инфекц. заболеваниям. При глубоком дефиците Н. развивается пеллагра - тяжелое
заболевание с поражением желудочно-кишечного тракта, кожи, центр. и периферич.
нервной системы.
Для профилактики ниациновой
недостаточности проводится обогащение муки никотиновой к-той (вместе с витаминами
B1 и В2). Источником Н. для человека служат мясо (4-18
мг на 100 г продукта), печень (7-47), крупы (напр., в гречневой 4), хлеб грубого
помола. Очень высоко содержание Н. в дрожжах (в сухих пекарских 25-50, в сухих
пивных 34-93) и сушеных грибах. Овощи более бедны ниацином (0,5-2,5). Также
мало Н. в молоке (0,1-0,5), но с учетом содержания триптофана оно является хорошим
источником ниациновых эквивалентов. В растит. продуктах значит. доля Н. представлена
никотиновой к-той, в продуктах животного происхождения-никотинамидом, остаток
к-рого входит в состав молекул никотинамидных коферментов. Консервирование,
замораживание и сушка мало влияют на содержание Н. в пищ. продуктах. Тепловая
обработка (варка, жарение) снижают его содержание на 15-20%.
Никотиновую к-ту (и никотинамид
после его гидролиза до никотиновой к-ты) определяют колориметрически по окрашиванию,
образующемуся при ее взаимод. с бромцианом и ароматич. амином (напр., с анилином),
а также микробиологически - с помощью Lactobacillus arabinosus. НАД и
НАДФ определяют флуориметрически по флуоресцирующему соед., образующемуся при
их взаимод. в щелочной среде с ацетоном или метилэтилкетоном. Восстановленные
формы кофермента м.б. определены спектрофотометри-чески по характерному интенсивному
поглощению при 340 нм. Раздельное определение НАД и НАДФ осуществляют с использованием
очищенных апоферментов алко-гольдегидрогеназы, к-рая активна в присут. НАД и
НАДН, и глюкозо-6-фосфат-дегидрогеназы, к-рая функционирует только в присут.
НАДФ и НАДФН.
Н., чаще всего в форме
никотинамида, входит в состав большинства поливитаминных препаратов, к-рые используют
для профилактики полигиповитаминозов и оптимизации витаминной обеспеченности
разл. групп населения.
О пром. получении Н. см.
Никотиновая кислота.
Лит.: Халмурадов А. Г., в кн.: Экспериментальная витаминология, Минск, 1979, с. 411-37; Hankes L. V., в кн.: Handbook of vitamins. Nutritional, biochemical and clinical aspects, N.Y.-Basel, 1984, p. 329-78. В.Б. Спиричев.


