НАТРИЯ ФОСФАТЫ, ортофосфаты,
пирофосфаты (дифос-фаты) и конденсир. фосфаты натрия. Кристаллич. или стеклообразные
в-ва, хорошо раств. в воде, образуют кристаллогидраты (см. табл. 1,2). О р т
о ф о с ф а т Na3PO4, д и г и д р о о р т о ф о с ф а
т NaH2PO4 и г и д р о о р т о ф
о с ф а т Na2HPO4 получают взаимод. Н3РО4
с Na2CO3 или NaOH
с послед. кристаллизацией солей и высушиванием их до безводных
солей или кристаллогидратов NaH2PO4.H2O,
Na2HPO4.12H2O и Na3PO4.12H2O.
Последний получают также нагреванием АlРО4 с Na2CO3
при 900 oС с послед. выщелачиванием водой и кристаллизацией из р-ра.
П и р о ф о с ф а т Na4P2O7
полиморфен; тригидро-NaH3P2O7, дигидро-Nа2Н2Р2О7
и гидропирофосфаты Na3HP2O7 разлагаются выше
250оС с образованием конденсированных
Н.ф. Получают нейтрализацией Н4Р2О7 щелочью,
дегидратацией гидроортофосфатов Na, Na3HP2O7
x х 9Н2О-подкислением р-ра Na4P2O7
соляной к-той.
Табл. 1.-СВОЙСТВА
ОРТО- И ПИРОФОСФАТОВ НАТРИЯ
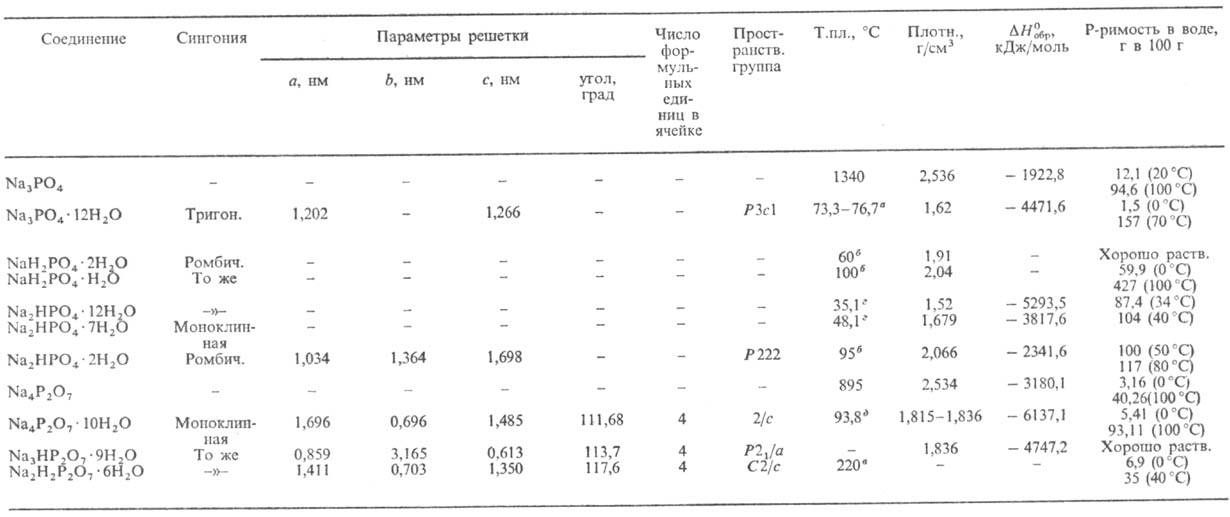
a С
потерей воды, полное обезвоживание при 100 °С. б
Полное обезвоживание при 95 °С. в Полное обезвоживание.
г С потерей 5 молекул воды. д Теряет
1 молекулу воды, не плавясь.
Табл. 2.-ХАРАКТЕРИСТИКА
КОНДЕНСИРОВАННЫХ ФОСФАТОВ НАТРИЯ
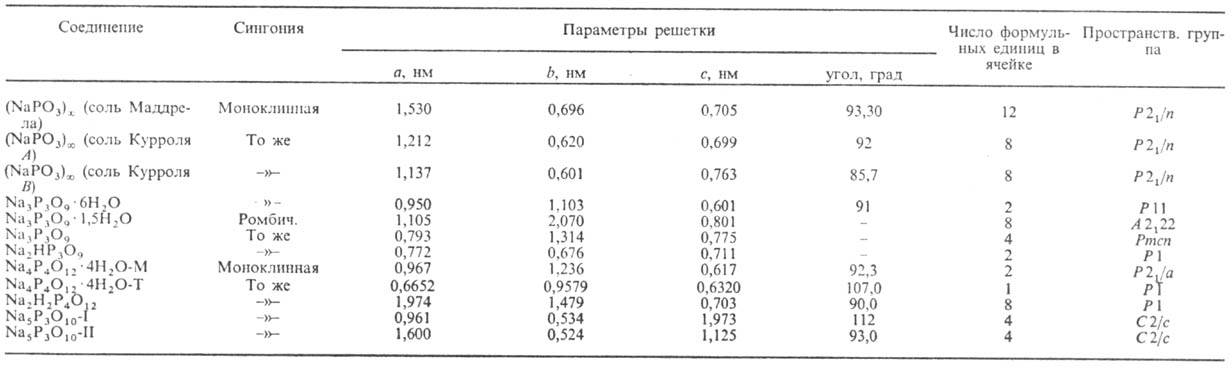
К о н д е н с и р о в а
н н ы е Н.ф. (устар. назв.-метафосфаты натрия) содержат группировку (РО3)-.
Полифосфаты 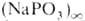 имеют линейное цепочечное строение, циклофос-фаты (NaPO3)n,
где п = 3,4,12-циклическое.
имеют линейное цепочечное строение, циклофос-фаты (NaPO3)n,
где п = 3,4,12-циклическое.
Структура полифосфатов
Na определяется условиями их получения. Нагревание NaH2PO4
при 500°С приводит к получению нерастворимой в воде соли Маддрела. При дегидратации
расплава NaH2PO4 при высоких т-рах образуется соль Грэма
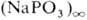 -гигроскопичное
водорастворимое стекло. Если расплавл. массу выдерживают при 550-560°С и
вносят затравку, то получают соль Курроля-ограниченно растворимый в воде полифосфат
с волокнистой структурой. В пром-сти трициклофосфат Na3P3O9
получают дегидратацией NaH2PO4 при 500 — 600°С или
прокаливанием Na4P2O7 с NH4Cl, гидраты
- выпариванием р-ров с эквимолярным содержанием Na2O и Р2О5.
-гигроскопичное
водорастворимое стекло. Если расплавл. массу выдерживают при 550-560°С и
вносят затравку, то получают соль Курроля-ограниченно растворимый в воде полифосфат
с волокнистой структурой. В пром-сти трициклофосфат Na3P3O9
получают дегидратацией NaH2PO4 при 500 — 600°С или
прокаливанием Na4P2O7 с NH4Cl, гидраты
- выпариванием р-ров с эквимолярным содержанием Na2O и Р2О5.
Тетрациклофосфат Na4P4O12
может иметь конформацшо кресла или ванны. Безводная соль известна только в конфор-мации
ванны. Тетрациклофосфат Na получают при нагр. эквимолярных кол-в NaH2PO4
и Н3РО4 при 400°С с послед. медленным охлаждением
плава. Получившийся Na2H2P4O12 нейтрализуют
р-ром NaOH. Др. способ заключается в нейтрализации р-ра Н4Р4О12
щелочью до рН 7 при охлаждении.
Олигомерный трифосфат Na5P3O10,
имеющий линейное цепочечное строение, существует в двух модификациях, т-ра перехода
II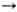 I 417°С.
Образуется при плавлении смеси соли Грэма с Na4P2O7
с послед. медленным охлаждением, дегидратацией смеси Na2HPO4
и NaH2PO4 при 350-400°С (форма II) или при 500-550°С
(I). Кол-во трифосфата составляет 70% от всех выпускаемых в пром-сти щелочных
фосфатов.
I 417°С.
Образуется при плавлении смеси соли Грэма с Na4P2O7
с послед. медленным охлаждением, дегидратацией смеси Na2HPO4
и NaH2PO4 при 350-400°С (форма II) или при 500-550°С
(I). Кол-во трифосфата составляет 70% от всех выпускаемых в пром-сти щелочных
фосфатов.
Н.ф. применяют в качестве
компонентов моющих ср-в, как умягчители воды, детергенты для очистки металлов,
ПАВ в произ-ве цементов и при бурении нефтяных скважин. Особенно хорошим моющим
эффектом обладают синтетич. моющие ср-ва с добавкой трифосфата Na (10-50%).
Для устранения жесткости воды используют дегидратированные Н.ф., образующие
комплексы с Mg, Ca, Ва и др. металлами. Н.ф. применяют при обогащении руд, в
произ-ве фосфатных стекол, красок и др. в качестве добавок или исходного сырья,
как тeкстильно-вспомогат. в-ва, в пищ. пром-сти (разрыхлители теста, для гомогенизации
и улучшения консистенции сыров, колбас, сгущенного молока), в фотографии (компоненты
проявителя), в электролитич. процессах и др.
Лит.: Корбридж Д.,
Фосфор. Основы химии, биохимии, технологии, пер. с англ., М., 1982; Comprehensive
inorganic chemistry, ed. by J.C. Bailar, A. F. Trot-man-Dickenson, v. 1, Oxf.,
1973. Л. H. Комиссарова, П. П. Мельников.


