МЫШЬЯКОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ,
содержат связь As—С. Иногда к М.с. относят все орг. соед., содержащие
As, напрю эфиры мышьяковистой (RO)3As и мышьяковой
(RO)3AsO к-т.
Известны производные As
с кординационными числами 2-6, последние
могут совпадать с валентностью или отличаться от
неё.
Наиб. многочисленная группа
М. с.-п р о и з в о д н ы е As c к
о о р д и н а ц. ч и с л о м 3. К ней относятся органоарсины RnAsH3-n
(n=1,3), тетраорганодиарсины R2As-AsR2, циклич.
и линейные полиорганоарсины (RAs)n, а также органоарсонистые
и диорганоарсинистые к-ты и их производные RnAsX3-n
(X=OH, SH, Hal, OR', NR'2 и др., n=1,2) (cм. Мышьяка
кислоты органические).
Большинство М.с. этой группы-жидкости, полиорганоарсины и орг. к-ты As-твёрдые в-ва, CH3AsH2 и CF3AsH2- газы; соед., как правило, раств. в орг. р-рителях, ограниченно в воде; в отсутствие кислорода и влаги сравнительно устойчивы (низкой устойчивостью обладают органоарсениды Mg, B, Al, Ga, In). Нек-рые тетраорганодиарсины на воздухе воспламеняются.
Конфигурация молекул соед.
трёхкоординац. As- тригон. пирамида,
напр. для (CH3)3As длина связи C-As 0,1959 нм, угол
CAsC 960 ; для CH3AsF, длины связей 0,192 нм (C-As), 0,174
нм (F—As), углы FAsF 96°, CAsF 95,5°. Значения m сравнительно
невысокие, напр. для (CH3)3As 2,869.10-30
Кл.м, для CH3AsF2 9,606.10-30
Кл.м (исключение составляет Ph2AsCN, для к-рого m 13,976.10-30Кл.м).
Спектры ИК и комбинац.
рассеяния имеют характеристич. полосы (см-1): ~200 (As—I), ~280 (As—Br),
260-420 (As—Cl), 590 b 40 (As—C), 670 b 20 (As—F), ~ 2100 (As—H).
В масс-спектрах часто наблюдаются пики мол. ионов; характерны ион-диссоциативные
процессы: разрыв связей As—С, миграция концевой части алкильного радикала (с
отщеплением нейтральной частицы, напр. С3Н6), атомов Н
или F к As.
Органоарсины и мн. производные
орг. к-т As устойчивы к нагреванию, напр. пиролиз (CH3)3As
и (CF3)3As происходит при 350-400 °С, диспропорционирование
галогенангидридов орг. к-т As-при 250-300°С.
Основные св-ва соед. трехкоординац.
As выражены слабее, чем соответствующих производных Р и N (напр., их соли с
неорг. к-тами и адцукты с к-тами Льюиса неустойчивы); однако эти производные
могут служить лигандами при комплексообразовании с солями переходных металлов.
Соед. легко присоединяют О2, S, Se, Hal2, образуя соответствующие
производные четырех- и пятикоординац. As, алки-лируются алкилгалогенидами, напр.:
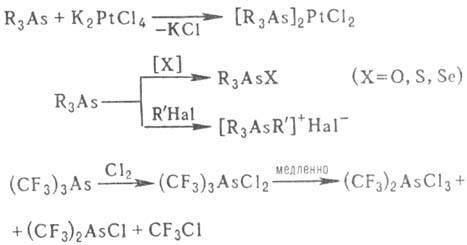
Органоарсины RAsH2
и R2AsH проявляют св-ва слабых к-т, с металлами (Li, Na, К, Са) или
их алкилъными производными образуют органоарсениды.
В соед. трехкоординац.
As связь As—X (X = Hal, OR, OAsR2, NR2) легко расщепляется
при действии нуклео-филов, связь As—Н-в электроф. и радикальных р-циях, напр.:
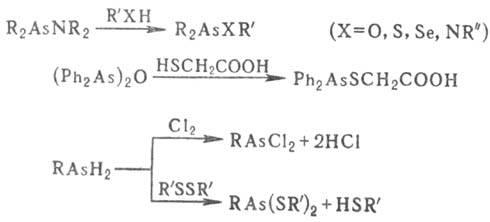
При действии нуклеофилов
на перфторалкил- и хлор-виниларсины, а также при действии О2 или
Н2 при высоких т-рах на Alk3As наблюдается разрыв связи
As—С.
Органоарсины получают алкилированием
соответствующих органоарсенидов или электроф. присоединением гидридов As к непредельным
соед., подобное присоединение галогенидов As приводит к галогенорганоарсинам
(см., напр., Люизит); R3As м.б. получены р-цией галогенидов
As с алкил- или перфторалкилгалогенидами в присут. Na, К, Hg; ArnAsHal3-n-действием
AsHal3 на арены в присут. к-т Льюиса; RnАsСl3-n-взаимод.
орг. производных Zn, Pb, Sn, Hg c AsCl3, напр.:
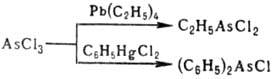
Прямое действие на As или
его сплавы алкилгалогенидов используют для синтеза органоарсинов ф-лы (RF)nAsI3_n
(RF-перфторалкил, n = 1-3, скорость и направление процесса
регулируют добавками I2 или иодидов As). Амиды к-т As получают действием
RMgHal на HalnAs(NR2)3-n (п = 1,2).
П р о и з в о д н ы е As
с к о о р д и н а ц. ч и с л о м 4. К ним относятся оксиды, тио- и селеноксиды
третичных арсинов R3As=X; алкилиденарсораны 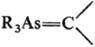 ; арсинимины R3As=NR'; арсониевые соед. [R3 AsX] +
Y- (X = R, OH, OR, SR, NH2; Y = Hal, OH, ClO4,
NO3 и др.), а также ор-ганоарсоновые и диорганоарсиновые к-ты и их
производные.
; арсинимины R3As=NR'; арсониевые соед. [R3 AsX] +
Y- (X = R, OH, OR, SR, NH2; Y = Hal, OH, ClO4,
NO3 и др.), а также ор-ганоарсоновые и диорганоарсиновые к-ты и их
производные.
Большинство соед. четырехкоординац.
As-твердые в-ва; раств. в полярных орг. р-рителях, ограниченно раств. в воде;
при рН >= 8, как правило, разлагаются. Мн. соли органоарсоновых к-т хорошо
раств. в воде; нерастворимость солей щел.-зем. металлов используют в аналит.
химии.
Конфигурация молекул соед.
четырехкоординац. As-тетраэдр, напр. для (CH3)3AsO длины
связей 0,1937 нм (С—As), 0,1631 нм (As=O), угол OAsC 112,6°; для (CH3)3As=S
0,1940 нм (С—As), 0,2059 нм (As=S), угол SAsC 113,4°; для Ph4As+
0,191 нм (С—As), угол CAsC 106-111°. Соед. с группировкой R3As=X
(X = О, S, NR') высокополярны,
напр. для Ph3As=O m 18,34.10-30 Кл.м,
для Ph3As=S m 11,67.10-30 Кл.м.
Соед. четырехкоординац.
As термически менее устойчивы, чем соед. трехкоординац. As, напр. AlknAs(O)Hal3_n
отщепляют AlkHal уже при комнатной т-ре. Большинство соед. при 100-250 °С
разлагаются или перегруппировываются с образованием, в частности, производных
трехкоординац. As, напр.:
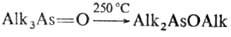
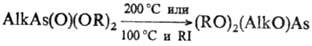
Последняя р-ция известна
под назв. "ретроарбузовская" перегруппировка (по направлению противоположна
р-ции Арбузова фосфорорг. соед.).
Производные четырехкоординац.
As проявляют основные св-ва: протонируются к-тами с образованием арсониевых
соед.; образуют аддукты с к-тами Льюиса (напр., с BF3 и S2O3)
и солями мн. металлов; алкилируются алкилгалогени-дами, напр.:
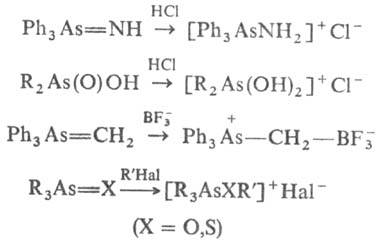
Под действием восстановителей
(H2,Ag, SO2, H3PO2, Ph3P
и др.) превращаются в соед. трехкоординац. As. При действии электроф. реагентов
М.с. типа R3As=X (X = О, S, NR, CR2) легко модифицируются,
напр.:
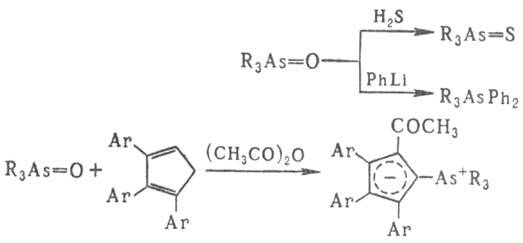
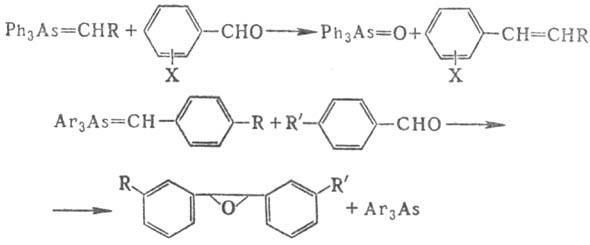
Р-ции алкилиденарсоранов
с карбонильными соед. используют для получения олефинов или оксиранов, напр.:
Для получения соед. четырехкоординац.
As используют Барта реакцию, р-цию Бешана, а также т. наз. р-цию Мейера-взаимод.
алкилгалогенидов с солями к-т As(III): RHal + Na3AsO3
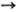 RAsO(ONa)2.
RAsO(ONa)2.
К п р о и з в о д н ы м
As с к о о р д и н а ц. ч и с л о м 5
относятся пентаорганоарсораны R5As, нек-рые органоалкоксиарсораны,
а также мн. квазиарсониевые соед. (RF)AsHal5-n
(Rp-перфторалкил) и RnAsX5-n (X = OCOR,
OOR, SR; n = = 1-3); соед. RnAsHal5-n,
видимо, склонны к образованию ионных форм.
Соед. пятикоординац. As-кристаллич.
в-ва, реже-жидкости; раств. во многих орг. р-рителях, разлагаются водой. Большинство
соед. в отсутствие влаги устойчивы, при длит. нагревании обычно разлагаются
с образованием соед. трехкоординац. As, напр.:
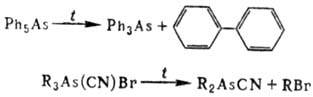
Для соед. пятикоординац.
As характерны р-ции замещения, напр.:
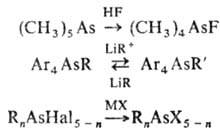
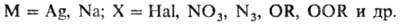
Получают их окислением
производных трех- и четырех-координац. As; пентаорганоарсораны получают р-цией
квазиарсониевых соед. с LiR.
П р о и з в о д н ы е As
с к о о р д и н а ц. ч и с л о м 2 сравнительно
мало изучены. К ним относятся арсенин (ф-ла I) и
его производные, 1,2,3-диазарсолы (II) и арсаметинцианины (III,
IV):
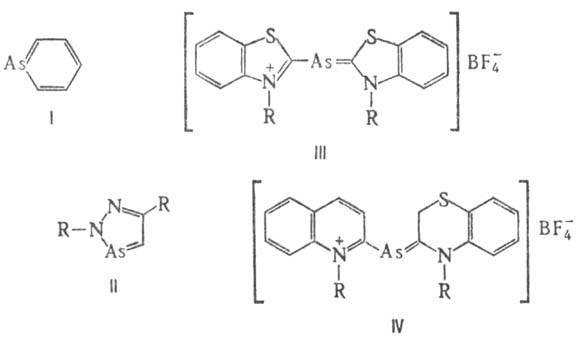
Известные соед. этой группы
-кристаллич. в-ва; раств. преим. в полярных орг. р-рителях; устойчивы при комнатной
т-ре (за исключением нек-рых производных арсенина, склонных к олигомеризации),
многие плавятся без разложения.
В арсенине атом As лежит
в плоскости кольца, длины связей 0,185 нм (С—As), 0,139-0,140 нм (С—С), угол
CAsC 97,3°.
Арсенин и его производные
получают перегруппировкой карбенов или из оловоорг. соед.:
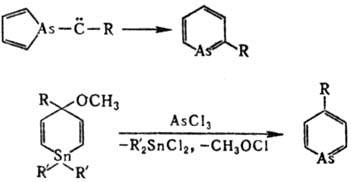
Диазарсолы получают циклоприсоединением
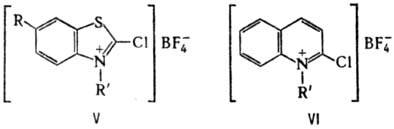
AsCl3 к гидразоналканам RNHN=C(R)CH3; арсаметинцианины
-взаимод. [(CH3)3Si]3As с тетрафторборатами
2-хлор-З-алкил(бензо-1,3-тиазолия) (V) или 1-алкилхинолиния (VI).
Известны также п р о и
з в о д н ы е As с к о о р д и н а ц. ч
и с л о м 6. К ним относятся арсенат-анионы AsX-6 (X =
OR, Аr). Соед. шестикоординац. As обладают большей устойчивостью, чем соответствующие
соед. фосфора.
М.с. применяют в качестве
лек. средств (напр., новарсе-нол, миарсенол, минарсон, осарсол), в электронной
промети (напр., R3As-для легирования эпитаксиальных слоев кремния),
в качестве реагентов в аналит. химии. Иодиды (RF)2AsI
предложено использовать в качестве активных сред фотодиссоционных оптических
квантовых генераторов.
Первые М.с. синтезированы
Л. Коде (1760). Наиб. интенсивно химия М.с. развивалась в нач. 20 в. в связи
с обнаружением у ряда М.с. противомикробного, а также раздражающего и кожно-нарывного
действия.
Лит.: Фрейдлина
Р. X., Синтетические методы в области металлооргани-ческих соединений мышьяка,
М.-Л., 1945; Doak G., Freedman L., Organo-metallic compounds of arsenic, antimony
and bismuth, N. Y., 1970; Organometallic compounds, 2 ed., v. 3-Compounds of
arsenic, antimony and bismuth, suppl. 1, ed. by M. Dub, B.-Hdlb.-N. Y., 1972;
Houben-Weyl, Methoden der organischen Chemie, Bd 13, Tl 8, Stuttg., 1978, S.
17-441; Tzschach A., Heinicke J., Arsenheterocyclen, Lpz., 1978. Г. И. Дрозд.


