МИХАЭЛЯ РЕАКЦИЯ, присоединение
соед. с реакционно-способной метиленовой или метиновой группой (доноры электронов)
к соед. с активир. двойной связью (акцепторы электронов) в присут. оснований:
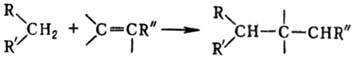
Основания - обычно алкоголяты,
гидриды, гидроксиды и карбонаты щелочных и щел.-зем. металлов, амины. Р-ритс-ли-спирты,
эфиры, 1,4-диоксан, ТГФ, бензол, ДМФА, ДМСО и др.
Донорами могут служить
малоновый и алкилмалоновый эфиры, b-дикетоны, нитро- и a,a-динитроалканы, бензилциа-ниды,
сульфоны, акцепторами-a,b-ненасыщ. альдегиды и кетоны, эфиры, амиды и нитрилы
a,b-ненасыщ. к-т, нитро-соединения и др., принадлежащие к алифатич., алициклич.
и жирно-ароматич. ряду.
Р-ция протекает по механизму
сопряженного присоединения и начинается с атаки карбанионом (генерируется под
действием оснований) связи С=С по атому С с наим. электронной плотностью; возникающий
при этом новый карбанион стабилизируется присоединением протона из среды:
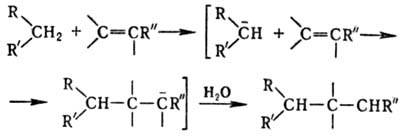
Если один из заместителей
в генерир. карбанионе способен легко уходить в виде аниона, то стабилизация
нового аниона может осуществляться с элиминированием этого заместителя (чаще
всего галогена) с послед. образованием цикло-пропанового кольца, напр.:
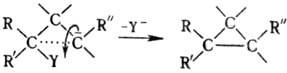
При избытке основания р-ция
может происходить аномально:
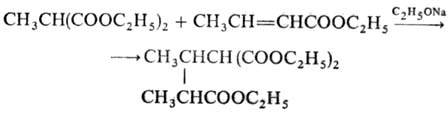
Имеются примеры внутримол.
р-ции Михаэля с образованием циклич. продуктов:
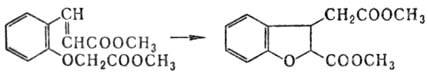
Модификация М.р.-в случае
чувствительных к основаниям a,b-ненасыщ. альдегидов р-цию проводят в условиях
межфазного катализа.
М. р.-одна из важнейших
р-ций орг. синтеза; применяется в лаб. и пром. практике для получения полифуикцион.
соединений. Р-ция открыта А. Михаэлем в 1887.
Лит.: Бергман Э. Д., Гинзбург В., Паппо Р., в сб.: Органические реак-ции, т. 10, М., 1963, с. 181-526; Вацуро К. В., Мищенко Г. Л., Именные реакции в органической химии, М., 1976; Марч Дж., Органическая химия, пер. с англ., т. 3, М., 1987, с. 140-43, 199-200. Л. А. Яновская.


