МЕТИЛСEРНАЯ КИСЛОТА
(метиловый эфир серной к-ты, метилсульфат) CH3OSO2OH,
мол.м. 112,1; маслянистая гигроскопичная жидкость, не смачивает стекло; т.пл.
— 27 °С, d204 1,352. Раств. в диэтиловом эфире,
моногидрат М. к. в эфире не раств.; плохо раств. в воде. Гидролизуется водой
с образованием H2SO4 и СН3ОН.
С метанолом при 110 °С
М. к. дает (CH3O)2SO2. При нагр. М. к. и при
попытке ее перегонки происходит диспропорцио-нирование:
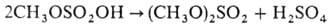
При растворении диметилсульфата
в 100%-ной H2SO4 при комнатной т-ре образуется М.к. Соли
М.к. получают прибавлением гидроксидов или карбонатов Са или Ва к реакц. смесям,
содержащим М.к. Эти соли М.к. раств. в воде, на чем и основано их выделение.
Обменными р-циями получают нужные соли, напр.:
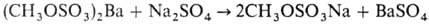
М.к. получают нагреванием
эквимолярных кол-в СН3ОН и H2SO4 при т-ре =<
100°С. М.к. образуется при обработке СН3ОН триоксидом S ниже
0°С. Удобный метод получения М.к.-взаимод. СН3ОН с SO2Cl(OH)
при низких т-рах. Р-цию проводят без р-рителя или в орг. р-рителе-диэтиловом
эфире, ди(b-хлорэтиловом) эфире, этилацетате, ССl4.
М.к. и ее Na-соль-алкилирующий
агент в орг. синтезе; интермедиат в произ-ве диметилсульфата, р-ритель.
М.к. токсична, раздражает
кожу. Na-соль М.к. менее токсична, ЛД50 5000 мг/кг (крысы).
Лит.: Сьютер Ч.,
Химия органических соединений серы, пер. с англ., ч. 1, М., 1950, с. 26-29;
Джильберт Э. Е., Сульфирование органических соединений, пер. с англ., М., 1969,
с. 33, 304. А. А. Дудинов.


