МЕЛАНИНЫ (от греч.
melas, род. падеж melanos - черный), обычно черные или темно-коричневые пигменты
животных, растений и микроорганизмов. У высших животных и человека М.-осн. группа
пигментов. У животных М. придают окраску шерсти, у птиц - оперению, у человека
ответственны за цвет глаз, волос, окраску кожи.
М.-аморфные высокомол.
в-ва. Не раств. в воде, минер. к-тах, орг. р-рителях; хорошо раств. в щелочах,
а затем выпадают в
осадок при подкислении р-ров, что используется для их выделения. Хим. разрушение
М. происходит при нагр. выше 200 °С, сплавлении со щелочью, окислении конц.
р-рами КМnО4 или Н2О2.
По предшественникам М.
в организме их разделяют на эумеланины, феомеланины и алломеланины. Эумеланины
(черные) и феомеланины (желтые, красные и коричневые) распространены у животных,
алломеланины (черные)-и в растениях, грибах, бактериях. Предшественник эумелани-нов-тирозин;
из него в организме получаются пигменты, содержащие С, Н, N и О. Предшественники
феомелани-нов-тирозин и цистеин; в организме превращ. в серосодер-жащие пигменты.
Предшественники алломеланинов - ди-фенолы (пирокатехин и др.); из них образуются
М., не содержащие азота. В организмах М. находятся в комплексе с белками.
Мн. св-ва и биол. ф-ции
М. определяются их способностью функционировать в организме в виде системы фенол-семихинон-хинон.-
Механизм образования М. окончательно не выяснен. Полагают, что первые стадии
биосинтеза М. являются ферментативными и катализируются о-дифенол: кислород
оксидоредуктазами (напр., тирозина-зой, полифенолоксидазой и др.), послед. стадии
протекают спонтанно с участием своб. радикалов. Предполагаемый механизм синтеза
эумеланинов в организме под влиянием тирозиназы состоит в окислении тирозина
(ф-ла I) до 3,4-дигидроксифенилаланина (ДОФА; ф-ла II) и ДОФА-хи-нона (III)
с послед. циклизацией, декарбоксилированием, окислением и полимеризацией по
схеме:
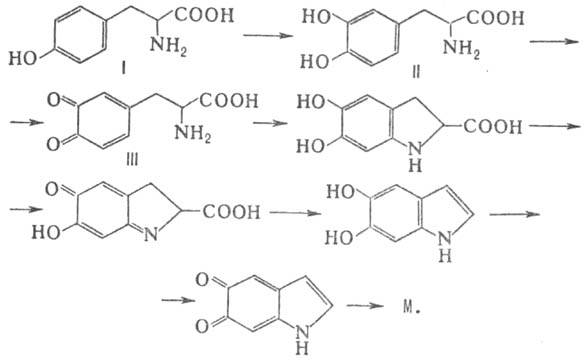
М. могут быть получены
автоокислением ДОФА, 5,6-ди-гидроксииндола и др. дифенолов.
Разнообразие исходных мономеров
и высокая активность промежут. продуктов делают хим. состав М. разнообразным,
а структуру полимера-нерегулярной.
М. характеризуются наличием
в их структуре неспаренных электронов и обладают св-вами стабильных своб. радикалов.
Эта особенность М. важна для выполнения ими защитные ф-ций в организме. М. не
только поглощают разл. излучения, но и нейтрализуют и обезвреживают опасные
для клеток своб. радикалы, образующиеся при действии ионизирующего излучения
и нек-рых хим. в-в на живые организмы.
М. могут существовать в
неск. окислит.-восстановит. состояниях. Они окисляют Na2S2O4,
восстановленную форму никотинамидадениндинуклеотида (НАДН) и др., восстанавливают
феррицианид, цитохром с и др. Обладают электрон-транспортными св-вами.
Р-ция восстановления ионов Ag до металла с помощью М.-гистохим. тест для их
идентификации.
У животных и человека процесс
образования М. в организме происходит в спец. клетках - меланоцитах и регулируется
гормональной системой, гл. обр. с помощью гормонов гипофиза ( a- и b-меланоцитстимулирующих
гормонов). Нек-рые физ. факторы (солнечные, УФ и рентгеновские лучи) и хим.
реагенты стимулируют образование М. в организме.
Повыш. содержание М. наблюдается также в нек-рых злокачеств. опухолях-меланомах.
Лит.: Бриттон Г.,
Биохимия природных пигментов, пер. с англ., М., 1986; Nicolaus R. A., Melanins,
P., 1968; Blois M.S., "Photochemical and hotobio-logical Reviews",
1978, v. 3, p. 115-34. T.A. Телегина.


