МЕЗОМЕРИЯ (от греч.
mesos- средний, промежуточный и meros - часть), теория электронного строения
соед., согласно к-рой истинное распределение электронной плотности в молекуле
(ионе) является промежуточным между распределениями, представленными неск. классич.
ф-лами. Так, особенности хим. св-в и структурных характеристик форма-мида, напр.
повышенная по сравнению с аминами кислотность группы NH2, отсутствие
ряда характерных для карбонильной группы р-ций, удлинение связи С=О и укорочение
связи С—N, не передаются в полной мере ф-лой I. Ионная структура II отражает
указанные тенденции, но сильно переоценивает истинную поляризацию связей. Действительное
электронное распределение является промежуточным между I и II с преобладанием
первой структуры (ф-ла III).
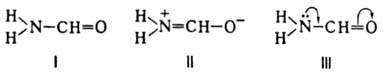
Характерные св-ва мезомерных
систем - повыш. поляризуемость, экзальтация молярной рефракции, выравненность
длин связей, увеличение дипольного момента по сравнению с аддитивной величиной,
сильно выраженная зависимость электронного спектра поглощения от полярности
р-рителя. В методах мол. орбиталей основой представлений о М. служит образование
делокализованных мол. орбиталей сопряженной p-системы.
По своему содержанию М.
практически совпадает с резонанса теорией, однако в отличие от последней
оперирует для описания св-в молекул не наборами резонансных струк-тур, а разработанными
правилами электронных смещений (см. Мезомерный эффект). Представления
о М., развитые в 30-х гг. 20 в. гл. обр. в работах англ. школы (Р. Робинсон,
К. Инголд и др.),
продолжают занимать важное место в системе электронных теорий орг. химии.
Лит.: Быков Г. В.,
История электронных теорий органической химии, М., 1963; Ингольд К. К., Теоретические
основы органической химии, пер. с англ., 2 изд., М., 1973. В. И. Минкин.


