МАЛЕИНОВЫЙ АНГИДРИД (ангидрид циc-этилен-1,2-дикарбоновой к-ты; 2,5-фурандион), мол. м. 98,06; бесцв. кристаллы с ромбич. решеткой (а = 0,7180 нм, b = 1,1231 нм, с = 0,539 нм, пространств. группа P212121); т. пл. 52,85 °С, т. кип. 202 °С; d2020 1,48, d7070 1,3; nD25 1,4429 (a-модификация), 1,4781 (b), 1,6384 (g); h 1,61 мПа.с (60 °С), 1,07 мПа.с (90 °С), 0,6 мПа.с (150°С); давление пара 0,13 кПа (44 °С), 1,3 кПа (78 °С), 8,0 кПа (122 °С), 100 кПа (202 °С); Ср (для твердого) 1,21 кДж/(моль.°С),
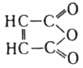
Сp (для жидкости) 1,67 кДж/(моль.°С); DH0обр -470,41 кДж/моль, DH0сгор -1392,29 кДж/моль, DH0исп 54,81 кДж/моль, DH0пл 13,65 кДж/моль, DH0гидр — 34,9 кДж/моль. Раств. в воде с образованием малеиновой к-ты (44,1% при 25 °С); р-римость (г в 100 г р-рителя при 25 °С): в ацетоне - 227, бензоле - 50, толуоле - 23,4, о-ксилоле - 19,4, керосине (т-ра выкипания 190-210°С) - 0,25, хлороформе - 52,5, ССl4 - 0,6, этилацетате - 112, диоксане - 182. М. а. очень реакционноспособен. При взаимод. с одноатомными спиртами образует моно- и диэфиры, с гликолями - ненасыщ. полиэфиры. Вступает в р-цию Дильса -Альдера с сопряженными диенами, образуя циклич. аддукты. При присоединении по двойной связи Н2О или Н2 превращ. в ангидриды соотв. яблочной или янтарной к-ты, при присоединении Н2О2 - в винную к-ту, NH3 или алифатич. аминов - в аспарагиновую к-ту или ее N-алкилзамещенные. С алкилбензолами реагирует с образованием ангидридов арилалкилянтарных к-т, напр.:
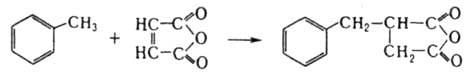
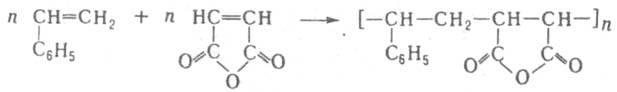
Аналогично М. а. взаимод. с несопряженными ненасыщ. соед., содержащими метильные или метиленовые группы при кратной связи. Сополимеризация М. а. с виниловыми соед. и олефинами приводит к насыщ. линейным полимерам:
М. а. легко гидролизуется до малеиновой к-ты, к-рая в присут. тиомочевины или др. катализаторов легко изомери-зуется в фумаровую к-ту. Пром. способы получения М. а.: 1) парофазное каталитич. окисление бензола воздухом над стационарным оксидным ванадиймолибденовым катализатором (ок. 50% мирового произ-ва в 1987); 2) парофазное окисление н-бутана над стационарным или псевдоожиженным оксидным ванадийфосфорным катализатором (ок. 40% мирового произ-ва). Этот метод экономически предпочтительней бензольного. В обоих способах М. а. из реакц. газов выделяют в жидком и твердом состоянии и в виде малеиновой к-ты, к-рую подвергают дегидратации, осуществляемой термически в аппаратах пленочного типа или посредством азеотропной перегонки с о-ксилолом. На нек-рых пром. установках применяется (с 1986) непрерывный способ улавливания М. а. из реакц. газов орг. р-рителями. Сырой продукт очищают термохим. обработкой и ректификацией. Выход 72-75 мол.% из бензола и 52-55 мол.% из н-бутана. Расход бензола или н-бутана 1150-1200 кг на 1000 кг М. а. Товарный М. а. содержит 99,7-99,9% основного в-ва. Небольшие кол-ва М. а. получают каталитич. парофазным окислением углеводородов фракции С4, а также выделяют из побочных продуктов произ-ва фталевого ангидрида из о-ксилола. Ок. 75-80% мирового произ-ва М. а. применяют для получения ненасыщ. полиэфирных смол (см. Полиалкиленгликольмалеинаты и полиалкиленгликольфумараты). Его используют также для синтеза фумаровой и яблочной к-т, гидразида малеиновой к-ты (регулятор роста растений), дефолиантов (напр., эндоталя), фунгицидов (кантона и др.), инсектицидов (карбофоса), как модификатор алкидных смол, добавку к смазочным маслам для изменения внутр. трения, сырье в произ-ве тетрагидрофталевого ангидрида, ТГФ и g-бутиролактона. Т. всп. 102-110°С, т. самовоспл. 447°С, ниж. КПВ 1,4% (для пыли 50 г/м3), верхний - 7,1%. М. а. раздражает слизистые оболочки глаз и верх. дыхат. путей (сопровождается бронхитами, желудочно-кишечными расстройствами); ПДК 1,0 мг/м3. Объем мирового произ-ва ок. 500 тыс. т/год (1986). Лит.: Молдавский Б. Л., Кернос Ю. Д., Малеиновый ангидрид и малеиновая кислота, Л., 1976; Kirk-Othmer encyclopedia, 3 ed., v. 14, N. Y., 1981, p. 770-93; Trivedi В. С., Culbertson В. М., Maleic anhydride, N. Y.-L., 1982. А. Г. Любарский.

Сp (для жидкости) 1,67 кДж/(моль.°С); DH0обр -470,41 кДж/моль, DH0сгор -1392,29 кДж/моль, DH0исп 54,81 кДж/моль, DH0пл 13,65 кДж/моль, DH0гидр — 34,9 кДж/моль. Раств. в воде с образованием малеиновой к-ты (44,1% при 25 °С); р-римость (г в 100 г р-рителя при 25 °С): в ацетоне - 227, бензоле - 50, толуоле - 23,4, о-ксилоле - 19,4, керосине (т-ра выкипания 190-210°С) - 0,25, хлороформе - 52,5, ССl4 - 0,6, этилацетате - 112, диоксане - 182. М. а. очень реакционноспособен. При взаимод. с одноатомными спиртами образует моно- и диэфиры, с гликолями - ненасыщ. полиэфиры. Вступает в р-цию Дильса -Альдера с сопряженными диенами, образуя циклич. аддукты. При присоединении по двойной связи Н2О или Н2 превращ. в ангидриды соотв. яблочной или янтарной к-ты, при присоединении Н2О2 - в винную к-ту, NH3 или алифатич. аминов - в аспарагиновую к-ту или ее N-алкилзамещенные. С алкилбензолами реагирует с образованием ангидридов арилалкилянтарных к-т, напр.:

Аналогично М. а. взаимод. с несопряженными ненасыщ. соед., содержащими метильные или метиленовые группы при кратной связи. Сополимеризация М. а. с виниловыми соед. и олефинами приводит к насыщ. линейным полимерам:

М. а. легко гидролизуется до малеиновой к-ты, к-рая в присут. тиомочевины или др. катализаторов легко изомери-зуется в фумаровую к-ту. Пром. способы получения М. а.: 1) парофазное каталитич. окисление бензола воздухом над стационарным оксидным ванадиймолибденовым катализатором (ок. 50% мирового произ-ва в 1987); 2) парофазное окисление н-бутана над стационарным или псевдоожиженным оксидным ванадийфосфорным катализатором (ок. 40% мирового произ-ва). Этот метод экономически предпочтительней бензольного. В обоих способах М. а. из реакц. газов выделяют в жидком и твердом состоянии и в виде малеиновой к-ты, к-рую подвергают дегидратации, осуществляемой термически в аппаратах пленочного типа или посредством азеотропной перегонки с о-ксилолом. На нек-рых пром. установках применяется (с 1986) непрерывный способ улавливания М. а. из реакц. газов орг. р-рителями. Сырой продукт очищают термохим. обработкой и ректификацией. Выход 72-75 мол.% из бензола и 52-55 мол.% из н-бутана. Расход бензола или н-бутана 1150-1200 кг на 1000 кг М. а. Товарный М. а. содержит 99,7-99,9% основного в-ва. Небольшие кол-ва М. а. получают каталитич. парофазным окислением углеводородов фракции С4, а также выделяют из побочных продуктов произ-ва фталевого ангидрида из о-ксилола. Ок. 75-80% мирового произ-ва М. а. применяют для получения ненасыщ. полиэфирных смол (см. Полиалкиленгликольмалеинаты и полиалкиленгликольфумараты). Его используют также для синтеза фумаровой и яблочной к-т, гидразида малеиновой к-ты (регулятор роста растений), дефолиантов (напр., эндоталя), фунгицидов (кантона и др.), инсектицидов (карбофоса), как модификатор алкидных смол, добавку к смазочным маслам для изменения внутр. трения, сырье в произ-ве тетрагидрофталевого ангидрида, ТГФ и g-бутиролактона. Т. всп. 102-110°С, т. самовоспл. 447°С, ниж. КПВ 1,4% (для пыли 50 г/м3), верхний - 7,1%. М. а. раздражает слизистые оболочки глаз и верх. дыхат. путей (сопровождается бронхитами, желудочно-кишечными расстройствами); ПДК 1,0 мг/м3. Объем мирового произ-ва ок. 500 тыс. т/год (1986). Лит.: Молдавский Б. Л., Кернос Ю. Д., Малеиновый ангидрид и малеиновая кислота, Л., 1976; Kirk-Othmer encyclopedia, 3 ed., v. 14, N. Y., 1981, p. 770-93; Trivedi В. С., Culbertson В. М., Maleic anhydride, N. Y.-L., 1982. А. Г. Любарский.


