ЛИПОПРОТЕИНЫ (липопротеиды), комплексы, состоящие из белков (аполипопротеинов; сокращенно - апо-Л.) и липидов, связь между к-рыми осуществляется посредством гидрофобных и электростатич. взаимодействий. Л. подразделяют на свободные, или р-римые в воде (Л. плазмы крови, молока, желтка яиц и др.), и нерастворимые, т. наз. структурные (Л. мембран клетки, миелиновой оболочки нервных волокон, хлоропластов растений). Нековалентная связь в Л. между белками и липидами имеет важное биол. значение. Она обусловливает возможность своб. обмена липидов и модуляцию св-в Л. в организме.
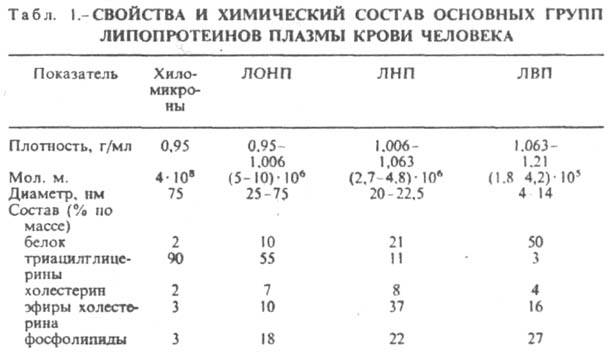
Среди своб. Л. (они занимают ключевое положение в транспорте и метаболизме липидов) наиб. изучены Л. плазмы крови, к-рые классифицируют по их плотности. Чем выше содержание в них липидов, тем ниже плотность Л. (табл. 1). Различают Л. очень низкой плотности (ЛОНП), низкой плотности (ЛНП), высокой плотности (ЛВП) и хиломикроны. Каждая группа Л. очень неоднородна по размерам частиц (самые крупные - хиломикроны) и содержанию в ней апо-Л. Все группы Л. плазмы содержат полярные и неполярные липиды в разных соотношениях.
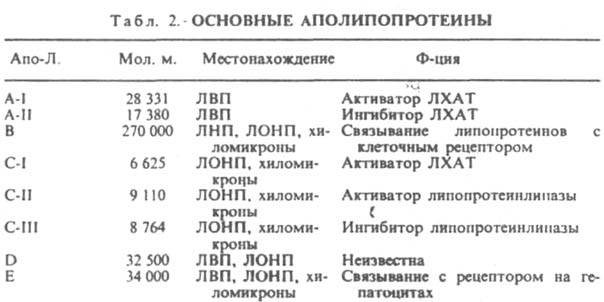
Во всех Л. плазмы имеется ядро, состоящее из эфиров холестерина и триацилглицеринов, к-рое покрыто мономолекулярным слоем холестерина, фосфолипидов и гидрофильной частью молекул апо-Л. Предполагают, что домены апо-Л. имеют две грани, одна из к-рых гидрофобная, а другая - гидрофильная. Первая грань контактирует с жирно-кислотными цепями фосфолипидов, вторая - ассоциирована с полярной группой фосфолипидов на пов-сти раздела липид - вода. Хиломикроны и ЛОНП образуются соотв. в кишечнике и печени, ЛВП - в кишечнике, печени, а также в крови из др. Л. Идентифицированы нек-рые апо-Л. (см. табл. 2), каждый из к-рых обладает определенными св-вами, связанными с превращением Л. в организме. Хиломикроны и ЛОНП, попадая в кровоток, захватывают апо-Л. С-II из ЛВП и активируют мембраносвязанную липопротеинлипазу, катализирующую расщепление в них триацилглицеринов. Во время катаболизма ацилглицеринов апо-Л. С-II возвращается к ЛВП, а хиломикроны и ЛОНП превращаются в ЛНП - осн. источник клеточного холестерина. ЛНП поступают во все клетки организма, взаимодействуя со спец. рецептором мембраны, активность к-рого понижается с увеличением концентрации внутриклеточного холестерина. ЛВП, наоборот, способны выводить холестерин из клеток. Предполагают, что высокое содержание в плазме ЛНП при низком содержании ЛВП - важный фактор возникновения атеросклероза (заболевания, обусловленного образованием обильных отложений холестерина и его эфиров на внутр. пов-сти кровеносных сосудов). Апо-Л. A-I - основной белок ЛВП. Он активирует сывороточный фермент лецитин : холестерол ацилтрансферазу (ЛХАТ), к-рый катализирует одновременно расщепление фосфолипидов и ацилирование холестерина, переводя его в биологически неактивную форму.
Выделяют Л. плазмы крови обычно методом флотации, используя водные р-ры бромидов Na или К разл. плотности. К структурным Л. относятся комплексы липидзависимых ферментов (напр., аденилатциклаза), рецспторные комплексы (напр., рецептор ацетилхолина), к-рые входят в состав мембран биологических. Их строение и биол. св-ва очень разнообразны. Лит.: Климов А. Н., в сб.: Биохимия липидов и их роль в обмене веществ, М., 1981, с. 45-75; Structural and functrond aspects of lipoproteins in living systems, ed. by E. Tria, A. M. Scanu, L. N. Y., 1969. Н. В. Проказова.

Во всех Л. плазмы имеется ядро, состоящее из эфиров холестерина и триацилглицеринов, к-рое покрыто мономолекулярным слоем холестерина, фосфолипидов и гидрофильной частью молекул апо-Л. Предполагают, что домены апо-Л. имеют две грани, одна из к-рых гидрофобная, а другая - гидрофильная. Первая грань контактирует с жирно-кислотными цепями фосфолипидов, вторая - ассоциирована с полярной группой фосфолипидов на пов-сти раздела липид - вода. Хиломикроны и ЛОНП образуются соотв. в кишечнике и печени, ЛВП - в кишечнике, печени, а также в крови из др. Л. Идентифицированы нек-рые апо-Л. (см. табл. 2), каждый из к-рых обладает определенными св-вами, связанными с превращением Л. в организме. Хиломикроны и ЛОНП, попадая в кровоток, захватывают апо-Л. С-II из ЛВП и активируют мембраносвязанную липопротеинлипазу, катализирующую расщепление в них триацилглицеринов. Во время катаболизма ацилглицеринов апо-Л. С-II возвращается к ЛВП, а хиломикроны и ЛОНП превращаются в ЛНП - осн. источник клеточного холестерина. ЛНП поступают во все клетки организма, взаимодействуя со спец. рецептором мембраны, активность к-рого понижается с увеличением концентрации внутриклеточного холестерина. ЛВП, наоборот, способны выводить холестерин из клеток. Предполагают, что высокое содержание в плазме ЛНП при низком содержании ЛВП - важный фактор возникновения атеросклероза (заболевания, обусловленного образованием обильных отложений холестерина и его эфиров на внутр. пов-сти кровеносных сосудов). Апо-Л. A-I - основной белок ЛВП. Он активирует сывороточный фермент лецитин : холестерол ацилтрансферазу (ЛХАТ), к-рый катализирует одновременно расщепление фосфолипидов и ацилирование холестерина, переводя его в биологически неактивную форму.

Выделяют Л. плазмы крови обычно методом флотации, используя водные р-ры бромидов Na или К разл. плотности. К структурным Л. относятся комплексы липидзависимых ферментов (напр., аденилатциклаза), рецспторные комплексы (напр., рецептор ацетилхолина), к-рые входят в состав мембран биологических. Их строение и биол. св-ва очень разнообразны. Лит.: Климов А. Н., в сб.: Биохимия липидов и их роль в обмене веществ, М., 1981, с. 45-75; Structural and functrond aspects of lipoproteins in living systems, ed. by E. Tria, A. M. Scanu, L. N. Y., 1969. Н. В. Проказова.


