ЛИПОЕВАЯ КИСЛОТА [3-(4-карбоксибутил)-1,2-дитиолан, тиоктовая к-та], мол. м. 206,192; кофермент, участвующий в каталитич. р-циях переноса атомов Н и ацильных групп; незаменимый фактор роста (витамин) для молочнокислых бактерий, к-рые его не синтезируют.
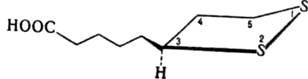
С ферментами связан пептидной связью, образованной его карбоксильной группой и e-аминогруппой остатка лизина в молекуле апофермента. В природе присутствует в тканях животных, растений и в микроорганизмах в виде физиологически активного правовращающего изомера - лимонно-желтое кристаллич. в-во; т. пл. 46-47 °С, [a]D25 + 96,7° (концентрация 1,88 г в 100 мл бензола); не раств. в воде, раств. в этаноле, хорошо раств. в хлороформе, эфире, циклогексане; lмакс335 нм. Под действием р-ров щелочей полимеризуется, образуя линейные полимеры, в к-рых остатки Л. к. связаны дисульфидными мостиками. Под влиянием восстановителей (напр., NaBH4) легко превращ. в 6,8-дитиооктановую (6,8-дигидролипоевую) к-ту HS(CH2)2CH(SHXCH2)4COOH. Л. к. наряду с тиаминдифосфатом (ТДФ, коферментная форма тиамина) - один из необходимых коферментов пируватдегидрогеназного ферментного комплекса, осуществляющего в живых клетках окислит. декарбоксилирование a-оксокислот, напр. пировиноградной и a-оксоглутаровой. Эти превращ. по-разному протекают у микроорганизмов и у животных. Так, в клетках дрожжей при этом образуется ацетальдегид и уксусная к-та; в клетках животных пировиноградная к-та (образуется в организме в результате гидролитич. расщепления глюкозы) превращ. в ацетилкофермент А [КоАSС(О)СН3]. Предполагают, что в последнем случае механизм р-ции включает взаимод. пировиноградной к-ты (ф-ла I) с тиазольным циклом ТДФ (вся молекула кофермента не показана) и перенос т. наз. ацетальдегидного эквивалента с пировиноградной к-ты восстановленную форму Л. к.:
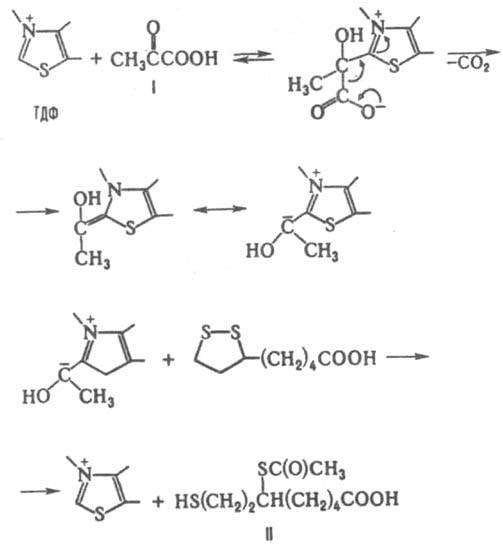
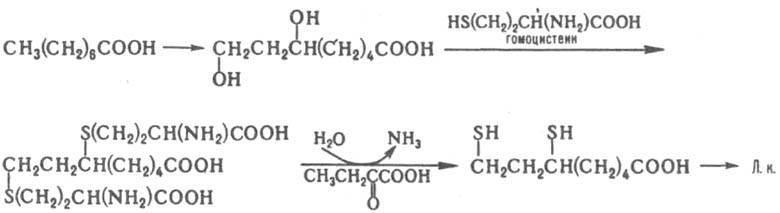
В результате образуется ацетилдигидролипоевая к-та (II), ацетильная группа к-рой переносится затем на кофермент А (КоASH) с образованием KoASC(O)CH3 и дигидролипоевой к-ты. Последняя под действием НАД-зависимого фермента окисляется до Л. к. КоASC(O)CH3 - важный метаболит в цикле трикарбоновых к-т. В организме Л. к. ускоряет окисление глюкозы, ее фосфорилирование, гликолиз и увеличивает накопление гликогена в печени. Л. к. обладает также детоксифицирующим действием при отравлениях фосфорорг. соед., тяжелыми металлами и их солями, цианидами, этанолом и др. Биосинтез Л. к. у животных и человека осуществляется гл. обр. в кишечной флоре по схеме:
D,L-Л.к. (т. пл. 59-60 °С) синтезируют конденсацией хлорангидрида моноэфира адипиновой к-ты с этиленом, восстановлением образующегося эфира 6-оксо-8-хлороктановой к-ты до 6-гидрокси-8-хлороктаноата, хлорированием его до 6,8-дихлороктаноата и тионированием последнего с помощью Na2S2. D,L-Л. к. и ее амид применяют как лек. ср-во при коронарном атеросклерозе, заболеваниях печени и диабетич. полиневрите. Потребность человека 1-2 мг/сут, что обычно обеспечивается синтезом Л. к. в организме. Лит.: Хайлова Л. С., Юркевич А. М., Северин С. Е., в кн.: Коферменты, под ред. В. А. Яковлева, М., 1973, с. 256-90; Bullock M. W. [а.о.], "J. Amer. Chem. Soc", 1952, v. 74, p. 3455. А. М. Юркевич.

С ферментами связан пептидной связью, образованной его карбоксильной группой и e-аминогруппой остатка лизина в молекуле апофермента. В природе присутствует в тканях животных, растений и в микроорганизмах в виде физиологически активного правовращающего изомера - лимонно-желтое кристаллич. в-во; т. пл. 46-47 °С, [a]D25 + 96,7° (концентрация 1,88 г в 100 мл бензола); не раств. в воде, раств. в этаноле, хорошо раств. в хлороформе, эфире, циклогексане; lмакс335 нм. Под действием р-ров щелочей полимеризуется, образуя линейные полимеры, в к-рых остатки Л. к. связаны дисульфидными мостиками. Под влиянием восстановителей (напр., NaBH4) легко превращ. в 6,8-дитиооктановую (6,8-дигидролипоевую) к-ту HS(CH2)2CH(SHXCH2)4COOH. Л. к. наряду с тиаминдифосфатом (ТДФ, коферментная форма тиамина) - один из необходимых коферментов пируватдегидрогеназного ферментного комплекса, осуществляющего в живых клетках окислит. декарбоксилирование a-оксокислот, напр. пировиноградной и a-оксоглутаровой. Эти превращ. по-разному протекают у микроорганизмов и у животных. Так, в клетках дрожжей при этом образуется ацетальдегид и уксусная к-та; в клетках животных пировиноградная к-та (образуется в организме в результате гидролитич. расщепления глюкозы) превращ. в ацетилкофермент А [КоАSС(О)СН3]. Предполагают, что в последнем случае механизм р-ции включает взаимод. пировиноградной к-ты (ф-ла I) с тиазольным циклом ТДФ (вся молекула кофермента не показана) и перенос т. наз. ацетальдегидного эквивалента с пировиноградной к-ты восстановленную форму Л. к.:

В результате образуется ацетилдигидролипоевая к-та (II), ацетильная группа к-рой переносится затем на кофермент А (КоASH) с образованием KoASC(O)CH3 и дигидролипоевой к-ты. Последняя под действием НАД-зависимого фермента окисляется до Л. к. КоASC(O)CH3 - важный метаболит в цикле трикарбоновых к-т. В организме Л. к. ускоряет окисление глюкозы, ее фосфорилирование, гликолиз и увеличивает накопление гликогена в печени. Л. к. обладает также детоксифицирующим действием при отравлениях фосфорорг. соед., тяжелыми металлами и их солями, цианидами, этанолом и др. Биосинтез Л. к. у животных и человека осуществляется гл. обр. в кишечной флоре по схеме:

D,L-Л.к. (т. пл. 59-60 °С) синтезируют конденсацией хлорангидрида моноэфира адипиновой к-ты с этиленом, восстановлением образующегося эфира 6-оксо-8-хлороктановой к-ты до 6-гидрокси-8-хлороктаноата, хлорированием его до 6,8-дихлороктаноата и тионированием последнего с помощью Na2S2. D,L-Л. к. и ее амид применяют как лек. ср-во при коронарном атеросклерозе, заболеваниях печени и диабетич. полиневрите. Потребность человека 1-2 мг/сут, что обычно обеспечивается синтезом Л. к. в организме. Лит.: Хайлова Л. С., Юркевич А. М., Северин С. Е., в кн.: Коферменты, под ред. В. А. Яковлева, М., 1973, с. 256-90; Bullock M. W. [а.о.], "J. Amer. Chem. Soc", 1952, v. 74, p. 3455. А. М. Юркевич.


