КРЁНКЕ РЕАКЦИЯ, получение альдегидов взаимод. четвертичных пиридиниевых солей с 4-нитрозо-N, N-диметиланилином и послед. гидролизом образующихся нитронов:
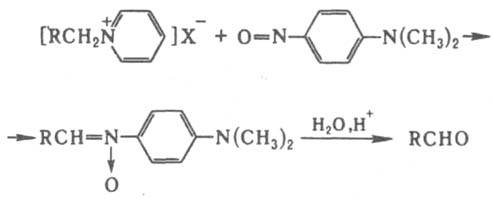
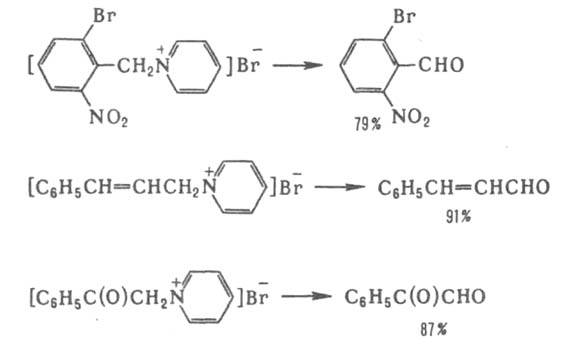
Четвертичную соль обрабатывают нитрозосоединением в водно-пиридиновом р-ре в присут. стехиометрич. кол-ва NaOH или др. основания. Нитрон, к-рый обычно выпадает в осадок, гидролизуют разб. НСl или H2SO4. Альдегид экстрагируют эфиром. Метод применяют для получения ароматич., гетероциклич., a, b-ненасыщенных альдегидов, а также a-кетоальдегидов, напр.:
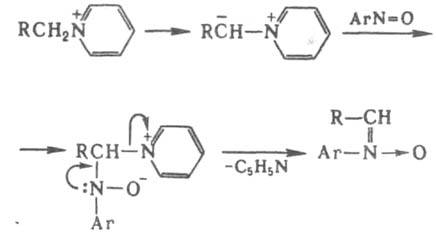
Исходные пиридиниевые соли получают алкилированием пиридина, а также иодированием метилкетонов или метил-замещенных гетероциклич. соед. в присут. пиридина (Ортолевы - Кинга реакция). Механизм получения нитрона предполагает промежут. образование пиридиний-илида и бетаина:
К. р. позволяет в мягких условиях получать альдегиды, малодоступные при использовании др. путей синтеза. Р-ция открыта Ф. Крёнке в 1936. Лит.: Общая органическая химия, пер. с англ., т. 2, М., 1982, с. 699-700; там же, т. 3, 1982, с. 615-16. Е. М. Рохлин.

Четвертичную соль обрабатывают нитрозосоединением в водно-пиридиновом р-ре в присут. стехиометрич. кол-ва NaOH или др. основания. Нитрон, к-рый обычно выпадает в осадок, гидролизуют разб. НСl или H2SO4. Альдегид экстрагируют эфиром. Метод применяют для получения ароматич., гетероциклич., a, b-ненасыщенных альдегидов, а также a-кетоальдегидов, напр.:

Исходные пиридиниевые соли получают алкилированием пиридина, а также иодированием метилкетонов или метил-замещенных гетероциклич. соед. в присут. пиридина (Ортолевы - Кинга реакция). Механизм получения нитрона предполагает промежут. образование пиридиний-илида и бетаина:

К. р. позволяет в мягких условиях получать альдегиды, малодоступные при использовании др. путей синтеза. Р-ция открыта Ф. Крёнке в 1936. Лит.: Общая органическая химия, пер. с англ., т. 2, М., 1982, с. 699-700; там же, т. 3, 1982, с. 615-16. Е. М. Рохлин.


