КOУПА ПЕРЕГРУППИРОВКА, изомеризация 1,5-ненасыщенных орг. соед., сопровождающаяся миграцией аллильной группы с одноврем. сдвигом двойной связи, напр.:
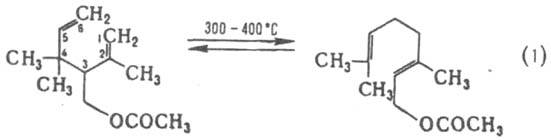
К. п. проводят: при нагр. в вакууме или инертной атмосфере при 150-450 °С; в присут. комплексов Pd(II) или Ni(0) при 0-20 °С; под действием КН в ТГФ в присут. краун-эфиров при 0-65 °С; при термолизе под давлением св. 100 МПа.
Hаиб. изучены обратимая изомеризация 1,5-диолефинов (р-ция 1) и необратимое превращ. 1,5-енин-З-олов (р-ция 2) в
ненасыщ. карбонильные соед. (т. наз. гидроокси-перегруппировка Коупа):
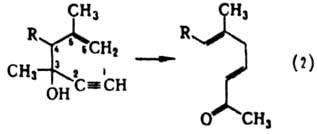
Эти р-ции обычно ускоряются в присут. электроно-акцепторных групп в положениях 3 и 4 и, в меньшей степени, электронодонорных групп в положениях 2 или 5; заместители в положениях 1 или 6 замедляют р-цию.
наиб. распространено представление о протекании К. п. по согласованному механизму, включающему [3,3] - сигматропный сдвиг, к-рый осуществляется через "креслоподобное" бp-электронное переходное состояние (ф-ла I):
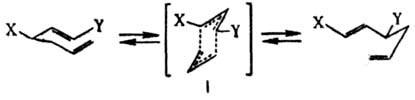
Считают также, что р-ция может протекать по гомолитич. механизму через промежут. образование пары аллильных радикалов или циклогексан-1,4-диильного бирадикала.
Побочный процесс при изомеризации 1,5-енин-З-олов-распад исходного соед. на низший олефин и a,b-ненасыщеннoe карбонильное соединение.
К. п. используют в орг. синтезе, напр. при получении гераниола, псевдоионона, терпеноидов, алкалоидов и др.
К. п. открыта А. Коупом и Э. Харди в 1940.
Лит.: Вудворд Р., Хоффман Р., Сохранение орбитальной симметрии, пер. с англ.. М.. 1971, с. 126-32, 160-63; Темникова Т. И., Семенова С. Н., Молекулярные перегруппировки в органической химия. Л., 1983; Rhoads S.J., Raulins N. R., в кн.: Organic reactions, v. 22, N.Y.-U 1975, p. 1-252; Lutz R. P., "Chem. Rev.", 1984, v. 84, № 3. p. 205-47; Overman LE, "Angew. Chem.", 1984, Bd 96, № 8, S. 565-73. Э. П. Серебряков.


