КОНСТАНТА СКOРОСТИ реакции, коэффициент пропорциональности в кинетич. ур-нии хим. р-ции, выражающем зависимость скорости р-ции v от концентрации к.-л. из компонентов реакц. смеси. Для бимолекулярных р-ций типа vAA+vBB: продукты, протекающих при постоянном объеме, согласно действующих масс закону, 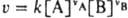 , где vA и vB - стехиометрич. коэф. реагирующих в-в А и В, k - константа скорости; численно k=v при [А]=[В]=1 моль/л. Для мономолекулярных р-ций К. с. имеет размерность с-1, для бимолекулярных - л/моль.с, для тримолекулярных - л2/моль2.с. Помимо истинной К. с. часто имеют дело с эффективной К. с. kэфф в рассматриваемом эксперименте; если, напр., бимолекулярная р-ция между А и В происходит при большом избытке в-ва В и концентрация [В] практически не меняется, кинетич. ур-ние р-ции м.б. записано в виде:
, где vA и vB - стехиометрич. коэф. реагирующих в-в А и В, k - константа скорости; численно k=v при [А]=[В]=1 моль/л. Для мономолекулярных р-ций К. с. имеет размерность с-1, для бимолекулярных - л/моль.с, для тримолекулярных - л2/моль2.с. Помимо истинной К. с. часто имеют дело с эффективной К. с. kэфф в рассматриваемом эксперименте; если, напр., бимолекулярная р-ция между А и В происходит при большом избытке в-ва В и концентрация [В] практически не меняется, кинетич. ур-ние р-ции м.б. записано в виде:
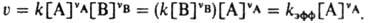
Для сложных р-ций, протекающих в неск. стадий, часто скорость р-ции не м.б. представлена как простая пропорциональная зависимость v от концентрации реагентов и выражается более сложным ур-нием, напр.: v=k'[A][B](l+k:[В])-1; тогда k' и k: наз. коэффициентами в ур-нии для скорости р-ции. Если скорость сложной р-ции м.б. выражена через произведение концентраций реагентов, то коэф. пропорциональности k наз. коэффициентом скорости или эффективной К.с. Если р-ция между А и В протекает на пов-сти (напр., катализатора) и ее скорость v~[А][В]S (S - площадь пов-сти), то k = v/[A][В]S чаще всего рассматривают как эмпирическую (кажущуюся) К. с. Зависимость К. с. от т-ры Г выражается Аррениуса уравнением: k=Aехр(-E/RT), где А - предэкспоненц. множитель, Е - энергия активации р-ции, R - газовая постоянная. Значения К. с. изменяются с т-рой в широких пределах, напр. для бимолекулярных р-ций - от 1010 до 10-10 л/моль.с. К. с. -фундам. кинетич. характеристика р-ции в данных условиях (фаза, среда, т-ра, давление), не зависящая от концентраций реагентов. Нахождение К. с. из эксперим. данных наз. обратной задачей хим. кинетики; использование известных К. с. для расчета концентраций компонентов реакц. смеси в данный момент времени (при известных начальных концентрациях) в хим. кинетике наз. прямой задачей. Лит. см. при ст. Кинетика химическая. Е. Т. Денисов.
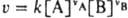 , где vA и vB - стехиометрич. коэф. реагирующих в-в А и В, k - константа скорости; численно k=v при [А]=[В]=1 моль/л. Для мономолекулярных р-ций К. с. имеет размерность с-1, для бимолекулярных - л/моль.с, для тримолекулярных - л2/моль2.с. Помимо истинной К. с. часто имеют дело с эффективной К. с. kэфф в рассматриваемом эксперименте; если, напр., бимолекулярная р-ция между А и В происходит при большом избытке в-ва В и концентрация [В] практически не меняется, кинетич. ур-ние р-ции м.б. записано в виде:
, где vA и vB - стехиометрич. коэф. реагирующих в-в А и В, k - константа скорости; численно k=v при [А]=[В]=1 моль/л. Для мономолекулярных р-ций К. с. имеет размерность с-1, для бимолекулярных - л/моль.с, для тримолекулярных - л2/моль2.с. Помимо истинной К. с. часто имеют дело с эффективной К. с. kэфф в рассматриваемом эксперименте; если, напр., бимолекулярная р-ция между А и В происходит при большом избытке в-ва В и концентрация [В] практически не меняется, кинетич. ур-ние р-ции м.б. записано в виде:
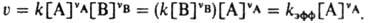
Для сложных р-ций, протекающих в неск. стадий, часто скорость р-ции не м.б. представлена как простая пропорциональная зависимость v от концентрации реагентов и выражается более сложным ур-нием, напр.: v=k'[A][B](l+k:[В])-1; тогда k' и k: наз. коэффициентами в ур-нии для скорости р-ции. Если скорость сложной р-ции м.б. выражена через произведение концентраций реагентов, то коэф. пропорциональности k наз. коэффициентом скорости или эффективной К.с. Если р-ция между А и В протекает на пов-сти (напр., катализатора) и ее скорость v~[А][В]S (S - площадь пов-сти), то k = v/[A][В]S чаще всего рассматривают как эмпирическую (кажущуюся) К. с. Зависимость К. с. от т-ры Г выражается Аррениуса уравнением: k=Aехр(-E/RT), где А - предэкспоненц. множитель, Е - энергия активации р-ции, R - газовая постоянная. Значения К. с. изменяются с т-рой в широких пределах, напр. для бимолекулярных р-ций - от 1010 до 10-10 л/моль.с. К. с. -фундам. кинетич. характеристика р-ции в данных условиях (фаза, среда, т-ра, давление), не зависящая от концентраций реагентов. Нахождение К. с. из эксперим. данных наз. обратной задачей хим. кинетики; использование известных К. с. для расчета концентраций компонентов реакц. смеси в данный момент времени (при известных начальных концентрациях) в хим. кинетике наз. прямой задачей. Лит. см. при ст. Кинетика химическая. Е. Т. Денисов.


