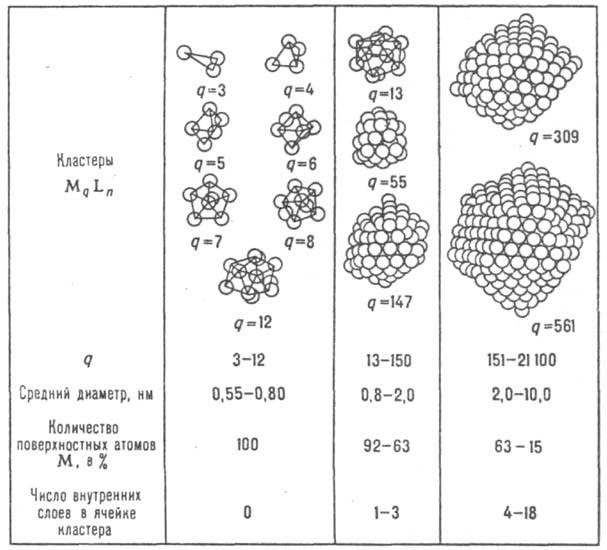
q/n<1 q/n~1 q/n>1 q>n
Кластерные соединения металлов (показаны только остовы кластеров).
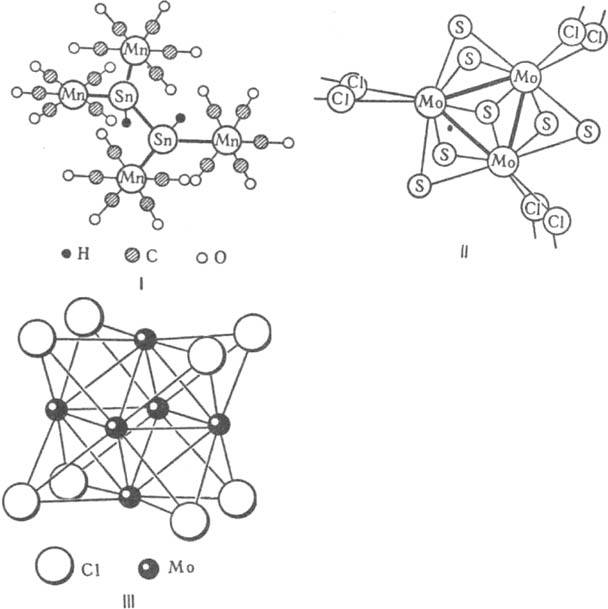
цепей разл. длины и разветвленности, напр. H2Sn2[Mn(CO)5]4 (ф-ла I), циклов, напр. Mo3S7Cl4 (II), полиэдров, напр. [Мо6Сl8]4+ (III), она м. б. каркасной, а также представлять собой комбинацию из перечисл. структурных элементов. Из
возможных полиэдров чаще всего реализуются те, стороны к-рых - правильные треугольники, напр. октаэдр III.
Кластерные соед. характерны как для переходных металлов, так и для многих непереходных. Известны гомометаллич. К., остов к-рых состоит из атомов одного металла, и гетерометал-лич. К., содержащие в остове атомы двух, трех и более металлов. Металлич. остов в молекулах К. покрыт плотным слоем лигандов, как концевых, так и мостиковых. Лигандами м. б. отдельные атомы (Н, Cl, Br, I, Se и др.), группы атомов (CR, ЭL) или молекулы (СО, NO, олефи-ны, арены и др.). Иногда моноатомные лиганды (N, С, Н, Р и др.) расположены внутри полостей металлич. остова, имеющего с внеш. стороны др. лиганды. Существует глубокое топологич. соответствие между строением кластерных соед. металлов и полиэдрич. соед. неметаллов (В, Р, As и др.). Изолобальной аналогии принцип позволяет, напр., заменить атомы В в полиэдре на металлсодержащие группы с образованием металлоборанов - соед., занимающих промежут. положение между каркасными неметаллич. соед. (часто также наз. кластерными) и металлич. К. Из рассмотрения структуры, электронного строения, энергетики известных К. следует, что на основе любого элемента периодич. системы м. б. реализованы кластерные соединения.
Назв. простейших К. строятся в соответствии с номенклатурными правилами ИЮПАК для координационных соединений, напр.: [Со6С(СО)14]- - карбидогекса-m-карбонил-октакарбонил-полиэдро-гексакобальт(1-)-ион; Ru4CO12(C2Ph2)-дифенилацетилен-клозо-тетракис-(тикарбонилрутений). Однако в связи с большой сложностью таких названий и трудностями, возникающими при использовании тех же правил для К. с большей нуклеарностью, К. обычно обозначают брутто-формулами и структурными ф-лами.
Электронное строение. Теория хим. связи в кластерных соед. находится в стадии разработки. В большинстве теоретич. работ устанавливают связь между общим числом т. наз. кластерных валентных электронов (КВЭ) и строением остова. Общее число КВЭ вычисляют по след. схеме: к суммарному числу электронов валентных оболочек атомов металлов, образующих остов молекулы К., прибавляют число электронов, предоставляемых лигандами по обычным правилам (см. Металлоорганические соединения); для кластерных ионов прибавляется также заряд К., взятый с обратным знаком. Напр., для H2Ru6(CO)18 число КВЭ=(6.8)Ru+(2.18)co+(2.l)H=86, для Со6(СО)16 (6.9)Со+(2.16)со=86, для [Со6(СО)15]2- (6.9)Со+(2.15)со+2=86. Осн. особенность небольших полиэдрич. К.-существование "магических" чисел КВЭ, определяющих геометрию полиэдров, что особенно хорошо соблюдается для разл. К. переходных металлов однотипного строения. Изменение числа валентных электронов приводит к перестройке металлополиэдра. Так, для треугольных К. магическое число КВЭ
равно 48, для тетраэдрических - 60, для октаэдрических - 86. Однако оказалось, что кол-во К. с числом КВЭ, отличным от магического, сравнимо с кол-вом К., имеющих магическое число КВЭ.
Квантовохим. расчет молекул кластерных соед. основан на приближении линейной комбинации орбиталей (см. ЛКАО - приближение). При этом, исходя из данных об энергиях и форме отдельных фрагментов молекул К., составляют орбитали, локализованные на фрагментах, затем получают делокализованные мол. орбитали (МО) кластерной молекулы в виде линейной комбинации МО, локализованных на фрагментах. Разработаны два подхода к описанию электронного строения К. с этих позиций. В первом случае (для средних и крупных К.) молекулу МqLn псевдосферич. симметрии разбивают на след. фрагменты: Мq - сферич. металлич. ядро (остов К.) - и окружающая оболочка из лигандов Ln. При ином способе фрагментации молекулу, как правило, низкой нуклеарности делят на одинаковые фрагменты MLm, где m = n/q. В первом подходе МО кластерной молекулы получают, комбинируя "внешние" МО металлич. остова с подходящими по симметрии МО лигандной сферы; при втором подходе МО строят из граничных орбиталей фрагментов MLm с учетом общей симметрии К. Для малых К. в основе существования корреляции между геометрией остова и числом КВЭ лежат значит. энергетич. различия между заполненными связывающими орбиталями и вакантными разрыхляющими. По мере роста размеров К. эти различия уменьшаются и энергия верх, заполненных МО в крупных К. практически совпадает с энергией Ферми (ЕF) для массивного металла; для переходных металлов EF~4-5 эВ близка к энергиям p-орбиталей своб. атомов металлов. Принято, что МО, лежащие ниже р-орбитали своб. атома металла, являются в К. валентными. Эти кластерные валентные МО построены преим. из орбиталей d- и s-типов с частичным вкладом р-орбиталей. Высоколежащие разрыхляющие МО кластерных молекул построены преим. из атомных p-орбиталей с нек-рым вкладом s-орбиталей. При координации лигандов с ядром К. валентные МО модифицируются вследствие участия в связывании, а разрыхляющие МО претерпевают меньшие изменения (из-за большей разницы по энергиям с орбиталями лигандов) и в молекуле реального К. остаются вакантными. Выделяя разрыхляющие МО на молекулярно-орбитальной диаграмме К., рассчитанной по расширенному методу Хюккеля, получают магические числа электронов, к-рые могут разместиться на валентных МО данного кластерного полиэдра при координации его лигандами (см. Молекулярных орбиталей методы).
Свойства. Кластерные соед. - окрашенные в темные цвета кристаллы [известны отдельные примеры слабоокрашенных или почти бесцв. соед.-Оs3(СО)12 и др.]. Большинство незаряженных К. умеренно растворимы в орг. р-рителях. Соли, содержащие кластерные ионы, раств. только в полярных орг. р-рителях, в редких случаях - в воде. Нек-рые незаряженные К. низкой нуклеарности летучи и их можно исследовать масс - спектрометрически. Большинство К. диамагнитно.
К. участвуют в р-циях двух типов - затрагивающих остов К. и не затрагивающих, когда реагируют только лиганды в лигандной оболочке. Окислит. - восстановит. р-ции включают перенос электронов в остове К., к-рый не сопровождается перестройкой самого остова, но приводит к изменению нуклеарности остова К. (окислит. деградация). Напр., в гетерометаллич. октаэдрич. К. возможны два направления р-ции - элиминирование осн. кластеробразующего элемента или гетероатома. Так, К. состава [Fe6C(CO)16]2- при окислении переходит в пятиядерный нейтральный Fe5C(CO)15, a в К. состава [Fe3M3C(CO)15]-, где М = Rh, Co, при окислении всегда элиминирует Rh или Со.
Р-ции присоединения характерны как для гомо-, так и для гетерометаллич. К., при этом вместе с изменением числа КВЭ происходит и перестройка металлополиэдров. Так, К. с конфигурацией тетрагон. пирамиды (число КВЭ 74) в
зультате р-ций присоединения переходят в октаэдрич. К. (число КВЭ 86).
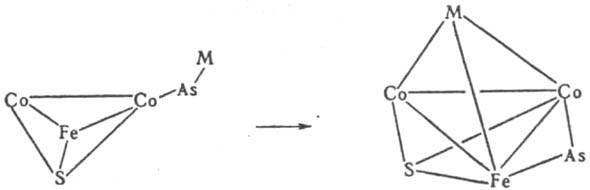
Разрыв одной из связей металл-металл в остове К., имеющего магическое число КВЭ, как правило, происходит в результате присоединения по этой связи двухэлектронного лиганда; разрыв одной из связей металл-металл сопровождается перегруппировкой остова К., напр. тетраэдр [H3Os4(CO)12]- переходит в "бабочку" H3Os4(CO)12NO. Замещение одного металла на другой при сохранении нуклеарности К. идет в соответствии с принципом изолобальной аналогии металлсодержащих фрагментов. наиб. активны в р-циях замещения галогениды металлов, напр.: [Fe6C(CO)16J2-+RhCl3.H2O:[Fe5RhC(CO)16]-.
Координация (реберная, граневая) лигандов на неск. металлич. центрах в К. существенно отличается от координации тех же лигандов в моноядерных комплексах, соотв. кардинально меняется и реакц. способность этих лигандов. Напр., необычен способ граневой координации молекул бензола на трех металлич. центрах в трехъядерных кластерах Os и Ru. В отличие от моно- и бис-ареновых комплексов переходных металлов, в к-рых плоская молекула бензола связана с металлом симметрично всеми шестью атомами углерода, в К. координация бензола с металлоциклом осуществляется благодаря одной связи С—С бензольного кольца, при этом два атома Н в качестве мостиковых лигандов переходят в металлоцикл (IV). Молекула этилена
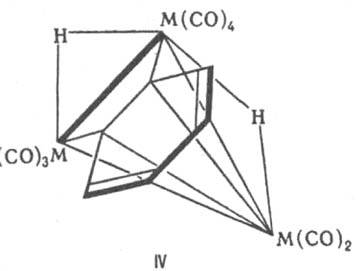
связана с трехъядерным металлоциклом Os3 (реберная координация) посредством одной a- и одной p-связи (V). При нагр. К. винильный лиганд теряет еще один атом Н (к-рый переходит в качестве лиганда в металлоцикл) и перемещается над плоскостью цикла Os3, что приводит к возникновению особого типа граневой координации (VI):
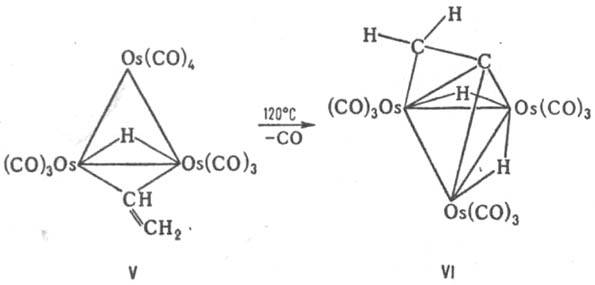
Методы синтеза. Кластерные соед. образуются при восстановлении солей металлов в присут. соответствующих лигандов, напр.:
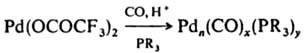
(п=3, х = 3, у=4; n=4, х=5, у = 4; n=10, х=14, у=4; n=23, x=20, у=8; n=38, х=28, у=12). К. получают также термич. или фотохим. отщеплением лигандов от др. К., напр.:
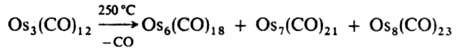
Лиганды СО отщепляются также при действии сильных восстановителей, напр.:
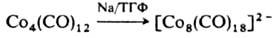
Разработаны менее общие приемы получения К. заданной нуклеарности, напр. при "сдваивании" димеров с кратными связями металл-металл:
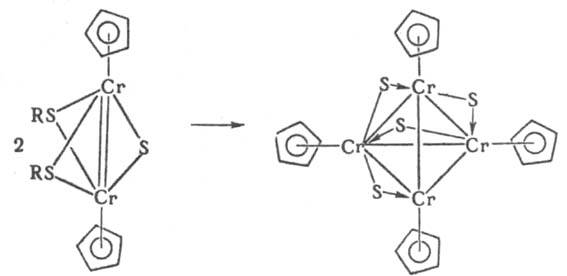
или благодаря "стягивающему" эффекту лигандов:
Кластерные частицы - безлигандные металлич. К. в виде ультрадисперсных металлич. систем или "голых" кластерных ионов. Это особое состояние в-ва, занимающее промежут. положение между кластерными соед., с одной стороны, и коллоидными частицами, чернями, порошками и, наконец, компактными материалами, с другой. Они имеют след. отличит. особенности: доля поверхностных атомов металла соизмерима с числом атомов в объеме частицы; поверхностная и внутр. энергия отдельно взятой частицы также соизмеримы; кристаллич. структура кластерных частиц отличается от структуры массивного образца металла - отсутствует плотная упаковка, увеличены расстояния между атомами и т. д. Форма и структура кластерной частицы носят неравновесный характер и соответствуют состояниям с энергией, отличной от минимальной. В кластерном состоянии могут находиться как любые металлы и сплавы, так и карбиды, нитриды, оксиды, бориды, сульфиды и др., в т. ч. кластерные частицы могут присутствовать в керамич. и композиц. материалах.
Методы получения кластерных частиц основаны на конденсации пара металла. Они отличаются по способам испарения металла (плазменное, термическое в ячейке Кнудсена, электроннолучевое) и по способам конденсации пара металла (сверхзвуковое истечение пара металла в вакуум, испарение в разреженной атмосфере инертного газа-метод газового испарения, криогенная конденсация пара металла на подложку, гомог. нуклеация металлич. пара и др.). Общее условие формирования ультрадисперсных частиц в таких системах - высокая скорость нуклеации при возможно меньшей скорости роста размеров частиц. Особое значение для получения ультрадисперсных частиц имеют взрывные методы; напр., метод электрич. взрыва проводников может с успехом использоваться для получения кластерных частиц трудноиспаряемых тугоплавких металлов. Хим. методы получения кластерных частиц основаны на термич. и фотохим.
разложении соед. металлов с летучими лигандами (карбонилов металлов, солей орг. к-т и др.).
Св-ва кластерных частиц и материалов на их основе сильно зависят от размеров частиц. Однако большинство методов получения кластерных частиц не позволяет контролировать рост К. в такой степени, чтобы получать ультрадисперсные частицы строго определенного и одинакового размера. Даже узкое (с разбросом не более b10%) распределение частиц по размерам - пока еще трудно достижимая цель.
Кластерные материалы. Представляют собой матрицу, в к-рой равномерно распределены металлич. К.-соед. или частицы. Матрицами чаще всего служат карбоцепные полимеры, напр. полиэтилен, графит и цеолиты. Установлена связь уникальных физ. характеристик кластерных материалов (квазиодномерной металлич. проводимости, полупроводниковых, сверхпроводящих, магн. св-в, особенностей взаимод. с излучением и др.) именно с наличием у них значительных взаимод. металл - металл, определяющих тип структуры материалов. Возможность достаточно широкого варьирования межъядерных расстояний металл-металл, природы и числа лигандов, степени окисления металла и др. факторов позволяет создавать материалы с тем или иным типом проводимости.
Разработан ряд методов заполнения каналов в жестких цеолитовых матрицах металлическими К.; таким путем получены К. ртути, железа, серебра и др. Показано, напр., что цеолиты, содержащие К. железа, - хорошие катализаторы синтезов по Фишеру-Тропшу, обладают высокой активностью и селективностью по отношению к метану, устойчивы длит. время и легко регенерируются. Исследуются каталитич. св-ва металлонаполненных полимеров и цеолитов. Найдены условия формирования металлич. К. в полимерных матрицах (полиэтилене, полипропилене, полифениленоксиде и др.) методом высокоскоростного термораспада р-ров соед. металлов в расплавах полимеров. Размер металлич. К. зависит от концентрации металла и природы матриц и находится в пределах 1,5-3,0 нм с узким распределением по размерам; К. расположены периодично в изотропном материале. Такие материалы являются новым классом однофазных металлополимеров с повыш. термич. устойчивостью, улучшенными мех. и необычными магн. и электрич. св-вами.
Применение. Кластерные соед. типа Fe4S4 входят в состав ферментов, таких, как ферредоксины, нитрогеназа, и играют большую роль в ряде важнейших биол. процессов (окисление, фиксация атм. азота и др.). Кластерные группировки -осн. структурные элементы т. наз. фаз Шеврёля состава PbMo6S8 (см. Молибдена сульфиды) - сверхпроводящих материалов с высокими критич. т-рами. Цепочки из атомов металлов - осн. структурный элемент квазиодномерных проводящих материалов.
Использование кластерных соед. в качестве катализаторов - важное направление в исследованиях по катализу. К. переходных металлов занимают промежут. положение между гетерогенными и гомогенными (металлокомплексными) катализаторами, сохраняя преимущества тех и других. Разработаны методы закрепления кластерных соед. на пов-сти носителей, в результате чего получен новый тип гетерог. катализаторов - кластерных, перспективных для процессов, в к-рых требуется участие в каталитич. акте нескольких (в т. ч. разных) атомов металлов. Реализованы процессы каталитич. гидрирования и окисления на кластерных палладиевых катализаторах.
Координац. соед. с неск. атомами металла, соединенными мостиковыми атомами неметаллич. элементов, часто наз. "обменными кластерами", рассмотрены в статье Полиядерные соединения.
Лит.. Петров Ю. И.. Физика малых частиц, М., 1982; Губин С. П., "Вестник АН СССР", 1984, № 1. с. 5-59; его же, "Успехи химии", 1985, т. 54, в. 4. с. 529-55; его же, Химия кластеров. Основы классификации и строение, М., 1987; Петров Ю. И., Кластеры и малые частицы. М., 1986.
С. П. Губин.


