КАРБОНОВЫЕ КИСЛОТЫ, орг. соед., содержащие карбоксильную группу СООН. По кол-ву этих групп различают одно-, двух- и многоосновные к-ты (см. также Дикарбоновые кислоты). Могут содержать Hal, а также группы NH2, С=О, ОН (соотв. галогенкарбоновые кислоты, аминокислоты, альдегидо- и кетокислоты, оксикислоты). Алифатич. к-ты, у к-рых число атомов С в молекуле больше 6, относят к высшим жирным кислотам.
По номенклатуре ИЮПАК, к-ты называют, выбирая за основу наиб. длинную цепь, содержащую группу СООН, и добавляя к назв. соединения-основы окончание "овая" и слово "к-та"; атому С карбоксильной группы приписывают номер 1, напр. СН3(СН2)4СН(СН3)СООН - 2-метилгептановая к-та. Часто к назв. соединения-основы добавляют слова "карбоновая к-та", напр. С6Н11СООН - циклогексанкарбоновая к-та. При использовании этого способа наименования в алифатич. ряду атом С карбоксильной группы в нумерацию цепи не включается. Мн. к-ты имеют тривиальные названия (см. табл.).
В своб. состоянии к-ты находятся в плодах нек-рых растений, крови, выделениях животных; они входят в состав жиров, эфирных и растит. масел, восков. Важную роль К. с. играют в обмене веществ.
Свойства. Карбоксильная группа имеет строение, промежуточное между двумя предельными структурами:

Группа планарна; длина связи С=О в разл. к-тах составляет 0,118-0,126 нм, связи С=О - 0,121-0,137 нм; угол ОСО 118-125,5°; m 5,4.10-30 Кл.м. В твердом и жидком состоянии к-ты в результате возникновения водородных связей образуют устойчивые циклич. димеры (ф-ла I).
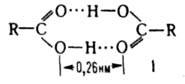
Атомы, образующие цикл, лежат практически в одной плоскости, а водородные связи (энергия 29 кДж/моль) почти линейны.
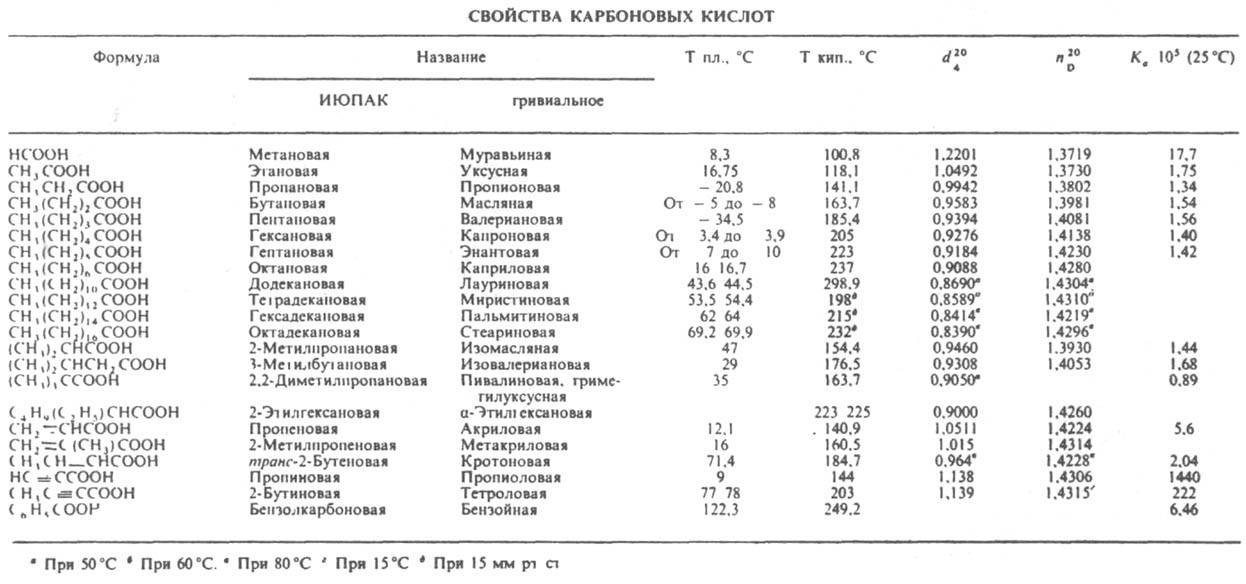
В р-рах к-т в инертных р-рителях существует равновесие между мономером и димером. В водных р-рах к-ты образуют ациклич. димеры. Насыщ. неразветвленные к-ты до С9 и разветвленные до С13 - жидкости, высшие - твердые в-ва. Т-ры плавления четных гомологов выше, чем ближайших нечетных. Высокие т-ры кипения и плавления к-т по сравнению с соед. с близкой мол. массой, но не содержащими группы СООН, обусловлены их димеризацией. Для неразветвленных насыщ. к-т, начиная с С5, DH0обр линейно связана с числом атомов углерода: - DH0обр = 458,8 + 25,5n кДж/моль, где n - число СН2-групп в молекуле к-ты. Расчетная DH0обр группы СООН - 149,6 кДж/моль. Важнейшее св-во к-т - их способность к диссоциации (ионизации) в водном р-ре с образованием стабилизир. карбоксилатного аниона и катиона гидроксония:
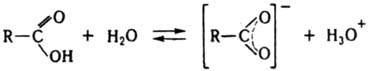
Величина рКа большинства алифатич. к-т ок. 4,8. Электроноакцепторные заместители, в т. ч. кратные связи, стабилизирующие карбоксилатный анион, увеличивают кислотность, электронодонорные снижают ее, однако в значительно меньшей степени. Влияние заместителя быстро падает по мере его отдаления от группы СОО-. К-ты C1-С3 смешиваются с водой во всех соотношениях, с ростом цепи р-римость падает. ИК спектры к-т характеризуются след. полосами поглощения n (в см-1):
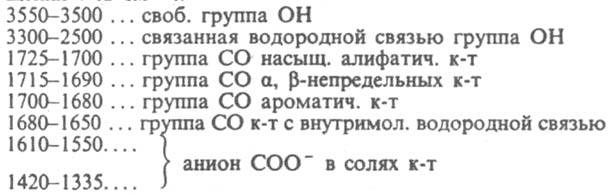
В УФ спектре к-т имеются слабые полосы п : p*-перехода при 200-210 нм и более сильные полосы p : p*-перехода при 210-220 нм в случае a,b-ненасыщ. к-т. Спектры ЯМР характеризуются хим. сдвигом протона карбоксильной группы при d 10,5-12 м.д. К. к. образуют твердые соли RCOOM. Na- и К-соли хорошо раств. в воде и хуже, чем исходные к-ты, в орг. р-рителях. Соли к-т от С11 и выше наз. мылами. При действии галогенангидридов неорг. к-т (РОСl3, РСl5, РСl3, SOCl2) К к. образуют галогенангидриды, при дегидратации - ангидриды. Атака нуклеоф. агента на атом С карбоксильной группы лежит в основе превращ. к-т во мн. производные (эфиры, амиды, тиоэфиры, гидразиды и др.), а также р-ций с металлоорг. соед. и процессов восстановления, напр.:
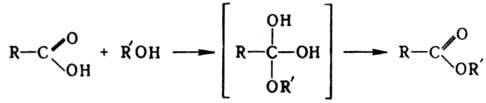
При образовании эфиров увеличение электрофильности карбонильного атома С достигается катализом ионами Н+ или предварит. превращением к-т в производные. Кислотный катализ осуществляется неорг. к-тами, сульфокислотами, катионитами, BF3 и др. В качестве производных используют галогенангидриды и ангидриды к-т, а также реакционноспособные промежуточные соед., получаемые in situ: О-ацилизомочевины (при действии на к-ты карбодиимидов), ацилимидазолиды (при действии N,N'-карбонилдиимидазола), N-ацилтиопиридины (при действии дипиридилсульфида и трифенилфосфина), N-ацилпиридиниевые соли (при действии N-галогенпиридиниевых солей) и др. Металлоорг. соед. реагируют с к-тами с образованием на первой стадии солей. Р-ция Li-соли с литийорг. соед. важный метод синтеза кетонов:
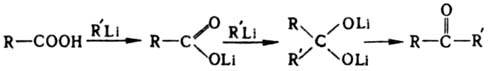
Магнийорг. соед. реагируют с солями только в жестких условиях, образуя, как правило, третичные спирты. Восстановление к-т приводит к альдегидам и далее к первичным спиртам. Избират. превращение к-т в альдегиды достигается действием Li в метиламине, где образующийся альдегид защищается р-рителем в виде азометина:
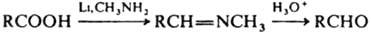
Др. методы восстановления до альдегида требуют превращ. к-т в их производные. Так, хлорангидриды восстанавливаются до альдегидов на Pd-катализаторах (Розенмунда реакция), хлорангидриды и ангидриды, в т.ч. смешанные, действием Na2Fe(CO)4, иминохлориды - хлористым оловом, арилсульфонилгидразиды ароматич. к-т - термич. разложением в присут. Na2CO3, разл. гетероциклич. производные к-т, напр., иодалкилаты оксазолинов, действием NaBH4. Борогидриды не восстанавливают к-ты, a LiAlH4 восстанавливают их в спирты. При одноэлектронном окислении к-т происходит их декарбоксилирование, приводящее к радикалам и далее к карбкатионам:
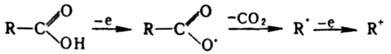
В зависимости от условий при превращ. радикалов и карбкатионов образуются разл. продукты: алканы, алкены, алкилгалогениды (см. Декарбоксилирование, Бородина-Хунсдиккера реакция, Кольбе реакции). Электроноакцепторные св-ва группы СООН (константа Тафта s* = 2,1) проявляются в избират. a-галогенировании насыщ. к-т:
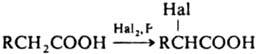
Наряду с прямым галогенированием в присут фосфора и его производных (Гелля-Фольгарда-Зелинского реакция), используется также взаимод. с N-хлор- и N-бромсукцинимидами и иодирование в присут. SOCl2. При свободнорадикальном хлорировании в сильнокислой среде к-т от С4 и выше образуются преим. продукты хлорирования по атому С-4. Отрицат. мезомерный эффект группы СООН (константы Гаммета sм = 0,37, sn = 0,45) дезактивирует бензольное кольцо ароматич. к-т, вследствие чего не удается провести их алкилирование и ацилирование. Галогенирование ароматич. к-т приводит к мета-производным. Ароматич. к-ты легко восстанавливаются металлами в жидком NH3, образуя дианион, протонируемый и алкилируемый по a-положению, напр.:
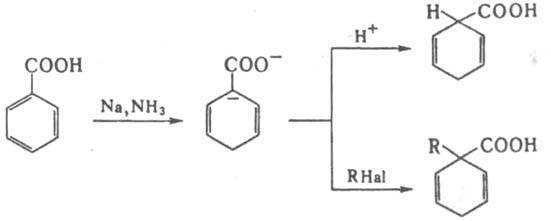
В аналогичных условиях восстанавливаются двойные связи a,b-непредельных к-т. К. к. с несопряженными двойными связями восстанавливаются каталитически. Особая р-ция b, g- и g,d-ненасыщ. к-т - галолактонизация, т.е. образование галогензамещенных лактонов:
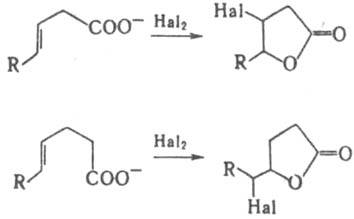
Получение. В пром-сти наиб. распространены окислительные и гидролитич. методы, а также гидрокарбонилирование. Окисление в присут. солей Со, Mn, Fe, Ni, Се применяют, напр., при получении к-т из альдегидов, уксусной к-ты из бутана, бензойной к-ты из толуола. Гидрокарбонилирование (гидрокарбоксилирование) проводят присоединением СО и Н2О к алкенам, алкинам, арил(алкил)галогенидам и тозилатам ароматич. и алифатич. спиртов под давлением в присут. катализаторов - комплексов Ph3P с солями Pd, p-аллильных комплексов Ni либо действием карбонилов Ni или Со, напр.
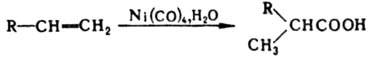
См. также Карбонилирование, Коха-Хаафа реакция. Для получения высших жирных к-т используют гидролиз животных жиров и растит масел, для получения w-галогенкарбоновых к-т гидролиз трихлорметильной группы продуктов теломеризации олефинов и ССl4. Применяется также щелочное плавление спиртов, получаемых оксосинтезом (до С10):
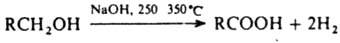
Уксусную и масляную к-ты получают брожением. Для препаративного синтеза к-т используют окисление первичных спиртов и альдегидов. Окислители - соед. Сr, Мn, в т.ч. солюбилизированный краун-6-эфиром КМnО4 в бензоле "пурпурный бензол", кислород в присут. катализаторов (соли Со, Fe, Се) или без них, НIO4 и ее соли, NaClO4, система RuO2 + КIO4, а также электрохим. окисление. К. к. могут быть получены также окислением арилметилкетонов, алкенов, алкинов, напр.:
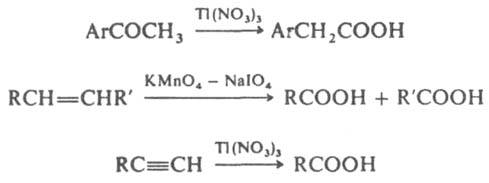
Их также синтезируют карбоксилированием металлоорг. соед. или действием СО2 на алкилиденфосфораны (илиды фосфора):
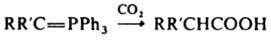
Гидролиз эфиров, амидов, нитрилов и др. производных к-т является как самостоят. методом получения к-т, так и составной частью мн. методов их синтеза, в т.ч. синтезов с эфирами малоновой и ацетоуксусной к-т, р-ции Реформатского. Классич. гидролиз эфиров включает разрыв О-ацильной связи под действием щелочи или к-ты. Более мягкие и избират методы гидролиза эфиров - О-алкильное расщепление их метиловых эфиров с помощью Li в ДМФА, этантиолята Li, NaCN в гексаметаполе, BF3 в СН2Сl2 и др. Амиды более устойчивы к гидролизу, чем эфиры, но легко гидролизуются с помощью Н2О2 в щелочной среде или нитрит-иона в кислой. К. к. получают также введением в орг. молекулу a-карбоксиалкильной СН2СООН или карбоксиалкилиденовой =СНСООН групп. К этим методам относятся классич. синтезы на основе производных малоновой и ацетоуксусной к-т и р-ции производных уксусной к-ты. Превращ. диэтилового эфира малоновой к-ты в анион под действием оснований и его алкилирование галогеналкилами приводит к эфирам замещенных малоновой к-ты, деалкоксикарбонилирование и гидролиз к-рых дает к-ты:
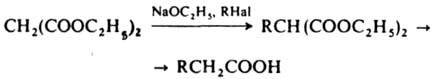
Применение диизопропиламида лития и др. аналогичных амидов позволило получать устойчивые дианионы монокарбоновых к-т и непосредственно вводить группу —СН2СООН:
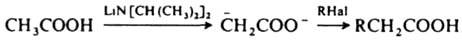
Др. способ введения этой группы р-ции эфиров a-галогенкарбоновых к-т с карбонильными соед. в присут. Zn или с алкилиденфосфораном и послед. гидролиз (см. Реформатского реакция, Виттига реакция). Используют также радикальное присоединение эфиров к-т к алкенам или аренам в присут. пероксидов, напр.:
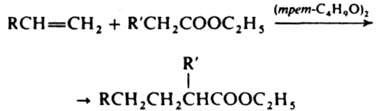
Для получения к-т из кетонов используют Байера-Виллигера реакцию. Галоформную реакцию, из альдегидов Канниццаро реакцию К-ты синтезируются с помощью перегруппировок и р-ций конденсации (см. Дарзана реакция, Кнёвенагеля реакция, Михаэля реакция, Перкина реакция, Фаворского реакции). Имеется неск. методов, применяемых только для синтеза ароматич. К. к., напр., карбоксилирование фенолятов металлов (Кольбе-Шмитта реакция)и р-ция Фриделя - Крафтса с использованием фосгена:
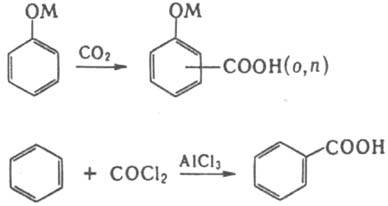
Разработаны спец. методы превращ. к-т в высшие гомологи, напр. Арндта- Айстерта реакция, и перевод в низший гомолог:
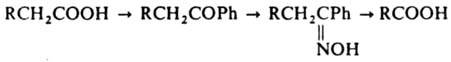
Определение. Качеств. анализ основан на определении рН водных или водно-спиртовых р-ров, выделении к-тами СО2 из р-ров NaHCO3, образовании нерастворимых солей Рb и Ag. Цветная р-ция - превращ. К. к. в гидроксамовые к-ты и образование окрашенных гидроксаматов Fe. К-ты образуют ряд производных с четкой т-рой плавления, применяемых для их идентификации (анилиды, фенациловые эфиры, уреиды, соли S-бензилизотиурония, гидразиды). Методы количеств. анализа включают водное и неводное титрование, определение активного водорода, напр., методом Церевитинова, превращ. в гидроксамовые к-ты и их колориметрич. определение, этерификацию метанолом и определение кол-ва выделившейся воды реактивом Фишера, декарбоксилирование и определение выделившегося СО2. Широко используются тонкослойная и газожидкостная хроматографии.
Применение. К-ты исходные соед. для получения промежут. продуктов орг. синтеза, в частности кетенов, галогенангидридов, виниловых эфиров, галогенкислот. Соли К. к. и щелочных металлов применяют как мыла, эмульгаторы, смазочные масла; соли тяжелых металлов - сиккативы, инсектициды и фунгициды, катализаторы. Эфиры к-т - пищ. добавки, р-рители; моно- и диэфиры гликолей и полигликолей пластификаторы, компоненты лаков и алкидных смол; эфиры целлюлозы - компоненты лаков и пластмассы. Амиды к-т эмульгаторы и флотоагенты. Об индивидуальных к-тах см., напр., в ст. Акриловая кислота, Бензойная кислота. Масляная кислота, Муравьиная кислота, Уксусная кислота. Лит.: Общая органическая химия, пер. с англ., т. 4, М., 1983, с. 11-137; The chemistry of carboxylic acids and esters, ed. by S. Patai, L, 1969; The chemistry of acid derivatives, ed. by S. Patai, pt. 1-2, N.Y., 1979. Д. В. Иоффе.
Свойства. Карбоксильная группа имеет строение, промежуточное между двумя предельными структурами:

Группа планарна; длина связи С=О в разл. к-тах составляет 0,118-0,126 нм, связи С=О - 0,121-0,137 нм; угол ОСО 118-125,5°; m 5,4.10-30 Кл.м. В твердом и жидком состоянии к-ты в результате возникновения водородных связей образуют устойчивые циклич. димеры (ф-ла I).

Атомы, образующие цикл, лежат практически в одной плоскости, а водородные связи (энергия 29 кДж/моль) почти линейны.

В р-рах к-т в инертных р-рителях существует равновесие между мономером и димером. В водных р-рах к-ты образуют ациклич. димеры. Насыщ. неразветвленные к-ты до С9 и разветвленные до С13 - жидкости, высшие - твердые в-ва. Т-ры плавления четных гомологов выше, чем ближайших нечетных. Высокие т-ры кипения и плавления к-т по сравнению с соед. с близкой мол. массой, но не содержащими группы СООН, обусловлены их димеризацией. Для неразветвленных насыщ. к-т, начиная с С5, DH0обр линейно связана с числом атомов углерода: - DH0обр = 458,8 + 25,5n кДж/моль, где n - число СН2-групп в молекуле к-ты. Расчетная DH0обр группы СООН - 149,6 кДж/моль. Важнейшее св-во к-т - их способность к диссоциации (ионизации) в водном р-ре с образованием стабилизир. карбоксилатного аниона и катиона гидроксония:
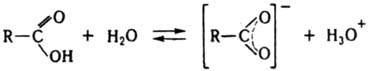
Величина рКа большинства алифатич. к-т ок. 4,8. Электроноакцепторные заместители, в т. ч. кратные связи, стабилизирующие карбоксилатный анион, увеличивают кислотность, электронодонорные снижают ее, однако в значительно меньшей степени. Влияние заместителя быстро падает по мере его отдаления от группы СОО-. К-ты C1-С3 смешиваются с водой во всех соотношениях, с ростом цепи р-римость падает. ИК спектры к-т характеризуются след. полосами поглощения n (в см-1):

В УФ спектре к-т имеются слабые полосы п : p*-перехода при 200-210 нм и более сильные полосы p : p*-перехода при 210-220 нм в случае a,b-ненасыщ. к-т. Спектры ЯМР характеризуются хим. сдвигом протона карбоксильной группы при d 10,5-12 м.д. К. к. образуют твердые соли RCOOM. Na- и К-соли хорошо раств. в воде и хуже, чем исходные к-ты, в орг. р-рителях. Соли к-т от С11 и выше наз. мылами. При действии галогенангидридов неорг. к-т (РОСl3, РСl5, РСl3, SOCl2) К к. образуют галогенангидриды, при дегидратации - ангидриды. Атака нуклеоф. агента на атом С карбоксильной группы лежит в основе превращ. к-т во мн. производные (эфиры, амиды, тиоэфиры, гидразиды и др.), а также р-ций с металлоорг. соед. и процессов восстановления, напр.:

При образовании эфиров увеличение электрофильности карбонильного атома С достигается катализом ионами Н+ или предварит. превращением к-т в производные. Кислотный катализ осуществляется неорг. к-тами, сульфокислотами, катионитами, BF3 и др. В качестве производных используют галогенангидриды и ангидриды к-т, а также реакционноспособные промежуточные соед., получаемые in situ: О-ацилизомочевины (при действии на к-ты карбодиимидов), ацилимидазолиды (при действии N,N'-карбонилдиимидазола), N-ацилтиопиридины (при действии дипиридилсульфида и трифенилфосфина), N-ацилпиридиниевые соли (при действии N-галогенпиридиниевых солей) и др. Металлоорг. соед. реагируют с к-тами с образованием на первой стадии солей. Р-ция Li-соли с литийорг. соед. важный метод синтеза кетонов:
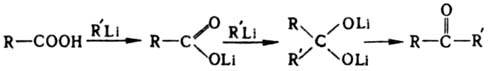
Магнийорг. соед. реагируют с солями только в жестких условиях, образуя, как правило, третичные спирты. Восстановление к-т приводит к альдегидам и далее к первичным спиртам. Избират. превращение к-т в альдегиды достигается действием Li в метиламине, где образующийся альдегид защищается р-рителем в виде азометина:
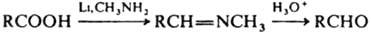
Др. методы восстановления до альдегида требуют превращ. к-т в их производные. Так, хлорангидриды восстанавливаются до альдегидов на Pd-катализаторах (Розенмунда реакция), хлорангидриды и ангидриды, в т.ч. смешанные, действием Na2Fe(CO)4, иминохлориды - хлористым оловом, арилсульфонилгидразиды ароматич. к-т - термич. разложением в присут. Na2CO3, разл. гетероциклич. производные к-т, напр., иодалкилаты оксазолинов, действием NaBH4. Борогидриды не восстанавливают к-ты, a LiAlH4 восстанавливают их в спирты. При одноэлектронном окислении к-т происходит их декарбоксилирование, приводящее к радикалам и далее к карбкатионам:

В зависимости от условий при превращ. радикалов и карбкатионов образуются разл. продукты: алканы, алкены, алкилгалогениды (см. Декарбоксилирование, Бородина-Хунсдиккера реакция, Кольбе реакции). Электроноакцепторные св-ва группы СООН (константа Тафта s* = 2,1) проявляются в избират. a-галогенировании насыщ. к-т:
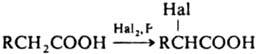
Наряду с прямым галогенированием в присут фосфора и его производных (Гелля-Фольгарда-Зелинского реакция), используется также взаимод. с N-хлор- и N-бромсукцинимидами и иодирование в присут. SOCl2. При свободнорадикальном хлорировании в сильнокислой среде к-т от С4 и выше образуются преим. продукты хлорирования по атому С-4. Отрицат. мезомерный эффект группы СООН (константы Гаммета sм = 0,37, sn = 0,45) дезактивирует бензольное кольцо ароматич. к-т, вследствие чего не удается провести их алкилирование и ацилирование. Галогенирование ароматич. к-т приводит к мета-производным. Ароматич. к-ты легко восстанавливаются металлами в жидком NH3, образуя дианион, протонируемый и алкилируемый по a-положению, напр.:

В аналогичных условиях восстанавливаются двойные связи a,b-непредельных к-т. К. к. с несопряженными двойными связями восстанавливаются каталитически. Особая р-ция b, g- и g,d-ненасыщ. к-т - галолактонизация, т.е. образование галогензамещенных лактонов:

Получение. В пром-сти наиб. распространены окислительные и гидролитич. методы, а также гидрокарбонилирование. Окисление в присут. солей Со, Mn, Fe, Ni, Се применяют, напр., при получении к-т из альдегидов, уксусной к-ты из бутана, бензойной к-ты из толуола. Гидрокарбонилирование (гидрокарбоксилирование) проводят присоединением СО и Н2О к алкенам, алкинам, арил(алкил)галогенидам и тозилатам ароматич. и алифатич. спиртов под давлением в присут. катализаторов - комплексов Ph3P с солями Pd, p-аллильных комплексов Ni либо действием карбонилов Ni или Со, напр.
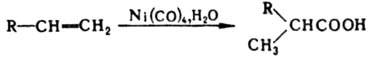
См. также Карбонилирование, Коха-Хаафа реакция. Для получения высших жирных к-т используют гидролиз животных жиров и растит масел, для получения w-галогенкарбоновых к-т гидролиз трихлорметильной группы продуктов теломеризации олефинов и ССl4. Применяется также щелочное плавление спиртов, получаемых оксосинтезом (до С10):
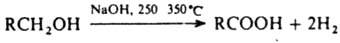
Уксусную и масляную к-ты получают брожением. Для препаративного синтеза к-т используют окисление первичных спиртов и альдегидов. Окислители - соед. Сr, Мn, в т.ч. солюбилизированный краун-6-эфиром КМnО4 в бензоле "пурпурный бензол", кислород в присут. катализаторов (соли Со, Fe, Се) или без них, НIO4 и ее соли, NaClO4, система RuO2 + КIO4, а также электрохим. окисление. К. к. могут быть получены также окислением арилметилкетонов, алкенов, алкинов, напр.:

Их также синтезируют карбоксилированием металлоорг. соед. или действием СО2 на алкилиденфосфораны (илиды фосфора):
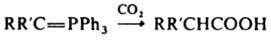
Гидролиз эфиров, амидов, нитрилов и др. производных к-т является как самостоят. методом получения к-т, так и составной частью мн. методов их синтеза, в т.ч. синтезов с эфирами малоновой и ацетоуксусной к-т, р-ции Реформатского. Классич. гидролиз эфиров включает разрыв О-ацильной связи под действием щелочи или к-ты. Более мягкие и избират методы гидролиза эфиров - О-алкильное расщепление их метиловых эфиров с помощью Li в ДМФА, этантиолята Li, NaCN в гексаметаполе, BF3 в СН2Сl2 и др. Амиды более устойчивы к гидролизу, чем эфиры, но легко гидролизуются с помощью Н2О2 в щелочной среде или нитрит-иона в кислой. К. к. получают также введением в орг. молекулу a-карбоксиалкильной СН2СООН или карбоксиалкилиденовой =СНСООН групп. К этим методам относятся классич. синтезы на основе производных малоновой и ацетоуксусной к-т и р-ции производных уксусной к-ты. Превращ. диэтилового эфира малоновой к-ты в анион под действием оснований и его алкилирование галогеналкилами приводит к эфирам замещенных малоновой к-ты, деалкоксикарбонилирование и гидролиз к-рых дает к-ты:

Применение диизопропиламида лития и др. аналогичных амидов позволило получать устойчивые дианионы монокарбоновых к-т и непосредственно вводить группу —СН2СООН:
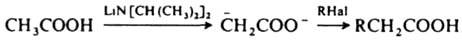
Др. способ введения этой группы р-ции эфиров a-галогенкарбоновых к-т с карбонильными соед. в присут. Zn или с алкилиденфосфораном и послед. гидролиз (см. Реформатского реакция, Виттига реакция). Используют также радикальное присоединение эфиров к-т к алкенам или аренам в присут. пероксидов, напр.:
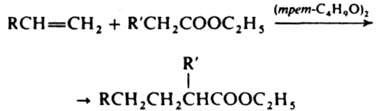
Для получения к-т из кетонов используют Байера-Виллигера реакцию. Галоформную реакцию, из альдегидов Канниццаро реакцию К-ты синтезируются с помощью перегруппировок и р-ций конденсации (см. Дарзана реакция, Кнёвенагеля реакция, Михаэля реакция, Перкина реакция, Фаворского реакции). Имеется неск. методов, применяемых только для синтеза ароматич. К. к., напр., карбоксилирование фенолятов металлов (Кольбе-Шмитта реакция)и р-ция Фриделя - Крафтса с использованием фосгена:

Разработаны спец. методы превращ. к-т в высшие гомологи, напр. Арндта- Айстерта реакция, и перевод в низший гомолог:
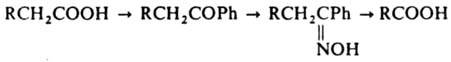
Определение. Качеств. анализ основан на определении рН водных или водно-спиртовых р-ров, выделении к-тами СО2 из р-ров NaHCO3, образовании нерастворимых солей Рb и Ag. Цветная р-ция - превращ. К. к. в гидроксамовые к-ты и образование окрашенных гидроксаматов Fe. К-ты образуют ряд производных с четкой т-рой плавления, применяемых для их идентификации (анилиды, фенациловые эфиры, уреиды, соли S-бензилизотиурония, гидразиды). Методы количеств. анализа включают водное и неводное титрование, определение активного водорода, напр., методом Церевитинова, превращ. в гидроксамовые к-ты и их колориметрич. определение, этерификацию метанолом и определение кол-ва выделившейся воды реактивом Фишера, декарбоксилирование и определение выделившегося СО2. Широко используются тонкослойная и газожидкостная хроматографии.
Применение. К-ты исходные соед. для получения промежут. продуктов орг. синтеза, в частности кетенов, галогенангидридов, виниловых эфиров, галогенкислот. Соли К. к. и щелочных металлов применяют как мыла, эмульгаторы, смазочные масла; соли тяжелых металлов - сиккативы, инсектициды и фунгициды, катализаторы. Эфиры к-т - пищ. добавки, р-рители; моно- и диэфиры гликолей и полигликолей пластификаторы, компоненты лаков и алкидных смол; эфиры целлюлозы - компоненты лаков и пластмассы. Амиды к-т эмульгаторы и флотоагенты. Об индивидуальных к-тах см., напр., в ст. Акриловая кислота, Бензойная кислота. Масляная кислота, Муравьиная кислота, Уксусная кислота. Лит.: Общая органическая химия, пер. с англ., т. 4, М., 1983, с. 11-137; The chemistry of carboxylic acids and esters, ed. by S. Patai, L, 1969; The chemistry of acid derivatives, ed. by S. Patai, pt. 1-2, N.Y., 1979. Д. В. Иоффе.


