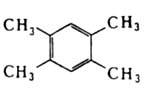
ДУРОЛ (1, 2, 4, 5-тетраметилбензол), мол. м. 134,212; бесцв. кристаллы с моноклинной решеткой, пространств. группа с22n; т. пл. 79,24 °С, т. кип. 196,8°С, 73,5°С/10 мм рт. ст.; возгоняется; d481,3 0,8380, nD81,3 1,47896; tкрит 411,4°С, pкрит 3,16 МПа, dкрит 0,306 г/см3; DH0исп 45,59 кДж/моль,
DH0обр (жидкость) — 98,46 кДж/моль; не раств. в воде, раств. в этаноле, диэтиловом эфире, бензоле, уксусной к-те, перегоняется с водяным паром. При взаимод. с 1,3,5-тринитробензолом Д. образует молекулярное соединение (т. пл. 92-98 °С), применяемое при синтезе красителей; при окислении в жестких условиях (кат. - V2O5) пиромеллитовый диангидрид. Разб. HNO3 последовательно окисляет Д. в 2,4,5-триметилбензойную к-ту, 2,5-диметилтерефталевую к-ту. Хлорметилированием Д. (в присут. ZnCl2) получают 1,4-дихлорметилдурол промежут. продукт в произ-ве антиоксидантов, лек. в-в, полиэфиров; хлорированием при УФ облучении продукты замещения атомов водорода метильных групп на атомы хлора, используемые как инсектофунгициды; ацилированием кетоны, к-рые превращают в винильные производные и применяют в произ-ве полимеров. Д. содержится в нефти и кам.-уг. смоле. В пром-сти его выделяют из продуктов каталитич. риформинга бензинов. Синтезируют метилированием псевдокумола и др. метилбензолов метанолом в присут алюмосиликатного или цеолитного катализатора, а также конденсацией псевдокумола с формальдегидом и послед. гидрокрекингом образовавшегося дифенилметана. Д. умеренно токсичен; ЛД50 3,4 г/кг (белые мыши); ПДК 50 мг/м3 (расчетная). Лит.: Сулимов А. Д. Производство ароматических углеводородов из нефтяного сырья, М., 1975. Свойства органических соединений. Справочник. Л., 1984. Earhart Н. W. Polymethylbenzenes 1969. Park Ridge (N. Y.) L., [1969] В. Я. Данюшевский.

DH0обр (жидкость) — 98,46 кДж/моль; не раств. в воде, раств. в этаноле, диэтиловом эфире, бензоле, уксусной к-те, перегоняется с водяным паром. При взаимод. с 1,3,5-тринитробензолом Д. образует молекулярное соединение (т. пл. 92-98 °С), применяемое при синтезе красителей; при окислении в жестких условиях (кат. - V2O5) пиромеллитовый диангидрид. Разб. HNO3 последовательно окисляет Д. в 2,4,5-триметилбензойную к-ту, 2,5-диметилтерефталевую к-ту. Хлорметилированием Д. (в присут. ZnCl2) получают 1,4-дихлорметилдурол промежут. продукт в произ-ве антиоксидантов, лек. в-в, полиэфиров; хлорированием при УФ облучении продукты замещения атомов водорода метильных групп на атомы хлора, используемые как инсектофунгициды; ацилированием кетоны, к-рые превращают в винильные производные и применяют в произ-ве полимеров. Д. содержится в нефти и кам.-уг. смоле. В пром-сти его выделяют из продуктов каталитич. риформинга бензинов. Синтезируют метилированием псевдокумола и др. метилбензолов метанолом в присут алюмосиликатного или цеолитного катализатора, а также конденсацией псевдокумола с формальдегидом и послед. гидрокрекингом образовавшегося дифенилметана. Д. умеренно токсичен; ЛД50 3,4 г/кг (белые мыши); ПДК 50 мг/м3 (расчетная). Лит.: Сулимов А. Д. Производство ароматических углеводородов из нефтяного сырья, М., 1975. Свойства органических соединений. Справочник. Л., 1984. Earhart Н. W. Polymethylbenzenes 1969. Park Ridge (N. Y.) L., [1969] В. Я. Данюшевский.


