1,8-бис-(ДИМЕТИЛАМИНО)НАФТАЛИН,
мол. м. 214,31; бесцв. кристаллы, темнеющие на воздухе; т. пл. 47-48°С
(из водного спирта); хорошо раств. в большинстве орг. р-рителей, плохо -в воде.
Решетка орторомбич. (а = 1,2855 нм, b = 1,0110 нм, с = 0,9664
нм; пространств. группа Р212121; z =
4).
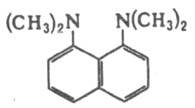
Из-за сильного отталкивания диметиламиногрупп плоскостной характер нафталинового кольца в молекуле Д. сильно нарушен; расстояния между атомами углерода в положениях 1 и 8, 4 и 5 составляют соотв. 0,2562 нм и 0,2443 нм. Д. - сильный донор электронов, о чем свидетельствуют пониж. потенциалы ионизации: при отрыве по одному п- и p-электрону они составляют соотв. 7,05 и 7,47 эВ. Потенциалы электрохим. окисления (в CH3CN; 20 °С, относительно насыщенного каломельного электрода) также низки: E1 = 0,36, Е2 = 1,02 В (две одноэлектронные волны). Для Д. характерны: очень высокая основность [рКa 12,34 (вода; 20 °С), 18,18 (CH3CN; 20°С], обусловленная большим энергетич. выигрышем при превращении Д. в катион I, в к-ром отсутствует отталкивание диметиламиногрупп и реализуется прочная водородная связь; низкая нуклеофильность, связанная с малым расстоянием между диметиламиногруппами, в результате чего Д. реагирует только с протоном. Именно благодаря этому св-ву Д. применяют в орг. синтезе. Его используют в тех случаях, когда от к.-л. молекулы надо отщепить протон, не затронув при этом др. высокоэлектрофильные и неустойчивые по отношению к основаниям группировки. Высокая термодинамич. стабильность катиона I сочетается с весьма низкими скоростями
присоединения протона к Д. и депротонирования катиона I под действием щелочей. Это напоминает св-во обычной губки медленно впитывать воду и с трудом отдавать ее. Поэтому Д. называют "протонная губка".
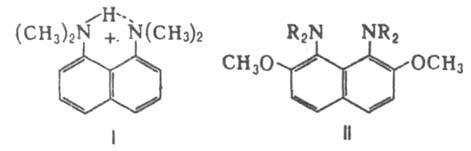
Известно много аналогов Д. Так, соединения II (R = СН3 или С2Н5) - самые сильные из всех известных нейтральных орг. оснований (рКа 16,1 и 16,3 соотв., вода, 20 °С). Однако удерживание протона в катионах этих соед. очень велико, что затрудняет их практич. использование.
Д. получают метилированием 1,8-диаминонафталина (лучше всего СН3l в системе КОН - ДМСО) или восстановлением иодида 1,3,3-триметил-2,3-дигидроперимидиния действием LiAlH4. Хранят Д. в темной стеклянной таре в атмосфере инертного газа или в виде соли с НСlО4.
Лит.: Курасов Л. А., Пожарский А. Ф., Кузьменко В. В., "Ж. орган. химии", 1981, т. 17, в. 9, с. 1944-47; Alder R. W. [а. о.], "Chem. Commun.", 1968, № 13, p. 723-24; Alder R. W. [a.o.], "J. Chem. Soc. Perkin Trans.", 1, 1981, № 11, p. 2840 47. А. Ф. Пожарский.


