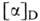 + 16,1 (23 С; 3,6 г в 100мл Н2О). Для D-изомера
+ 16,1 (23 С; 3,6 г в 100мл Н2О). Для D-изомера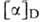 - 8,9° (25 °С; 2 г в 100 мл Н2О). Г. плохо раств. в воде и эта-ноле,
не раств. в эфире. При 25 °С рКа 2,17 (СООН), 9,13
- 8,9° (25 °С; 2 г в 100 мл Н2О). Г. плохо раств. в воде и эта-ноле,
не раств. в эфире. При 25 °С рКа 2,17 (СООН), 9,13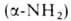 и 5,65
и 5,65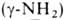 ; р/ 5,65.
; р/ 5,65.
По хим. св-вам Г.-типичная алифатич.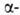 аминокислота.
При взаимод. с H2SO4 или ферментом глутаминазой гидролизуется
амидная связь и выделяется NH3, что используется для количеств.
определения Г. Осаждается нитратом ртути. При синтезе из Г. пептидов наряду
с
аминокислота.
При взаимод. с H2SO4 или ферментом глутаминазой гидролизуется
амидная связь и выделяется NH3, что используется для количеств.
определения Г. Осаждается нитратом ртути. При синтезе из Г. пептидов наряду
с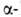 NН2-группой
(см. Аминокислоты)защищают у-амидную группу, для чего в нее вводят
бензгидрильную, 4,4'-диметоксибензгидрильную или ксантенильную группу.
Возможен также синтез пептидов с незащищенной амидной группой с использованием
реакционноспособных эфиров Г., напр. n-нитрофениловых или N-гидроксисукцинимидных
(т. наз. метод активиров. эфиров).
NН2-группой
(см. Аминокислоты)защищают у-амидную группу, для чего в нее вводят
бензгидрильную, 4,4'-диметоксибензгидрильную или ксантенильную группу.
Возможен также синтез пептидов с незащищенной амидной группой с использованием
реакционноспособных эфиров Г., напр. n-нитрофениловых или N-гидроксисукцинимидных
(т. наз. метод активиров. эфиров).
L-Г. встречается во всех организмах в своб. виде (в свекле до 5,6%)
и в составе белков. Для опухолевых клеток L-Г.-незаменимый компонент, на
чем основан один из подходов в создании противоопухолевых препаратов (напр.,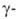 гидрокси-Д-глутамин - антиметаболит для опухолевых тканей). Изомер Г.-D-изоглутамин
(
гидрокси-Д-глутамин - антиметаболит для опухолевых тканей). Изомер Г.-D-изоглутамин
(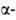 амид D-глутаминовой
к-ты) входит в состав гликопептидов клеточных стенок бактерий. L-Г.-промежут.
продукт ассимиляции азота в организме, участвует в переаминировании. Его
биосинтез осуществляется в результате амидирования карбоксильной группы
глутаминовой к-ты.
амид D-глутаминовой
к-ты) входит в состав гликопептидов клеточных стенок бактерий. L-Г.-промежут.
продукт ассимиляции азота в организме, участвует в переаминировании. Его
биосинтез осуществляется в результате амидирования карбоксильной группы
глутаминовой к-ты.
Выделяют L-Г. из свеклы и др. растений. В спектре ЯМР в D2O
хим. сдвиги протонов у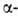 ,
,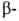 и
и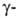 атомов
С составляют соотв. 3,78; 2,142 и 2,259 м.д. Он применяется для синтеза
пептидов, в смеси с др. аминокислотами-для парэнтерального питания. Мировое
произ-во L-Г. 500 т/год (1982). В.В.Баев.
атомов
С составляют соотв. 3,78; 2,142 и 2,259 м.д. Он применяется для синтеза
пептидов, в смеси с др. аминокислотами-для парэнтерального питания. Мировое
произ-во L-Г. 500 т/год (1982). В.В.Баев.


