ГАЛОГЕНОСПИРТЫ
(галогенгидрины), алифатич. соед., содержащие в молекуле гидроксильную
группу и атомы галогенов. Назв. Г. производят от назв. спирта с указанием
числа атомов галогена и их положения относительно группы ОН, напр. СН2С1СН2ОН-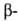 хлорэтанол,
СН2С1СНС1СН2ОН-
хлорэтанол,
СН2С1СНС1СН2ОН-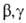 -дихлорпропанол.
-дихлорпропанол.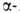 Г. (кроме фторметанола) легко разлагаются, напр.: С1СН2ОН ->
СН20 + HCL
Г. (кроме фторметанола) легко разлагаются, напр.: С1СН2ОН ->
СН20 + HCL
Г. вступают
в р-ции, характерные для спиртов и галогензамещенных углеводородов.
Кислотность
гидроксильной группы возрастает с увеличением электроотрицательности и
числа атомов галогенов. Последние в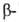 Г.
и несколько меньше в
Г.
и несколько меньше в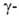 Г.
легче подвергаются нуклеоф. замещению, чем в галогеналканах.
Г.
легче подвергаются нуклеоф. замещению, чем в галогеналканах.
В присут.
оснований Г. циклизуются:
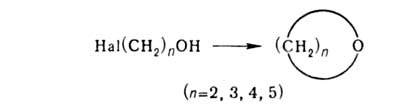
Третичные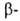 хлоро-
и
хлоро-
и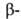 иодоспирты
претерпевают под действием солей Ag или Hg г а л о г е н г и д р и н н
у ю перегруппировку, напр.:
иодоспирты
претерпевают под действием солей Ag или Hg г а л о г е н г и д р и н н
у ю перегруппировку, напр.:
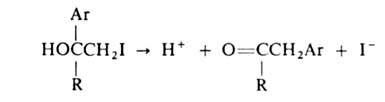
Общий
метод получения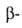 Г.-гипогалогенирование
олефинов:
Г.-гипогалогенирование
олефинов:
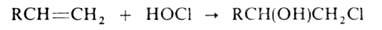
Присоединение
происходит в осн. по правилу Марковникова.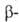 Г.
получают также взаимод. эпоксидов с галогено-водородами или к-тами Льюиса;
присоединением комплекса Ag-соли карбоновой к-ты с галогеном к олефинам
в среде СС14 или СНС13 с послед. гидролизом ацилированного
галогенгидрина (р-ция Прево).
Г.
получают также взаимод. эпоксидов с галогено-водородами или к-тами Льюиса;
присоединением комплекса Ag-соли карбоновой к-ты с галогеном к олефинам
в среде СС14 или СНС13 с послед. гидролизом ацилированного
галогенгидрина (р-ция Прево).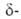 Г.
синтезируют фотохим. или термич. изомеризацией алкилгипохлоритов. Общие
методы синтеза Г.-замещение одной гидроксильной группы в
Г.
синтезируют фотохим. или термич. изомеризацией алкилгипохлоритов. Общие
методы синтеза Г.-замещение одной гидроксильной группы в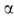 ,
,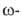 гликолях,
восстановление галогенкарбоновых к-т, замещение хлора в хлоргидринах на
атом др. галогена.
гликолях,
восстановление галогенкарбоновых к-т, замещение хлора в хлоргидринах на
атом др. галогена.
Г.-промежут.
продукты пром. орг. синтеза. Этиленхлоргидрин используется для получения
этиленоксида и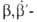 дихлордиэтилового эфира (хлорекса), для оксиэтилирования аминов и фенолов
в произ-ве красителей и лек. в-в; пропиленхлоргидрин применяют для получения
пропиленоксида; 1,3-дихлоргидрин глицерина (вместе с 1,2-изомером) - для
синтеза эпихлоргидрина и глицерина; ди- и три-хлоргидрины пентаэритрита
- для получения 3,3-бис-(хлорметил)оксациклобутана. 1,1,1-Трихлор-2-метилпропанол
(хлорэтон) - лекарств. ср-во. См. также Этиленхлоргидрин.
дихлордиэтилового эфира (хлорекса), для оксиэтилирования аминов и фенолов
в произ-ве красителей и лек. в-в; пропиленхлоргидрин применяют для получения
пропиленоксида; 1,3-дихлоргидрин глицерина (вместе с 1,2-изомером) - для
синтеза эпихлоргидрина и глицерина; ди- и три-хлоргидрины пентаэритрита
- для получения 3,3-бис-(хлорметил)оксациклобутана. 1,1,1-Трихлор-2-метилпропанол
(хлорэтон) - лекарств. ср-во. См. также Этиленхлоргидрин.
Г. поражают нервную систему. наиб. токсичны фторсодержащие спирты; напр., для фторэтанола и 4-фторбутанола ЛД5о 15 мг/кт и 0,9 мг/кг соотв. (белые мыши, перорально). Д.В.Иоффе.


