ВАЛЕНТНОСТЬ (от лат. valentia - сила), способность атома присоединять или замещать определенное число др. атомов или атомных групп с образованием хим. связи. Количеств. мерой В. атома элемента Э служит число атомов водорода или кислорода (эти элементы принято считать соотв. одно- и двухвалентными), к-рые Э присоединяет, образуя гидрид ЭНx или оксид ЭnОm. В. элемента м.б. определена и по др. атомам с известной валентностью. В разл. соединениях атомы одного и того же элемента могут проявлять разл. В. Так, сера двухвалентна в H2S и CuS, четырехвалентна в SO2 и SF4, шестивалентна в SO3 и SF6. До развития электронных представлений о строении в-ва В. трактовалась формально. В рамках электронной теории химической связи В. атома определяется числом его неспаренных электронов в основном или возбужденном состоянии, участвующих в образовании общих электронных пар с электронами др. атомов. Поскольку электроны внутр. оболочек атома не участвуют в образовании хим. связей, макс. В. элемента считают равной числу электронов во внеш. электронной оболочке атома. Макс. В. элементов одной и той же группы периодич. системы обычно соответствует ее порядковому номеру. Напр., макс. В. атома С должна быть равной 4, С1 - 7. Электростатич. теория хим. связи привела к формулировке близкого к В. и дополняющего ее понятия степени окисления (окислит. числа), соответствующей заряду, к-рый приобрел бы атом, если бы все электронные пары его хим. связей сместились в сторону более электроотрицат. атомов. При этом электронные пары, обобщенные одинаковыми атомами, делятся пополам. По знаку степень окисления, как правило, совпадает с экспериментально определяемым эффективным зарядом атома, но численно намного превышает его. Напр., степень окисления серы в SO3 равна +6, а ее эффективный заряд - ок. + 2.
Развитие представлений о донорно-акцепторных связях (см. Координационная
связь), водородной связи, обнаружение новых классов хим. соед. (мостиковых
электронодефицитных, металлоорг., сэндвичевых, металлич. кластеров,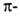 комплексов), а также исследования кристаллич. структур показали ограниченность
правил определения формальной В. Было найдено, что координац. числа атомов
могут превышать их формальную В. Так, атом С в карбонильном кластере [CFe5(CO)15]
связан с 5 атомами Fe, в анионе [ССо8(СО)18]2-
- с 8 атомами Со. Хим. связь в подобных соед. не м. б. описана с
помощью представлений о двух-электронных двухцентровых связях и обусловлена
образованием много центровой связи.
комплексов), а также исследования кристаллич. структур показали ограниченность
правил определения формальной В. Было найдено, что координац. числа атомов
могут превышать их формальную В. Так, атом С в карбонильном кластере [CFe5(CO)15]
связан с 5 атомами Fe, в анионе [ССо8(СО)18]2-
- с 8 атомами Со. Хим. связь в подобных соед. не м. б. описана с
помощью представлений о двух-электронных двухцентровых связях и обусловлена
образованием много центровой связи.
Термин "В." введен в 60-х гг. 19 в. На представлениях о В. была основана классич. теория хим. строения A.M. Бутлерова. В совр. теории хим. строения представления о В. часто отождествляют с общим учением о хим. связи.
Лит.: Коулсон Ч., Валентность, пер. с англ., М., 1965; Развитие
учения о валентности, под ред. В. И. Кузнецова, М., 1977; Картмелл Э.,
Фоулз Г., Валентность и строение молекул, пер. с англ., М., 1979. В.
И. Минкин.


