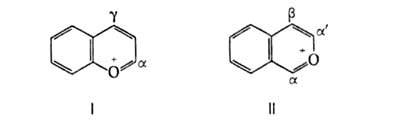
Соед. I не обменивает атом кислорода на др. гетеро-атомы и не превращ.
в замещенные нафталина. Из его производных наиб. реакционноспособны соли
со своб.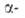 и
и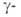 положениями или содержащие в этих положениях функц. группы (Cl, OR и др.).
Атака нуклеоф. агентов (метиленовые соед., эфиры фенолов, диалкиланилины,
аминокислоты и др.) по
положениями или содержащие в этих положениях функц. группы (Cl, OR и др.).
Атака нуклеоф. агентов (метиленовые соед., эфиры фенолов, диалкиланилины,
аминокислоты и др.) по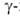 положению
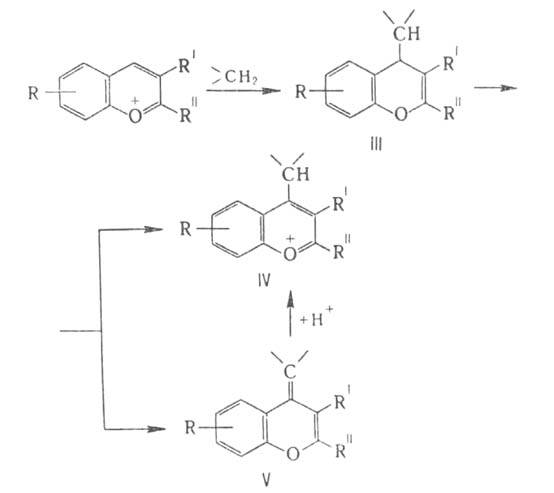
приводит к образованию аддукта III, новой соли бензопирилия IV или ее ангидроосновання
V:
положению
приводит к образованию аддукта III, новой соли бензопирилия IV или ее ангидроосновання
V:
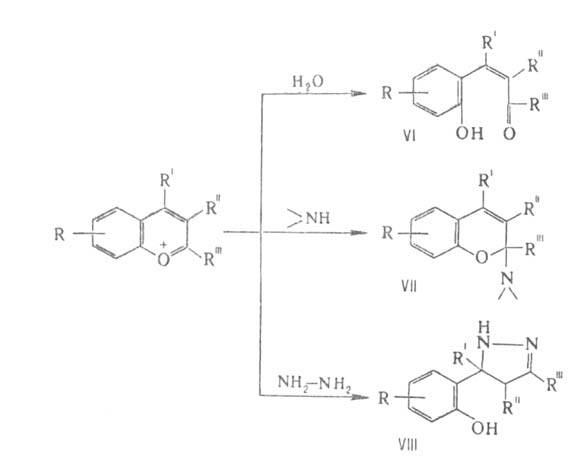
Присоединение нуклеофила в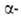 положение
обычно ведет к образованию о-гидроксихалконов (VI), аддуктов VII или VIII,
напр.:
положение
обычно ведет к образованию о-гидроксихалконов (VI), аддуктов VII или VIII,
напр.:
Соед. I способны к димеризации через присоединившийся нуклеофил,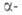 и
и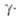 алкильные
группы либо непосредственно через гетерокольцо.
алкильные
группы либо непосредственно через гетерокольцо.
Для соед. II нуклеоф. присоединение идет в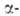 положение
с образованием после рециклизации новой гетероциклич. системы (IX) или
положение
с образованием после рециклизации новой гетероциклич. системы (IX) или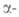 производных
нафталина (X), реже - в положение
производных
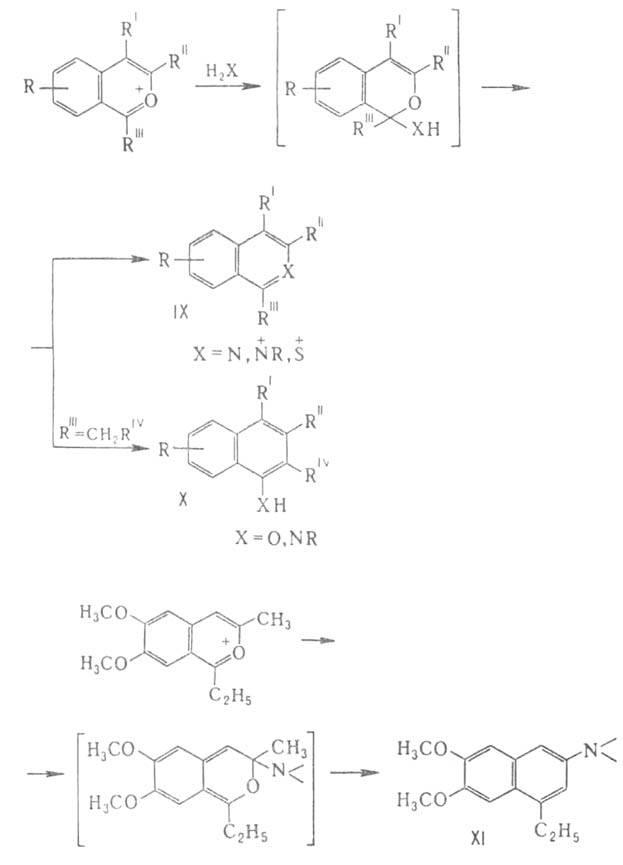
нафталина (X), реже - в положение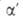 с образованием
с образованием производных
нафталина, напр. (XI):
производных
нафталина, напр. (XI):
1-Метилзамещенные II со своб. положением
легко образуют замещенные хризены, напр.:
положением
легко образуют замещенные хризены, напр.:
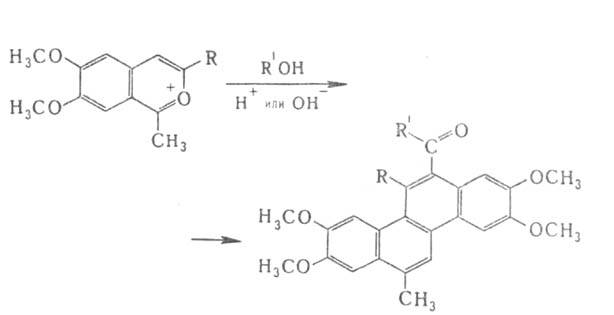
где R = Alk, Аг.
Общим для Б.с. обеих структур является существование в их р-рах равновесия
между ионной формой и псевдооснованием, а при наличии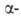 или
или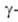 алкильных
групп - ангидрооснованием, напр.:
алкильных
групп - ангидрооснованием, напр.:
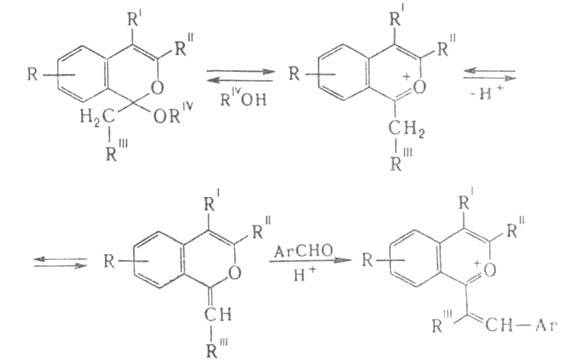
Получают Б. с. из соед., содержащих пирановый цикл, а также конденсационными
методами, напр.:
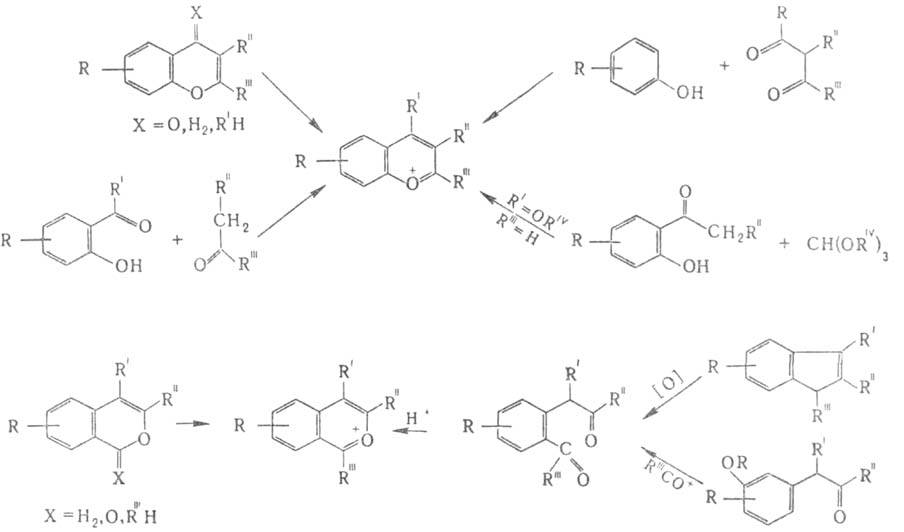
Полигидроксизамещенные I-структурные фрагменты антоцианов. Соед. II в природе не найдены.
Б.с. - ингибиторы коррозии, фото- и термохромы, сенсибилизаторы, люминофоры. Нек-рые Б. с. используются в синтезе изохинолиновых оснований и прир. алкалоидов.
Лит.: Джоуль Д., Смит Г., Основы химии гетероциклических соединений, пер. с англ., М., 1975; Щербакова И. В., Кузнецов Е. В., Химия гетероциклических соединений. 198Z № 4, с. 552-53; Коробка И. В.. Кузнецов Е. В.. там же, 1983, № 2, с. 274-81; Balaban А.Т. [а. о.]. Advances in hetcrocyclie chemistry, Suppl. 2, N.Y., 1982; Sham ma M., MoniotJ.-L. Isoquinoline alkaloids research. 1972-1977, N.Y.. 1978. Е.В.Кузнецов.


