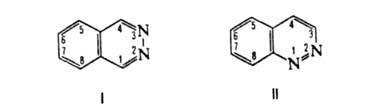
БЕНЗОПИРИДАЗИНЫ, мол. м. 121,14. Существуют в виде двух изомеров
- бензо[d]пиридазина, или фталазина (ф-ла I), и бензо[с]пиридазина, или
циннолина (II).
Светло-желтые кристаллы (см. табл.); хорошо раств. в воде, спирте, бензоле, хлороформе.
СВОЙСТВА ИЗОМЕРНЫХ БЕНЗОПИРИДАЗИНОВ

Электроф. замещение идет в Б. гл. обр. в положения 5 и 8; реакц. способность
др. положений для циннолина уменьшается в ряду 6, 7>3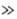 4.
Группы Hal, CH3SO2, CH3SO, NO2,
SH в положениях 1 и 4 фталазина, 3 и 4 циннолина, а также Hal в бензольном
кольце легко замещаются при р-циях Б. с алкоголятами, аминами, NH3,
гидразином. Алкилзамещенные в положениях 1 и 4 для фталазина или 4 для
циннолина конденсируются с хлоралем, бензальдегидом, фталевым ангидридом.
При окислении щелочным р-ром КМnО4 фталазин образует пиридазин-4,5-дикарбоновые
к-ты, а циннолин-пиридазин-3,4-дикарбоновые к-ты. Окисление фталазина монопероксифталевой
к-той, а циннолина - Н2О2 в уксуснокислой среде приводит
к N-оксидам. Фталазин получают взаимод. фталевого альдегида со спиртовым
р-ром гидразингидрата:
4.
Группы Hal, CH3SO2, CH3SO, NO2,
SH в положениях 1 и 4 фталазина, 3 и 4 циннолина, а также Hal в бензольном
кольце легко замещаются при р-циях Б. с алкоголятами, аминами, NH3,
гидразином. Алкилзамещенные в положениях 1 и 4 для фталазина или 4 для
циннолина конденсируются с хлоралем, бензальдегидом, фталевым ангидридом.
При окислении щелочным р-ром КМnО4 фталазин образует пиридазин-4,5-дикарбоновые
к-ты, а циннолин-пиридазин-3,4-дикарбоновые к-ты. Окисление фталазина монопероксифталевой
к-той, а циннолина - Н2О2 в уксуснокислой среде приводит
к N-оксидам. Фталазин получают взаимод. фталевого альдегида со спиртовым
р-ром гидразингидрата:
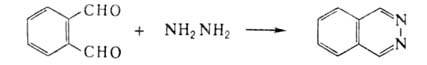
Производные фталазина, не имеющие заместителей в бензольном кольце,
образуются по р-циям:
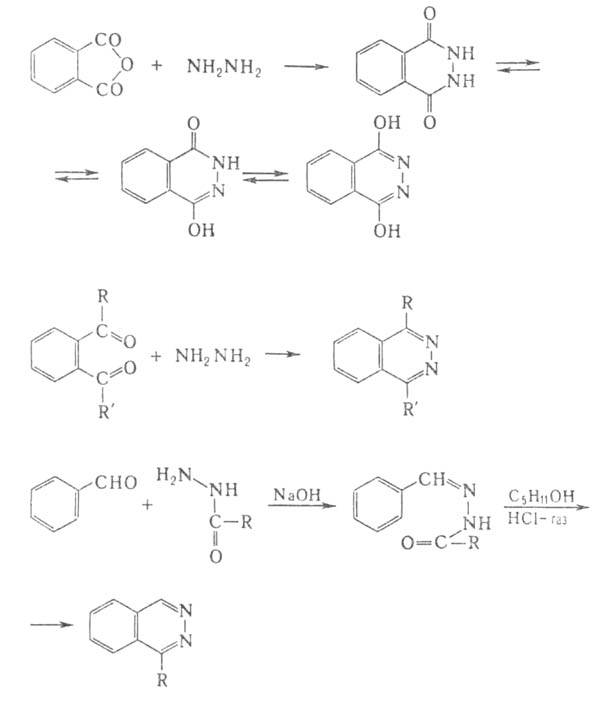
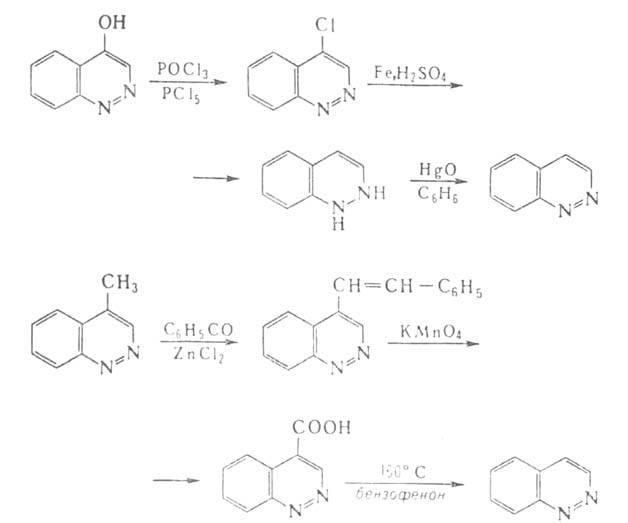
Циннолин синтезируют из 4-гидроксициннолина, восстанавливая промежут.
хлорпроизводное, или из 4-метилциннолина, напр.:
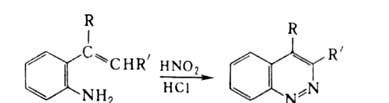
Внутримолекулярная циклизация производных о-аминостирола или о-аминоацетофенона
приводит соотв. к замещенным циннолина или 4-гидроксициннолина, напр.:
Производные 4-гидроксициннолина получают также по р-ции:
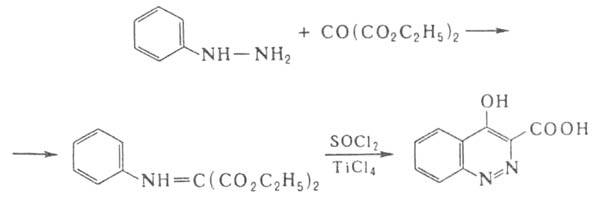
Гидрохлорид 1-гидразинофталазина (апрессин) и 1,4-дигидразинофталазина (непрессол) - спазмолитич. и гипотензивное ср-во. Циннолин токсичен.
Лит.: Иванекий В. И., Химия гетероциклических соединений, М.. 1978; Гетероциклические соединения, пер. с англ., т. 6, М., 1960, с. 1 17-94: Общая органическая химия, пер. с англ., т. 8, М., 1985, с. 160-64.


