БЕНЗОЙНАЯ КИСЛОТА (бензолкарбоновая к-та) С6Н5СООН,
мол. м. 122,05; бесцв. кристаллы; т. пл. 122,4°С, т. кип. 249,2 °С, 133°С/10
мм рт. ст., т. воз'г. 100°С; d424 1,316;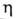 1,67мПа*с(122,5°С), 1,26 мПа*с (130°С);
1,67мПа*с(122,5°С), 1,26 мПа*с (130°С);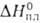 18 ± 0,1 кДж/моль,
18 ± 0,1 кДж/моль,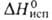 527 Дж/г,
527 Дж/г,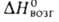 686 Дж/г. Р-римость при 25 °С (г в 100 г р-рителя): в воде-0,34 (1,77 при
70 °С; Nа-соли - 61,2), абс. этаноле - 58,4; эфире - 40,8; бензоле - 12,2.
Б. к. обладает всеми хим. св-вами монокарбоновых к-т. При 370°С она разлагается
до бензола и СО2 (в небольшом кол-ве образуются фенол и СО);
процесс ускоряется в присут. порошкообразных Си или Со. При взаимод. с
бензоилхлоридом при повыш. т-рах Б. к. превращается в бензойный ангидрид
(С6Н5СО)2О - кристаллы; т. пл. 42°С, т.
кип. 360°С; р-римость в воде 0,01 г/л; устойчив в воде и холодных р-рах
щелочей.
686 Дж/г. Р-римость при 25 °С (г в 100 г р-рителя): в воде-0,34 (1,77 при
70 °С; Nа-соли - 61,2), абс. этаноле - 58,4; эфире - 40,8; бензоле - 12,2.
Б. к. обладает всеми хим. св-вами монокарбоновых к-т. При 370°С она разлагается
до бензола и СО2 (в небольшом кол-ве образуются фенол и СО);
процесс ускоряется в присут. порошкообразных Си или Со. При взаимод. с
бензоилхлоридом при повыш. т-рах Б. к. превращается в бензойный ангидрид
(С6Н5СО)2О - кристаллы; т. пл. 42°С, т.
кип. 360°С; р-римость в воде 0,01 г/л; устойчив в воде и холодных р-рах
щелочей.
Б. к. и ее эфиры содержатся в эфирных маслах (напр., в гвоздичном), толуанском и перуанском бальзамах, бензойной смоле. Производное Б. к. и глицина - гиппуровая к-та C6H5CONHCH2COOH-продукт жизнедеятельности животных.
Осн. пром. способ получения Б.к.: жидкофазное окисление толуола воздухом при 130-160°С и давл. 308-790 кПа (кат. - бензоаты Со и Мп, промотированные соединениями Вг); выход близок к теоретическому. Б. к. может быть получена также гидролизом бензотрихлорида С6Н5СС13 или бензонитрила.
Б. к. и ее соли обладают высокой бактерицидной и бактериостатич. активностью, резко возрастающей с уменьшением рН среды. Благодаря этим св-вам, а также нетоксичности Б. к. применяют как консервант в пищ. пром-сти (добавка 0,1% к-ты к соусам, рассолам, фруктовым сокам, джемам, мясному фаршу и др.), антисептик в медицине (гл. обр. в дерматологии), парфюмерии и косметике. Б. к. используют в произ-ве фенола, капролактама, бензоилхлорида, как добавку к алкидным лакам, улучшающую блеск, адгезию, твердость и хим. стойкость покрытия.
Большое практич. значение имеют соли и эфиры Б. к. (бензоаты). Бензоат Na - консервант пищ. продуктов, стабилизатор полимеров, ингибитор коррозии в теплообменниках, отхаркивающее ср-во в медицине. Бензоат аммония (т. возг. 160°С, т. разл. 198 °С) - антисептик, консервант в пищ. пром-сти, ингибитор коррозии, стабилизатор в произ-ве латексов и клеев. Бензоаты переходных металлов - катализаторы жидкофазного окисления алкилароматич. углеводородов в бензойную к-ту. Сложные эфиры Б. к. (см. табл.) от метилового до изоамилового - душистые в-ва. Метил- и этилбензоаты входят в состав эфирных масел -иланг-илангового, туберозы, гвоздики. Метилбензоат -р-ритель эфиров целлюлозы. Изоамилбензоат - компонент фруктовых эссенций. Бензилбензоат - фиксатор запаха в парфюмерии, р-ритель душистых в-в, антисептик, репеллент от моли.
СВОЙСТВА ЭФИРОВ БЕНЗОЙНОЙ КИСЛОТЫ
|
Соединение
|
Т. пл., °С
|
Т. кип., °С/мм рт.ст.
|
d420
|
nD20
|
|
Метилбензоат
|
-12,21
|
199,5; 95/25
|
1,0888
|
1,570
|
|
Этилбензоат
|
-34,7
|
212,4; 106/25
|
1,0468
|
1,5051
|
|
Изоамилбснзоат
|
-
|
262
|
0,9925
|
1,493
|
|
Бензилбензоат
|
21
|
323; 187/20
|
1,1192
|
1,5681
|
Для Б.к. т. воспл. 121-131 °С Раздражает кожу; вдыхание аэрозоля вызывает судорожный кашель, насморк, иногда тошноту и рвоту. Получение Б. к. при сухой перегонке бензойной смолы было описано еще в сер. 16 в.; в 1832 Ф. Вёлер и Ю. Либих установили ее структуру.
Лит.: Гауптман 3., Грефе Ю., Ремане X., Органическая химия, пер.
с нем., М., 1979; Kirk-Othmer encyclopedia, 3 ed, v. 3, N.Y., 1978, p.
778. Ю.Л. Москович.


