БЕНЗОИНОВАЯ КОНДЕНСАЦИЯ, взаимод. двух молекул альдегида
с образованием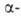 гидроксикетона
(ацилоина):
гидроксикетона
(ацилоина):
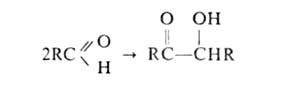
Классич. Б. к.-превращение ароматич. альдегидов в ароматич. апилоины (бензоины), катализируемое цианидами. Вместо последних можно применять тетракис-(диалкил-амино)этилены (источники нуклеоф. карбенов) или четвертичные соли тиазолия в присут. оснований.
С цианидами р-цию проводят в кипящем водно-спиртовом р-ре в течение
1-3 ч. Применение солей тиазолия в присут. триэтиламина позволяет осуществлять
Б. к. в этаноле, диоксане, ДМФА или без р-рителя при комнатной т-ре. Многие
ароматич. альдегиды, с трудом или вовсе не образующие симметричные бензоины,
легко конденсируются с др. альдегидами, образуя несимметричные бензоины,
причем СО-группа в последних располагается у кольца, несущего электронодонорные
заместители, напр.:
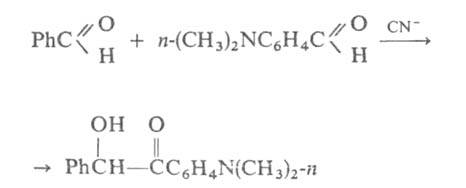
В присут. ионов CN ~ неароматич. альдегиды вступают в Б. к. только с
альдегидами, не содержащими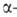 атомов
водорода. Однако применение в кач-ве катализаторов тиазолиевых солей позволяет
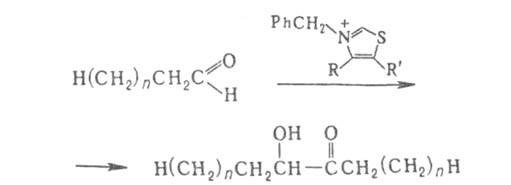
получать ацилоины из алифатич. альдегидов, напр.:
атомов
водорода. Однако применение в кач-ве катализаторов тиазолиевых солей позволяет
получать ацилоины из алифатич. альдегидов, напр.:
Б.к. обратима: обработка цианидом К смеси бензоина с альдегидом или
с др. бензоином приводит к смешанному бензоину:
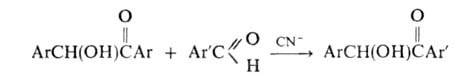
При Б. к. терефталевого альдегида образуется полимер, содержащий бензоиновые
группировки:
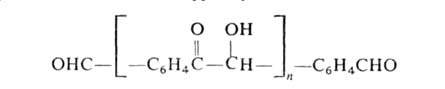
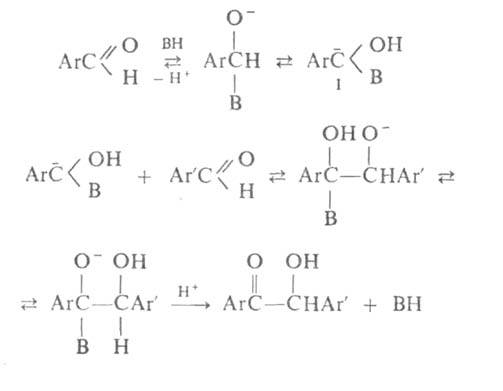
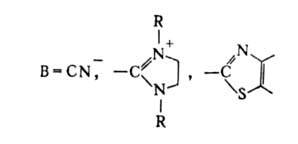
Механизм Б. к. включает стадию образования карбаниона (ф-ла I):
Симметричные и несимметричные бензоины широко используют для синтеза
дезоксибензоинов, бензилов, гидробензоинов,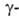 дикетонов,
производных
дикетонов,
производных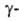 кетокислот
и др.
кетокислот
и др.
Лит.: Общая органическая химия, пер. с англ., т. 2, М., 1982,
с. 739-47; Lappert M. F., Maskell R. К., "J. Chem. Soc. Chemical Communications",
1982, № II, p. 580-81. Н.П. Гамбарян.


